Hintergrund
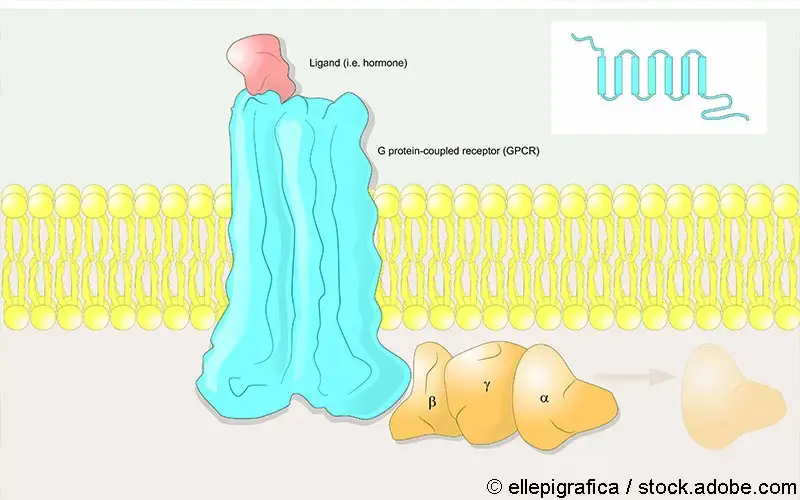
G-Protein-gekoppelte Rezeptoren (GPCR) bilden mit mehr als 1000 Vertretern eine der größten Proteinfamilien. Sie sind für die Weiterleitung zahlreicher extrazellulärer Signale (z.B. Sinnesempfindungen, Hormone und Entzündungsprozesse) in das Zellinnere verantwortlich und Angriffspunkt zahlreicher Medikamente. So sind etwa ein Drittel aller rezeptpflichtigen Arzneimittel gegen GPCR gerichtet. Damit diese ihre Wirkung entfalten und ein bestimmtes Signal auslösen bzw. einen konkreten Signalweg blockieren können, müssen sie nach dem Schlüssel-Schloss-Prinzip in die entsprechende Bindungstasche des jeweiligen Rezeptors passen.
Die Selektivität eines Wirkstoffs ist dabei abhängig von der Passform, und durch eine möglichst präzise Passform werden nicht nur Wirkungen verstärkt, sondern auch Nebenwirkungen minimiert. Häufig sind orthosterische Bindungstaschen bestimmter Rezeptor-Subtypen (z.B. β1 und β2-Rezeptoren) hoch konserviert und zeichnen sich durch nur geringe Unterschiede aus. Das ist ein Grund dafür, dass viele auf orthosterische Bindungstaschen ausgerichtete Arzneistoffe nicht ausreichend selektiv sind. Neben der orthosterischen Tasche, in der Regel Angriffspunkt des endogenen Agonisten, existieren aber auch zahlreiche allosterische Taschen, die Konformationsänderungen des Rezeptors bewirken können und potenzielle Bindungsstellen für synthetische Modulatoren darstellen. Zwar wurde bislang angenommen, dass allosterische Bindungsstellen eine geringere Sequenzhomologie aufweisen als orthosterische, gezeigt worden war es jedoch noch nicht, und nur wenig war bekannt über Ähnlichkeiten und Unterschiede ihrer Form und Sequenz. [1,2].
Zielsetzung
Unter Mitwirkung einer kanadischen Arbeitsgruppe der Université de Montréal setzte sich das Team der Marburger Pharmazeuten zum Ziel, die Bindungstaschen an G-Protein-gekoppelten Rezeptoren zu analysieren und neue Bindungstaschen für G-Protein-gekoppelte Rezeptor-Liganden zu identifizieren, um die Entwicklung maßgeschneiderter Medikamente mit einem Minimum an Nebenwirkungen zu ermöglichen.
Methoden
Mit Hilfe einer computergestützten Analyse wurde an insgesamt 557 Strukturen von 113 verschiedenen GPCR-Proteinen nach alternativen Bindungsstellen gesucht. Dafür wurden verschiedene kleine Moleküle eingesetzt, die an unterschiedliche Stellen der Rezeptorproteine andockten. Anhand des verwendeten Algorithmus konnten durch sie initiierte Effekte simuliert und analysiert werden.
Zwei der neu gefundenen Bindungstaschen wurden exemplarisch für weitergehende experimentelle Untersuchungen genutzt. Dazu wurden der muskarinische Acetylcholinrezeptor Subtyp M3 und der β2-adrenerge Rezeptor als Modellrezeptoren ausgewählt. Für Bindungsstudien sind Mutationen eingefügt und anschließend Funktionsanalysen durchgeführt worden. Darüber hinaus wurden Korrelationen zwischen interhelikalen Kontakten und dem Aktivierungsstatus des Rezeptors analysiert sowie im Hinblick auf ein quantitatives Assessment des Selektivitätspotenzials vergleichende Sequenzanalysen durchgeführt.
Ergebnisse
Alle zuvor identifizierten und bereits bekannten Bindungstaschen wurden anhand der Computeranalyse bestätigt. Darüber hinaus konnten neun neue Bindungstaschen identifiziert werden. Durch Mutationen und funktionelle Analysen an zwei der neu identifizierten Bindungstaschen wurde gezeigt, dass diese Regionen in die Rezeptoraktivierung nach Stimulation mit einem orthosterischen Agonisten involviert sind und eine essenzielle Funktion für die Aktivität des Rezeptors haben.
Im Zusammenhang mit den Kontaktanalysen zeigten die Studienergebnisse, dass Liganden für diese zwei Bindungstaschen als potenzielle negative allosterische Modulatoren (NAMs) fungieren könnten, indem sie Kontakte zerstören, die für einen aktiven Status essenziell sind. Mit dem zielgerichteten Design von Liganden, die den aktiven Status stabilisieren oder die interhelikale Kontakte aufbrechen, die für einen inaktiven Status wichtig sind, könnten dagegen positive allosterische Modulatoren (PAMs) entwickelt werden. Die Autoren geben zu bedenken, dass für ihre Analyse starre Rezeptorstrukturen zugrunde gelegt wurden, bei der Entwicklung passgenauer Liganden jedoch Konformationsänderungen berücksichtigt werden müssen.
Fazit
Mit dieser Studie haben die Forscher die derzeit umfassendste Analyse von Bindungstaschen an G-Protein-gekoppelten Rezeptoren durchgeführt. Neben den bisher bekannten wurden auch neun neue Bindungstaschen identifiziert. Die Ergebnisse dieser Computeranalyse dürften es künftig erleichtern, passgenaue Bindungspartner (Arzneistoffe) für die neu entdeckten Bindungsstellen zu entwickeln. Ein weiterer Schritt auf dem Weg zu zielgerichteten Therapien.










