Apremilast
Apremilast gehört zur Wirkstoffgruppe der Phosphodiesterase-4-Hemmer. Der Wirkstoff wird zur Behandlung von chronischer Plaque-Psoriasis, Psoriasis-Arthritis sowie zur Therapie des Behçet-Syndroms angewendet.
Apremilast: Übersicht
Anwendung
Der PDE-4-Hemmer Apremilast wird zur Behandlung der mittelschweren bis schweren chronischen Plaque-Psoriasis sowie zur Psoriasis-Arthritis eingesetzt. Zudem wird der Wirkstoff zur Therapie von oralen Aphthen, welche mit dem Behçet-Syndrom assoziiert sind, angewendet.
Wirkmechanismus
Apremilast ist ein Hemmstoff der Phosphodiesterase-4 (PDE-4). Der Wirkstoff entfaltet seinen antiphlogistischen Effekt, indem er die Spaltung der Phosphodiesterbindung durch das Enzym und damit den Abbau von zyklischem Adenosinmonophosphat (cAMP) zu Adenosinmonophosphat (AMP) verhindert. Die Isoform 4 der Phosphodiesterase wird in verschiedenen Entzündungszellen, wie zum Beispiel Makrophagen, neutrophilen und eosinophilen Leukozyten, exprimiert.
Über die Degradierung von cAMP durch die PDE-4 wird die Bildung pro- und anti-inflammatorischer Zytokine sowie die Zellproliferation reguliert. Die Inhibierung des Enzyms führt daher zu einem Anstieg der intrazellulären cAMP-Konzentration.
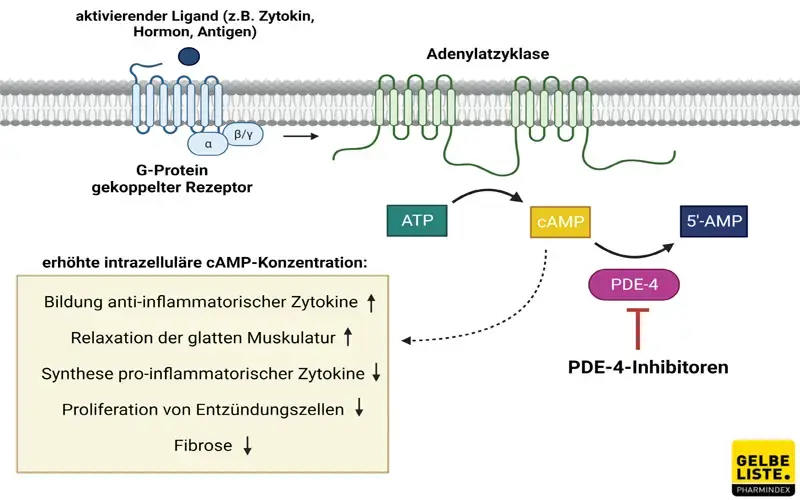
Eine Konsequenz des gestreigerten cAMP-Spiegels ist die Aktivierung der Proteinkinase A (PKA). Dies hat Einfluss auf folgende Signalwege in der Zelle:
- Die Phosphorylierung von CREB ("cAMP response element binding protein) und des Activating Transcription Factor 1 (ATF-1) führt zur Bildung anti-inflammatorischer Zytokine.
- Die Interaktion zwischen NFκB und dem CREB-Bindeprotein (CBP) wird beeinflusst. Dies hat zur Folge, dass die Bildung pro-inflammatorischer Zytokine unterdrückt wird.
- Die durch Bcl-6 (B-cell lymphoma 6 protein)-vermittelte Synthese proinflammatorischer Zytokine und die Proliferation von Entzündungszellen wird ebenfalls verhindert.
Neben der PKA wird durch die erhöhte cAMP-Konzentration auch das Epac-Protein (Isoform 1 und 2) aktiviert. Epac ist ein Guaninnukleotid-Austauschfaktor und ist nach der Bindung von cAMP in der Lage, die sogenannte Rap-GTPase in Gang zu bringen. Dadurch wird die Proliferation von Entzündungszellen sowie die Bildung proinflammatorischer Zytokine unterdrückt.
Pharmakokinetik
Resorption
- Apremilast wird mir einer absoluten oralen Bioverfügbarkeit von etwa 73% gut resobiert.
- Maximale Plasmakonzentrationen (Cmax) werden im Median nach etwa 2,5 Stunden (tmax) erreicht.
- Die Kumulation ist bei einmal täglicher Gabe minimal und beträgt bei zweimal täglicher Gabe bei gesunden Probanden etwa 53% und bei Psoriasis-Patienten 68%.
- Gleichzeitige Nahrungsaufnahme verändert die Bioverfügbarkeit nicht.
Verteilung
- Die Plasmaproteinbindung von Apremilast beträgt etwa 68%.
- Das mittlere scheinbare Verteilungsvolumen (Vd) beträgt 87 Liter, was auf eine extravaskuläre Verteilung hindeutet.
Biotransformation
- Apremilast wird sowohl über CYP-vermittelte als auch über CYP-unabhängige Stoffwechselwege umfassend metabolisiert, unter anderem durch Oxidation, Hydrolyse und Konjugation
- Die vielseitige Metabolisierung lässt darauf schließen, dass es bei Hemmung eines einzelnen Eliminationsweges wahrscheinlich zu keiner ausgeprägten Arzneimittelwechselwirkungen kommt.
- Die oxidative Metabolisierung des Wirkstoffes wird primär von CYP3A4 getragen, wobei in geringerem Maße auch CYP1A2 und CYP2A6 daran beteiligt sind.
- Nach oraler Gabe ist Apremilast die Hauptkomponente im Blutkreislauf.
- Lediglich 3% bzw. 7% werden im Urin bzw. in den Fäzes wiedergefunden.
- Der zirkulierende inaktive Hauptmetabolit ist das Glucoronidkonjugat von O-demethyliertem Apremilast.
Elimination
- Die Plasma-Clearance von Apremilast beträgt bei gesunden Probanden im Durchschnitt etwa 19 Liter pro Stunde, mit einer terminalen Eliminationshalbwertszeit von etwa 9 Stunden.
- Nach oraler Gabe von radioaktiv markiertem Apremilast werden etwa 58% bzw. 39% der Radioaktivität im Urin bzw. in den Fäzes wiedergefunden.
Die Pharmakokinetik von Apremilast ist linear und zeigt einen dosisproportionalen Anstieg der systemischen Exposition im Dosisbereich von 10 bis 100 mg täglich.
Dosierung
Die empfohlene Dosis von Apremilast beträgt 30 mg zweimal täglich, eingenommen im Abstand von etwa 12 Stunden (morgens und abends) und unabhängig von den Mahlzeiten. Ein initiales Titrationsschema ist wie in der nachfolgenden Tabelle dargestellt erforderlich. Nach initialer Titration ist keine erneute Titration erforderlich.
| Tag 1 | Tag 2 | Tag 3 | Tag 4 | Tag 5 | Tag 6 |
| Morgens | Morgens / Abends | Morgens / Abends | Morgens / Abends | Morgens / Abends | Morgens / Abends |
| 10 mg | 10 mg / 10 mg | 10 mg / 20 mg | 20 mg / 20 mg | 20 mg / 30 mg | 30 mg / 30 mg |
Bei Patienten, deren Nierenfunktion stark eingeschränkt ist (mit einer geschätzten Kreatinin-Clearance von weniger als 30 ml pro Minute, basierend auf der Cockroft-Gault-Formel), sollte die Dosis von Apremilast auf 30 mg pro Tag reduziert werden. In dieser Patientengruppe wird empfohlen, bei der initialen Dosistitration Apremilast gemäß dem in der Tabelle angegebenen Schema ausschließlich am Morgen zu titrieren und die Abenddosen auszulassen.
Nebenwirkungen
Die am häufigsten berichteten unerwünschten Arzneimittelwirkungen von Apremilast sind gastrointestinale Störungen, darunter Durchfall (15,7%) und Übelkeit (13,9%). Weiter wurden Infektionen der oberen Atemwege (8,4%), Kopfschmerzen (7,9%) und Spannungskopfschmerzen (7,2%) gemeldet. In der Regel sind diese Nebenwirkungen leicht bis mäßig ausgeprägt.
Zudem traten Oberbauchschmerzen (8,7%), Erbrechen (8,7%) sowie Rückenschmerzen (7,7%) in leichter bis mittelschwerer Ausprägung auf.
Die gastrointestinalen Nebenwirkungen treten in der Regel innerhalb der ersten zwei Wochen der Behandlung auf und klingen in der Regel innerhalb von vier Wochen wieder ab.
Gelegentlich können Überempfindlichkeitsreaktionen auftreten.
Wechselwirkungen
Bei der Anwendung von Apremilast sind folgende Wechselwirkungen zu beachten:
- CYP-Induktoren (z.B. Rifampicin, Phenobarbital, Carbamazepin, Phenytoin und Johanniskraut) können zu einer reduzierten therapeutischen Wirksamkeit von Apremilast führen.
Kontraindikation
Apremilast ist kontraindiziert bei Personen, die eine Überempfindlichkeit gegen den Wirkstoff aufweisen.
Schwangerschaft/Stillzeit
Die Anwendung von Apremilast während der Schwangerschaft und Stillzeit wird nicht empfohlen.
Frauen im gebärfähigen Alter sollten angewiesen werden, während der Behandlung mit Apremilast eine zuverlässige Verhütungsmethode anzuwenden.
Verkehrstüchtigkeit
Apremilast hat keinen oder einen zu vernachlässigenden Einfluss auf die Verkehrstüchtigkeit und die Fähigkeit zum Bedienen von Maschinen.
Anwendungshinweise
- Apremilast sollte bei Kindern und Jugendlichen bis zum Alter von 17 Jahren nicht angewendet werden.
- Es liegen nach Markteinführung Berichte über schwere Fälle von Diarrhoe, Übelkeit und Erbrechen im Zusammenhang mit der Anwendung von Apremilast vor. Die meisten Ereignisse traten innerhalb der ersten Behandlungswochen auf. In manchen Fällen wurden die Patienten in ein Krankenhaus eingewiesen. Bei Patienten ab 65 Jahren besteht möglicherweise ein erhöhtes Risiko für Komplikationen. Wenn Patienten eine schwere Form von Diarrhoe, Übelkeit oder Erbrechen entwickeln, kann ein Absetzen der Behandlung mit Apremilast erforderlich sein.
- Apremilast ist mit einem erhöhten Risiko für psychiatrische Erkrankungen, wie Schlaflosigkeit und Depression, assoziiert. Fälle von Suizidgedanken und suizidalem Verhalten, einschließlich Suizid, wurden bei Patienten mit oder ohne Depression in der Anamnese beobachtet. Risiken und Nutzen der Aufnahme oder des Fortsetzens der Behandlung sollten sorgfältig abgewogen werden, wenn Patienten über frühere oder bestehende psychiatrische Symptome berichten oder eine Begleitbehandlung mit anderen Arzneimitteln, die wahrscheinlich psychiatrische Ereignisse verursachen, beabsichtigt wird. Patienten und Pflegekräfte sollten angewiesen werden, den verschreibenden Arzt über jegliche Verhaltens- oder Stimmungsänderungen oder Suizidgedanken zu informieren. Wenn bei Patienten neue psychiatrische Symptome oder eine Verschlechterung bestehender Symptome auftreten oder Suizidgedanken oder ein Suizidversuch festgestellt werden, wird empfohlen, die Behandlung mit dem Wirkstoff abzubrechen.
- Bei zu Beginn der Behandlung untergewichtigen Patienten sollte das Körpergewicht regelmäßig kontrolliert werden. Bei ungeklärtem und klinisch relevantem Gewichtsverlust sollte bei diesen Patienten eine ärztliche Abklärung erfolgen und das Absetzen der Behandlung erwogen werden.
Wirkstoff-Informationen
- EMA-Produktinformation zu Otezla (Apremilast)
- Li et al. (2018): Phosphodiesterase-4 Inhibitors for the Treatment of Inflammatory Diseases. Frontiers in Pharmacology, DOI: https://doi.org/10.3389/fphar.2018.01048
- Mulhall et al. (2015): Phosphodiesterase 4 inhibitors for the treatment of chronic obstructive pulmonary disease: A review of current and developing drugs. Expert Opinion on Investigational Drugs, DOI: 10.1517/13543784.2015.1094054
- Sehrawat et al. (2008): Role of Epac1, an Exchange Factor for Rap GTPases, in Endothelial Microtubule Dynamics and Barrier Function. Molecular Biology of the Cell, DOI: https://doi.org/10.1091/mbc.e06-10-0972
Abbildung:
Anika Mifka adapted from Li et al. (2018): Phosphodiesterase-4 Inhibitors for the Treatment of Inflammatory Diseases. Frontiers in Pharmacology, DOI: https://doi.org/10.3389/fphar.2018.01048; Mulhall et al. (2015): Phosphodiesterase 4 inhibitors for the treatment of chronic obstructive pulmonary disease: A review of current and developing drugs. Expert Opinion on Investigational Drugs, DOI: 10.1517/13543784.2015.1094054
-
Apremilast 089PHARM 10 mg + 20 mg + 30 mg Filmtabletten, Starterpack
089PHARM GmbH
-
Apremilast 089PHARM 30 mg Filmtabletten
089PHARM GmbH
-
Apremilast 123 Acurae Pharma® 30 mg Filmtabletten
123 Acurae Pharma GmbH
-
Apremilast Accord 10 mg + 20 mg + 30 mg Starterpackung
Accord Healthcare GmbH
-
Apremilast Accord 30 mg Filmtabletten
Accord Healthcare GmbH
-
Apremilast AL 10 mg + 20 mg + 30 mg Filmtabletten
ALIUD PHARMA® GmbH
-
Apremilast AL 30 mg Filmtabletten
ALIUD PHARMA® GmbH
-
Apremilast Amarox 10 mg + 20 mg + 30 mg Filmtabletten, Starterpackung
Amarox Pharma GmbH
-
Apremilast Amarox 30 mg Filmtabletten
Amarox Pharma GmbH
-
Apremilast biomo 10 mg + 20 mg + 30 mg Filmtabletten, Starterpackung
biomo pharma GmbH
-
Apremilast biomo 30 mg Filmtabletten
biomo pharma GmbH
-
Apremilast Dermapharm 10 mg + 20 mg + 30 mg Starterpackung Filmtabletten
Dermapharm AG
-
Apremilast Dermapharm 30 mg Filmtabletten
Dermapharm AG
-
Apremilast Devatis 10 mg + 20 mg + 30 mg Filmtabletten, Starterpackung
Devatis GmbH
-
Apremilast Devatis 30 mg Filmtabletten
Devatis GmbH
-
Apremilast GALEN 10 mg + 20 mg + 30 mg Starterpackung Filmtabletten
GALENpharma GmbH
-
Apremilast GALEN 30 mg Filmtabletten
GALENpharma GmbH
-
Apremilast Glenmark 30 mg Filmtabletten
Glenmark Arzneimittel GmbH
-
Apremilast Glenmark Starterpackung 10 mg + 20 mg + 30 mg Filmtabletten
Glenmark Arzneimittel GmbH
-
Apremilast Heumann 30 mg Filmtabletten
Heumann Pharma GmbH & Co. Generica KG
-
Apremilast HEXAL 10 mg + 20 mg + 30 mg Filmtabletten
Hexal AG
-
Apremilast HEXAL 30 mg Filmtabletten
Hexal AG
-
Apremilast-ratiopharm® 10 mg + 20 mg + 30 mg Filmtabletten, Starterpackung
ratiopharm GmbH
-
Apremilast-ratiopharm® 30 mg Filmtabletten
ratiopharm GmbH
-
Apremilast STADA® 10 mg + 20 mg + 30 mg Filmtabletten
STADAPHARM GmbH
-
Apremilast STADA® 30 mg Filmtabletten
STADAPHARM GmbH
-
Apremilast TAD® 30 mg Filmtabletten
TAD Pharma GmbH
-
Apremilast Zentiva 30 mg Filmtabletten
Zentiva Pharma GmbH
-
Apremilast Zentiva Starterpackung 10 mg + 20 mg + 30 mg Filmtabletten
Zentiva Pharma GmbH
-
Otezla® 10 mg/20 mg/30 mg Filmtabletten, Starterpackung
Amgen GmbH
-
Otezla 10 mg/20 mg/30 mg kohlpharma Filmtabletten
kohlpharma GmbH
-
Otezla® 10 mg/20 mg Filmtabletten, Starterpackung
Amgen GmbH
-
Otezla 10mg/20mg/30mg Eurim Filmtabletten Starterpackung
Eurim-Pharm Arzneimittel GmbH
-
Otezla 10mg/20mg/30mg Paranova Filmtabletten Starterpackung
Paranova Pack A/S
-
Otezla® 20 mg Filmtabletten
Amgen GmbH
-
Otezla 30 mg Axicorp Filmtabletten
axicorp Pharma B.V.
-
Otezla 30 mg CC Pharma Filmtabletten
CC Pharma GmbH
-
Otezla 30 mg Eurim Filmtabletten
Eurim-Pharm Arzneimittel GmbH
-
Otezla 30 mg Fd Pharma Filmtabletten
FD Pharma GmbH
-
Otezla® 30 mg Filmtabletten
Amgen GmbH
-
Otezla 30 mg Haemato-Pharm Filmtabletten
HAEMATO PHARM GmbH
-
Otezla 30 mg kohlpharma Filmtabletten
kohlpharma GmbH
-
Otezla 30 mg Medicopharm Filmtabletten
Medicopharm AG
-
Otezla 30 mg NMG Pharma Filmtabletten
NMG Pharma GmbH
-
Otezla 30 mg Orifarm Filmtabletten
Orifarm GmbH
-
Otezla 30mg Abacus Filmtabletten
Abacus Medicine A/S
-
Otezla 30mg Paranova Filmtabletten
Paranova Pack A/S














