Degarelix
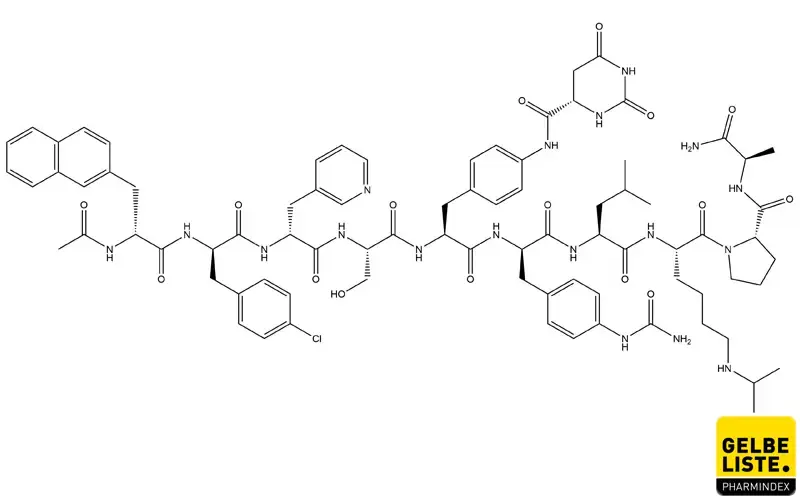
Degarelix wird als Zytostatikum zur Behandlung von fortgeschrittenem, hormonabhängigem Prostatakarzinom sowie in Kombination mit Strahlentherapie zur Behandlung des lokal begrenzten und fortgeschrittenen Prostatakarzinoms bei erwachsenen Männern verwendet.
Degarelix: Übersicht
Anwendung
Degarelix ist ein Gonadotropin-Releasing-Hormon-(GnRH)-Antagonist, der Anwendung in der Therapie von folgenden Indikationen findet:
- Zur Behandlung von erwachsenen männlichen Patienten mit fortgeschrittenem hormonabhängigem Prostatakarzinom.
- Zur Behandlung des lokal begrenzten Hochrisiko- und des lokal fortgeschrittenen, hormonabhängigen Prostatakarzinoms in Kombination mit Strahlentherapie.
- Als neoadjuvante Therapie vor einer Strahlentherapie bei Patienten mit lokal begrenztem Hochrisiko- oder lokal fortgeschrittenem, hormonabhängigem Prostatakarzinom.
Anwendungsart
Der Wirkstoff Degarelix darf ausschließlich subkutan verabreicht werden. Von einer intramuskulären Injektion wird abgeraten.
Die subkutane Injektion sollte in den Abdominalbereich gegeben werden, wobei die Injektionsstelle in regelmäßigen Abständen gewechselt werden sollte. Die Injektionsstelle sollte keinem erhöhten Druck ausgesetzt sein, also z. B. nicht in Rippennähe oder in der Nähe des Hosenbundes oder des Gürtels.
Wirkmechanismus
Degarelix ist ein Gonadotropin-Releasing-Hormon (GnRH)-Antagonist, der durch reversible und kompetitive Bindung an die GnRH-Rezeptoren in der Hypophyse die Freisetzung der Gonadotropine LH und FSH sowie indirekt die Testosteronproduktion in den Hoden verringert. Diese Wirkung verhindert im Gegensatz zu GnRH-Agonisten einen initialen Anstieg der LH- und Testosteronspiegel, was das Risiko für typische Symptomverschlimmerungen zu Beginn der Therapie minimiert. Das androgensensitive Prostatakarzinom spricht auf die Verringerung der Androgene an.
Die anfängliche Dosis von 240 mg Degarelix, gefolgt von monatlichen Erhaltungsdosen von 80 mg, führt rasch zu reduzierten LH, FSH und Testosteronwerten. Über ein Jahr hinweg ermöglicht die Behandlung eine nachhaltige Unterdrückung des Testosteronspiegels auf ein Niveau, das als medikamentöse Kastration betrachtet wird, ohne dass es zu Testosteron-Microsurges kommt.
Pharmakokinetik
Resorption
- Nach der subkutanen Injektion von 240 mg Degarelix bei Patienten mit Prostatakarzinom erreicht die Substanz ihre maximale Plasmakonzentration (Cmax) nach etwa 40 Stunden.
- Die Anfangsspitzenkonzentration liegt bei ca. 66,0 ng/ml.
- Die mittleren Talspiegel nach der Erhaltungsdosis von 80 mg bewegen sich zwischen 11 – 16 ng/ml.
- Die Bioverfügbarkeit und Halbwertszeit variieren je nach Konzentration der Injektionslösung, wobei die Plasmakonzentration nach Erreichen des Spitzenwerts langsam und biphasisch abnimmt.
Verteilung
- Das Verteilungsvolumen bei älteren, gesunden Männern liegt bei etwa 1 l/kg.
- Degarelix zeigt eine hohe Plasmaproteinbindung von ca. 90%.
Metabolismus (Biotransformation)
- Degarelix wird durch normalen Peptidabbau hauptsächlich über das hepatobiliäre System metabolisiert, wobei keine signifikanten Metaboliten im Plasma entstehen.
- Das Arzneimittel ist kein Substrat für das humane CYP450-System.
Elimination
- Etwa 20 – 30% einer verabreichten Dosis werden renal ausgeschieden, während 70 – 80%, über das hepatobiliäre System eliminiert wird.
- Die Clearance von Degarelix beträgt bei gesunden älteren Männern 35 – 50 ml/h/kg Körpergewicht.
Dosierung
Dosierung von Degarelix:
- Anfangsdosis: 240 mg, aufgeteilt in zwei subkutane Injektionen von je 120 mg.
- Erhaltungsdosis: 80 mg als eine subkutane Injektion monatlich. Die erste Erhaltungsdosis sollte einen Monat nach der Anfangsdosis gegeben werden.
- Anwendung bei speziellen Patientengruppen: Bei älteren Patienten oder solchen mit leichter bis mittelschwerer Leber- oder Nierenfunktionsstörung ist keine Dosisanpassung notwendig. Vorsicht ist bei Patienten mit schwerer Leber- oder Nierenfunktionsstörung geboten, da hierzu keine Daten vorliegen.
- Anwendung bei Kindern und Jugendlichen: Degarelix ist nicht für die Behandlung von Kindern und Jugendlichen vorgesehen.
Überwachung der therapeutischen Wirksamkeit:
- Durch klinische Parameter und Bestimmung des Prostata-spezifischen Antigens (PSA).
- Eine schnelle Testosteron-Suppression wird unmittelbar nach der Anfangsdosis erwartet, wobei die meisten Patienten innerhalb von drei Tagen und alle Patienten innerhalb eines Monats die medikamentöse Kastration entsprechende Testosteronspiegel erreichen.
Nebenwirkungen
Zu den weiteren Nebenwirkungen, die während einer Therapie mit Degarelix auftreten können, zählen:
- Hitzewallungen
- Nebenwirkungen an der Injektionsstelle
- Anämie
- Gewichtszunahme
- Schlaflosigkeit
- Schwindelgefühl und Kopfschmerzen
- Diarrhoe und Übelkeit
- Erhöhte Lebertransaminasen
- Hyperhidrose und Hautausschlag
- Skelettmuskelschmerzen und -beschwerden
- Gynäkomastie, testikuläre Atrophie sowie erektile Dysfunktion
- Schüttelfrost, Pyrexie sowie grippeähnliche Symptome
Gelegentliche Nebenwirkungen, die potenziell unter Degarelix auftreten können, umfassen:
- Überempfindlichkeit
- Hyperglykämie, erhöhte Cholesterinwerte sowie Veränderungen des Blutkalziums
- Psychische Störungen, Depression und verminderte Libido
- Hypästhesie
- Verschwommenes Sehen
- Herzrhythmusstörungen (inkl. Vorhofflimmern), Herzklopfen, QT-Verlängerung
- Hypertonie und vasovagale Reaktionen
- Dyspnoe
- Konstipation, Erbrechen, abdominale Beschwerden sowie trockener Mund
- Erhöhte Bilirubinwerte und alkalische Phosphatase erhöht
- Urtikaria, Alopezie und Pruritus
- Osteopenie, Arthralgie und Gelenksteifheit
- Pollakisurie, Dysurie, Nykturie und Nierenfunktionsstörungen
- Periphere Ödeme
- Reizung der Genitalien, ausbleibende Ejakulation und Hodenschmerzen
Wechselwirkungen
Folgende Wechselwirkungen sind bei der Anwendung von Degarelix zu beachten:
- Wechselwirkungen mit QTc-Intervall verlängernden Arzneimitteln: Die gleichzeitige Verwendung von Degarelix mit Medikamenten, die das QTc-Intervall verlängern oder Torsades de pointes auslösen können, sollte mit Vorsicht erfolgen. Dazu gehören Antiarrhythmika der Klassen IA (wie Quinidin und Disopyramid) und III (wie Amiodaron, Sotalol), sowie andere Medikamente wie Methadon und Moxifloxacin.
- Einfluss auf CYP450-Enzyme: Degarelix ist kein Substrat für das CYP450-Enzymsystem und hat keine signifikante induzierende oder hemmende Wirkung auf wichtige CYP-Enzyme wie CYP1A2, CYP2C8, CYP2C9, CYP2C19, CYP2D6, CYP2E1, und CYP3A4/5. Daher ist es unwahrscheinlich, dass Degarelix klinisch bedeutende pharmakokinetische Wechselwirkungen mit Medikamenten zeigt, die durch diese Enzyme metabolisiert werden.
Kontraindikationen
Die Anwendung von Degarelix ist kontraindiziert bei:
- Überempfindlichkeit oder Allergie gegen den Wirkstoff
Verkehrstüchtigkeit
Degarelix beeinträchtigt die Verkehrstüchtigkeit oder die Fähigkeit zum Bedienen von Maschinen nicht oder nur in vernachlässigbarem Maße.
Anwendungshinweise
Folgende Warnhinweise und Vorsichtsmaßnahmen sind bei der Anwendung von Degarelix zu beachten:
- QT/QTc-Intervall Verlängerung: Bei langzeitiger Androgendeprivationstherapie wurde eine Verlängerung des QT-Intervalls beobachtet. Patienten mit einem vorherigen längeren QT-Intervall oder Risikofaktoren für Torsades de pointes sollten besonders sorgfältig überwacht werden, da keine spezifischen Daten für diese Gruppen vorliegen.
- Eingeschränkte Leberfunktion: Patienten mit bekannter oder vermuteter Lebererkrankung sollten während der Behandlung mit Degarelix auf Leberfunktionsstörungen hin überwacht werden, obwohl leichte Anstiege von ALT und AST beobachtet wurden, die nicht mit weiteren klinischen Symptomen verbunden waren.
- Eingeschränkte Nierenfunktion: Bei Patienten mit schwerer Nierenfunktionsstörung ist Vorsicht geboten, da keine spezifischen Daten über die Verwendung von Degarelix in dieser Gruppe vorliegen.
- Überempfindlichkeitsreaktionen: Patienten mit schweren allergischen Vorgeschichten wie unbehandeltem Asthma, anaphylaktischen Reaktionen oder schwerer Urtikaria sollten unter besonderer Überwachung stehen.
- Knochendichteveränderungen: Langzeittestosteronsuppression kann zu einer verminderten Knochendichte führen, ähnlich wie nach einer Orchiektomie oder einer Behandlung mit GnRH-Agonisten.
- Glucosetoleranz: Eine Androgendeprivation kann die Glucosetoleranz beeinträchtigen, was bei Diabetikern zu einer Entwicklung oder Verschlechterung des Diabetes führen kann. Häufigere Blutzuckerkontrollen können erforderlich sein.
- Kardiovaskuläre Risiken: Die Behandlung kann das Risiko für kardiovaskuläre Ereignisse erhöhen. Patienten sollten auf mögliche Symptome eines Herzinfarkts oder Schlaganfalls hin überwacht und alle kardiovaskulären Risikofaktoren sollten berücksichtigt werden.
Alternativen
Je nach Indikationsgebiet und patientenindividuellen Gegebenheiten kommen weitere Wirkstoffe in der hormonalen Therapie von Prostatakarzinomen als Alternative in Frage:
Androgenantagonisten
CYP17A-/ Androgensynthese-Hemmer
Wirkstoff-Informationen
Molare Masse: 1632.26 g·mol-1
Mittlere Halbwertszeit: ca. 28.0 D
Q0-Wert: 0.75
Kindstoff(e): Degarelix acetat
Wirkstoff-Informationen
- Freissmuth et al., Pharmakologie und Toxikologie, 2020, Springer
- Fachinformationen des Degarelix-Herstellers Ferring Arzneimittel (Fachinformation Firmagon 120 mg / Firmagon 80 mg)
- Europäische Arzneimittelagentur (EPAR): Firmagon (Degarelix), 2021
-
Firmagon 80 mg Abacus Pulver und Lösungsmittel zur Herstellung einer Injektionslösung
Abacus Medicine A/S
-
Firmagon 80 mg axicorp B.V. Pulver und Lösungsmittel zur Herstellung einer Injektionslösung
axicorp Pharma B.V.
-
Firmagon 80 mg axicorp Pulver und Lösungsmittel zur Herstellung einer Injektionslösung
axicorp Pharma GmbH
-
Firmagon 80 mg CC Pharma Pulver und Lösungsmittel zur Herstellung einer Injektionslösung
CC Pharma GmbH
-
Firmagon 80 mg Eurim Pulver und Lösungsmittel zur Herstellung einer Injektionslösung
Eurim-Pharm Arzneimittel GmbH
-
Firmagon 80 mg kohlpharma Pulver und Lösungsmittel zur Herstellung einer Injektionslösung
kohlpharma GmbH
-
Firmagon 80 mg Orifarm Pulver und Lösungsmittel zur Herstellung einer Injektionslösung
Orifarm GmbH
-
Firmagon 80 mg Paranova Pulver und Lösungsmittel zur Herstellung einer Injektionlösung
Paranova Pack A/S
-
FIRMAGON® 80 mg Pulver und Lösungsmittel zur Herstellung einer Injektionslösung
Ferring Arzneimittel GmbH
-
Firmagon 120 mg Abacus Pulver und Lösungsmittel zur Herstellung einer Injektionslösung
Abacus Medicine A/S
-
Firmagon 120 mg axicorp B.V. Pulver und Lösungsmittel zur Herstellung einer Injektionslösung
axicorp Pharma B.V.
-
Firmagon 120 mg CC Pharma Pulver und Lösungsmittel zur Herstellung einer Injektionslösung
CC Pharma GmbH
-
Firmagon 120 mg Eurim Pulver und Lösungsmittel zur Herstellung einer Injektionslösung
Eurim-Pharm Arzneimittel GmbH
-
Firmagon 120 mg kohlpharma Pulver und Lösungsmittel zur Herstellung einer Injektionslösung
kohlpharma GmbH
-
Firmagon 120 mg Orifarm Pulver und Lösungsmittel zur Herstellung einer Injektionslösung
Orifarm GmbH
-
Firmagon 120 mg Paranova Pulver und Lösungsmittel zur Herstellung einer Injektionslösung
Paranova Pack A/S
-
FIRMAGON® 120 mg Pulver und Lösungsmittel zur Herstellung einer Injektionslösung
Ferring Arzneimittel GmbH











