Fampridin
Fampridin ist ein Kaliumkanalblocker, der die Gehfähigkeit bei Patienten mit Multipler Sklerose verbessert. Der Wirkstoff ist bislang die einzige zugelassene medikamentöse Therapieoption in dieser Indikation.
Fampridin: Übersicht
Anwendung
Fampridin wird angewendet zur Verbesserung der Gehfähigkeit von erwachsenen Patienten mit Multipler Sklerose (MS) mit Gehbehinderung. Gangstörungen und andere Mobilitätseinschränkungen können Alltagsaktivitäten sowie die berufliche Leistungsfähigkeit von Betroffenen stark einschränken und werden von ihnen als hohe Belastung eingestuft.
Anwendungsart
Fampridin steht in Form von Retardtabletten zur Verfügung. Diese müssen im Ganzen geschluckt werden und dürfen nicht geteilt, zerdrückt, aufgelöst, gelutscht oder zerkaut werden.
Das Arzneimittel sollte auf nüchternen Magen eingenommen werden.
Wirkmechanismus
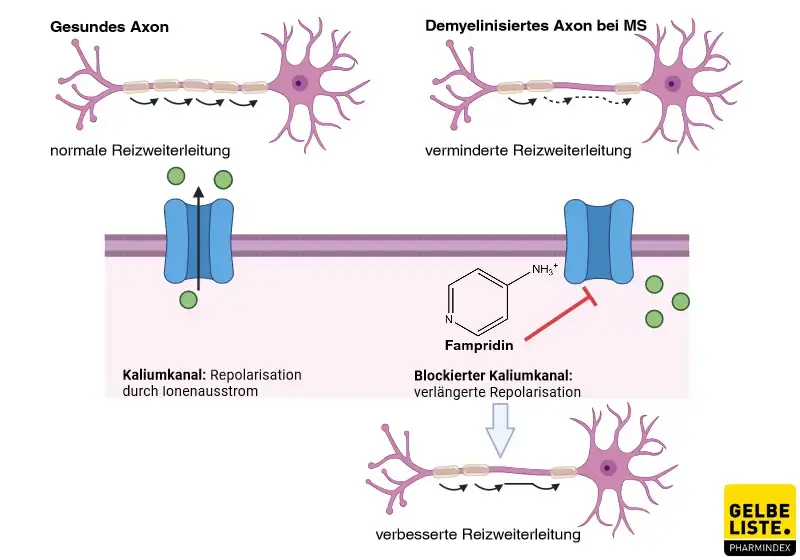
Fampridin ist ein Kaliumkanalblocker. Durch die Blockierung der Kaliumkanäle verringert der Wirkstoff das Austreten von Ionenstrom, verlängert so die Repolarisation und verstärkt die Aktionspotentialbildung in demyelinisierten Axonen sowie die neurologische Funktion bei MS-Patienten. Es wird vermutet, dass durch die Verstärkung der Aktionspotentialbildung mehr Impulse im zentralen Nervensystem weitergeleitet werden.
Pharmakokinetik
Resorption
Fampridin wird schnell und vollständig aus dem Gastrointestinaltrakt resorbiert. Die relative Bioverfügbarkeit liegt bei 95%. Die Retardierung bewirkt zwar eine verzögerte Resorption, beeinflusst die Resorptionsrate jedoch nicht.
Die Einnahme gemeinsam mit Nahrungsmitteln kann die maximale Plasmakonzentration von Fampridin erhöhen und damit auch dosisbedingt die Nebenwirkungen steigern.
Verteilung
Fampridin passiert als lipidlöslicher Wirkstoff leicht die Bluthirnschranke und ist größtenteils nicht an Plasmaproteine gebunden. Das mittlere Verteilungsvolumen beträgt etwa 2,6 L/kg.
Metabolismus
Fampridin (4-Aminopyridin) wird durch Oxidation zu 3-Hydroxy-4-Aminopyridin metabolisiert und weiter zu 3-Hydroxy-4-Aminopyridin-Sulfat konjugiert. Die Metaboliten weisen keine pharmakologische Wirkung auf Kaliumkanäle auf.
Die 3-Hydroxylierung scheint durch das Cyotchrom-P450-Enzym CYP2E1 katalysiert zu werden und es gibt Hinweise auf eine direkte Hemmung dieses Enzyms durch eine Fampridin-Konzentration, die etwa dem 100-fachen der pharmazeutisch eingesetzten Konzentration entspricht.
Elimination
Fampridin wird vor allem über die Nieren und nur zu weniger als 1% über die Fäzes eliminiert. Etwa 90% der Dosis werden dabei innerhalb von 24 Stunden unverändert über den Urin ausgeschieden. Die Halbwertszeit beträgt etwa 6 Stunden.
Aufgrund der kombinierten glomerulären Filtration und etwa zu 60% aktiven Ausscheidung durch den renalen OCT2-Transporter ist die renale Clearance (3370 ml/min) erheblich größer als die glomeruläre Filtrationsrate.
Bei Patienten mit Nierenfunktionsstörung akkumuliert Fampridin relativ zum Grad der Störung.
Dosierung
Die empfohlene Dosis von Fampridin beträgt zweimal täglich eine 10 mg Tablette im Abstand von 12 Stunden, z.. B. morgens und abends.
Nebenwirkungen
Die folgenden Nebenwirkungen könnten bei der Behandlung mit Fampridin häufig (≥1/100, <1/10) bis sehr häufig (≥1/10) auftreten.
- Harnwegsinfektion
- Influenza, Nasopharyngitis, Virusinfektion
- Schlaflosigkeit, Angst
- Schwindel, Kopfschmerzen, Gleichgewichtsstörung, Vertigo, Parästhesie, Tremor
- Palpitationen
- Dyspnoe, Pharyngolaryngealschmerzen
- Übelkeit, Erbrechen, Obstipation, Dyspepsie
- Rückenschmerzen
- Asthenie
Wechselwirkungen
Fampridin wird zu einem hohen Anteil aktiv über den renalen OCT2-Transporter eliminiert. Die gleichzeitige Anwendung von Inhibitoren dieses Transporters ist daher kontraindiziert. Auch bei der parallelen Therapie mit OCT2-Substraten, wie den folgenden, ist Vorsicht geboten.
Kontraindikationen
Fampridin darf in den folgenden Fällen nicht angewendet werden.
- Überempfindlichkeit gegen den Wirkstoff
- Gleichzeitige Behandlung mit anderen Fampridin-haltigen Arzneimitteln
- Krampfanfälle in der Vorgeschichte oder gegenwärtig
- Mittelschwere oder schwere Nierenfunktionsstörung (Kreatinin-Clearance <50 ml/min)
- Gleichzeitige Anwendung mit OTC2-Inhibitoren (organischer Kationentransporter 2), wie Cimetidin
Schwangerschaft
Tierexperimentelle Studien zeigten eine Reproduktionstoxizität von Fampridin und es liegen bisher sehr begrenzte Erfahrungen zur Anwendung in der Schwangerschaft vor. Daher sollte die Behandlung mit Fampridin während der Schwangerschaft vermieden werden.
Stillzeit
Da nicht bekannt ist, ob Fampridin in die Muttermilch übergeht, wird die Anwendung in der Stillzeit nicht empfohlen.
Verkehrstüchtigkeit
Da Fampridin Schwindel hervorrufen kann, hat der Wirkstoff einen mäßigen Einfluss auf die Verkehrstüchtigkeit und die Fähigkeit zum Bedienen von Maschinen.
Anwendungshinweise
Beginn und Beurteilung der Behandlung
Ein Behandlungserfolg mit Fampridin ist in der Regel innerhalb von zwei bis vier Wochen nach Behandlungsbeginn erkennbar. Daher sollte die Erstverordnung auf diesen Zeitraum begrenzt sein.
Zur Beurteilung der Verbesserung nach zwei bis vier Wochen wird die Bewertung der Gehfähigkeit, z. B. mittels Timed 25 Foot Walk-Test (T25FW) oder anhand der Bewertungsskala MSWS-12 (Twelve Item Multiple Sclerosis Walking Scale) empfohlen.
Wenn keine Verbesserung beobachtet wird, sollte die Behandlung abgesetzt werden. Verschlechtert sich die Gehfähigkeit wieder, sollte eine Neubewertung der Wirkung inklusive eines Absetzens der Therapie erfolgen.
Bestimmung der Nierenfunktion
Fampridin wird hauptsächlich unverändert über die Nieren ausgeschieden, daher kann die Plasmakonzentration bei Patienten mit Nierenfunktionsstörung erhöht sein, was zu vermehrten unerwünschten Reaktionen, v. a. neurologischen Wirkungen, führt. Aus diesem Grund wird die Bestimmung der Nierenfunktion vor der Behandlung und ihre regelmäßige Kontrolle während der Behandlung für alle Patienten, insbesondere Ältere, empfohlen.
Vorsicht ist geboten bei der Verordnung für Patienten mit leichter Nierenfunktionsstörung sowie der gleichzeitigen Anwendung von OCT2-Substraten.
Schwerwiegende Überempfindlichkeitsreaktionen
Es sind Fälle schwerwiegender Überempfindlichkeitsreaktionen bekannt, die vorwiegend in der ersten Behandlungswoche auftraten. Daher ist bei Patienten mit allergischen Reaktionen in der Anamnese besondere Vorsicht geboten. Tritt eine anaphylaktische oder sonstige schwere allergische Reaktion auf, sollte Fampridin abgesetzt und die Behandlung nicht wieder aufgenommen werden.
Kardiovaskuläre Rhythmus- und Erregungsleitungsstörungen
Fampridin ist bei Patienten mit kardiovaskulären Rhythmusstörungen und sinuatrialen oder atrioventrikulären Erregungsleitungsstörungen mit Vorsicht anzuwenden, da diese Wirkungen bei einer Überdosierung zu beobachten sind.
Sturzgefahr
Das vermehrte Auftreten von Schwindel und Gleichgewichtsstörungen unter Fampridin kann zu einem erhöhten Sturzrisiko führen. Patienten sollten daher bei Bedarf Gehhilfen benutzen.
Alternativen
Fampridin ist die bisher einzige zugelassene medikamentöse Therapie zur Verbesserung der Gehfähigkeit von erwachsenen MS-Patienten mit Gehbehinderung. Es stehen jedoch verschiedene nichtmedikamentöse Maßnahmen zur Verfügung, die in der S2e-Leitlinie "Bewegungstherapie zur Verbesserung der Mobilität von Patienten mit Multipler Sklerose" der Deutschen Gesellschaft für Neurologische Rehabilitation zusammengefasst werden.
Häufige Ursache einer Gangstörung ist die Fußheberschwäche mit Auswirkungen auf Gangsicherheit und -geschwindigkeit. Für diese Patienten stehen beispielsweise starre oder dynamische Fußheberorthesen oder Stimulationssysteme mit funktioneller Elektrostimulation (FES) zur Verfügung.
Weitere Informationen sind der jeweiligen Fachinformation zu entnehmen.
Wirkstoff-Informationen
- Hexal AG: Fachinformation Fampridin Hexal, Stand: März 2023
- Hemmer B. et al. (2023): Diagnose und Therapie der Multiplen Sklerose, Neuromyelitis-optica-Spektrum-Erkrankungen und MOG-IgG-assoziierten Erkrankungen, S2k-Leitlinie. Deutsche Gesellschaft für Neurologie (Hrsg.), Leitlinien für Diagnostik und Therapie in der Neurologie, abgerufen am 22.11.2023
- Tholen et al. (2019): Bewegungstherapie zur Verbesserung der Mobilität von Patienten mit Multipler Sklerose, S2e-Leitlinie. Neurol Rehabil 2019; 25(1): 03–40, DOI 10.14624/NR1902001
Abbildung
Janina Seiffert; Created with BioRender.com (2023)
-
Fampridin AL 10 mg Retardtabletten
ALIUD PHARMA® GmbH
-
Fampridin Ascend 10 mg Retardtabletten
Ascend GmbH
-
FAMPRIDIN BASICS 10 mg Retardtabletten
Basics GmbH
-
Fampridin beta 10 mg Retardtabletten
betapharm Arzneimittel GmbH
-
Fampridin Heumann 10 mg Retardtabletten
Heumann Pharma GmbH & Co. Generica KG
-
Fampridin HEXAL® 10 mg Retardtabletten
Hexal AG
-
Fampridin Micro Labs 10 mg Retardtabletten
Micro Labs GmbH
-
Fampridin neuraxpharm 10 mg Retardtabletten
neuraxpharm Arzneimittel GmbH
-
Fampridin PUREN 10 mg Retardtabletten
PUREN Pharma GmbH & Co. KG
-
Fampridin-ratiopharm 10 mg Retardtabletten
ratiopharm GmbH
-
Fampridin STADA® 10 mg Retardtabletten
STADAPHARM GmbH
-
Fampridin Zentiva 10 mg Retardtabletten
Zentiva Pharma GmbH
-
Fampyra 10 mg kohlpharma Retardtabletten
kohlpharma GmbH
-
Fampyra® 10 mg Retardtabletten
Merz Therapeutics GmbH













