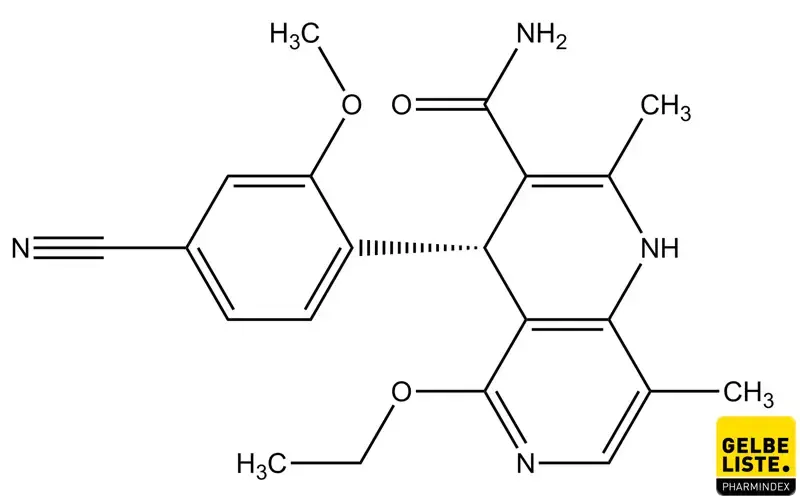
Finerenon
Finerenon ist ein selektiver Mineralokortikoid-Rezeptor-Antagonist mit antiinflammatorischen und antifibrotischen Eigenschaften. Es wird hauptsächlich bei Patienten mit chronischer Nierenerkrankung und Typ-2-Diabetes zur Reduktion kardiovaskulärer Risiken eingesetzt.
Finerenon : Übersicht
Anwendung
Finerenon (Kerendia) wird angewendet zur Behandlung von chronischer Nierenerkrankung (mit Albuminurie) in Verbindung mit Diabetes mellitus Typ 2 bei Erwachsenen.
Anwendungsart
Finerenon ist in Form von Filmtabletten der Stärken 10- und 20 mg für die orale Anwendung auf dem Markt.
Wirkmechanismus
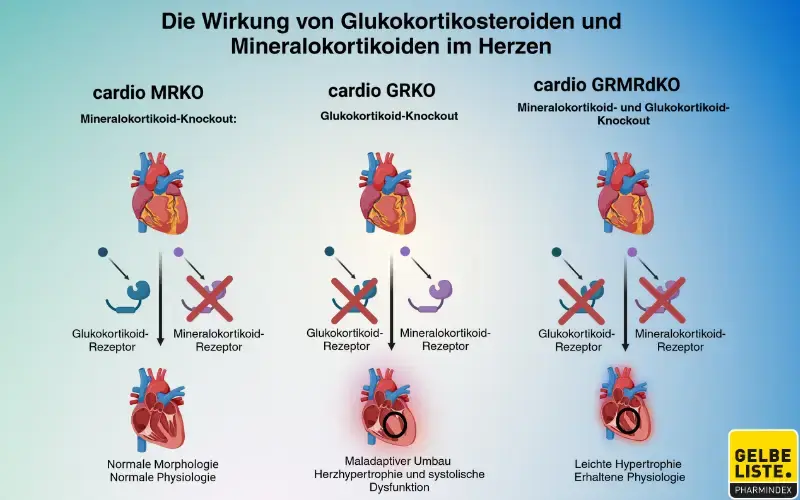
Finerenon ist ein nicht-steroidaler, selektiver Mineralokortikoid-Rezeptor-Antagonist (MRA). Der Wirkmechanismus von Finerenon basiert auf der selektiven Blockade des Mineralokortikoid-Rezeptors (MR), der eine Schlüsselrolle bei der Regulation des Wasser- und Elektrolythaushalts spielt. Durch die Hemmung des MR wird die Bindung von Aldosteron verhindert, was zu einer Reduktion von Entzündungen und Fibrose im Herz-Kreislauf-System und den Nieren führt.
Diese antiinflammatorischen und antifibrotischen Effekte tragen dazu bei, das Risiko von kardiovaskulären Ereignissen und die Progression der Nierenerkrankung bei Patienten mit Typ-2-Diabetes und chronischer Nierenerkrankung zu reduzieren. Im Gegensatz zu anderen MRAs zeigt Finerenon eine höhere Selektivität für den MR, was das Risiko von Hyperkaliämie und anderen Nebenwirkungen verringern kann.
Pharmakokinetik
Resorption
- Fast vollständige Aufnahme nach oraler Einnahme
- Maximale Plasmakonzentrationen nach 0,5 bis 1,25 Stunden
- Absolute Bioverfügbarkeit von 43,5 % aufgrund des First-Pass-Metabolismus
- In vitro Substrat des Effluxtransporters P-Glykoprotein, aber in vivo nicht relevant für die Resorption
- Auswirkung von Nahrung: AUC um 21% erhöht, Cₘₐₓ um 19% reduziert und Zeit bis Cₘₐₓ auf 2,5 Stunden verlängert bei Einnahme mit fetter, kalorienreicher Nahrung
Verteilung
- Verteilungsvolumen im Steady State beträgt 52,6 l
- Plasmaproteinbindung von 91,7 %, primäres Bindungsprotein ist Serumalbumin
Metabolisierung
- Metabolismus zu etwa 90% durch CYP3A4 und zu 10% durch CYP2C8
- Vier Hauptmetaboliten im Plasma, alle pharmakologisch inaktiv
Elimination
- Eliminationshalbwertszeit von etwa 2 bis 3 Stunden
- Systemische Clearance von etwa 25 l/h
- 80% über Urin und 20 % über Fäzes ausgeschieden, hauptsächlich in Form von Metaboliten
Linearität
- Pharmakokinetik ist linear im untersuchten Dosisbereich von 1,25 mg bis 80 mg
Besondere Patientengruppen
- Keine Unterschiede in Sicherheit und Wirksamkeit zwischen älteren und jüngeren Patienten
- Höhere Plasmakonzentrationen bei älteren im Vergleich zu jüngeren gesunden Teilnehmern
- Leichte Nierenfunktionsstörung hat keine Auswirkung auf AUC und Cₘₐₓ
- Mittelschwere bis schwere Nierenfunktionsstörung erhöht AUC um 34-36%
- Leichte Leberfunktionsstörung verändert Finerenon-Exposition nicht
- Mittelschwere Leberfunktionsstörung erhöht AUC um 38% bzw. 55%
- Körpergewicht als Kovariate für Cₘₐₓ identifiziert, aber keine Dosisanpassung notwendig
Dosierung
Anfangsdosis nach eGFR:
- Tagesdosis: 20 mg einmal täglich.
- Höchstdosis: 20 mg einmal täglich.
Einleitung der Behandlung:
- Serumkalium und eGFR prüfen.
- Bei Serumkalium ≤ 4,8 mmol/l kann Behandlung beginnen.
- Bei Serumkalium > 4,8 bis 5,0 mmol/l ist zusätzliche Überwachung nötig.
- Bei Serumkalium > 5,0 mmol/l sollte nicht begonnen werden.
- Anfangsdosis nach eGFR: ≥ 60 = 20 mg, ≥ 25 bis < 60 = 10 mg, < 25 = nicht empfohlen.
Fortsetzung der Behandlung:
- Serumkalium und eGFR nach 4 Wochen erneut messen.
- Dosisanpassung nach Serumkalium: ≤ 4,8 = erhöhen auf 20 mg, > 4,8 bis 5,5 = aktuelle Dosis beibehalten, > 5,5 = aussetzen und bei ≤ 5,0 mit 10 mg wieder aufnehmen.
Vergessene Dosis:
- Am selben Tag nachholen.
- Keine doppelte Menge nehmen.
Nebenwirkungen
Die am häufigsten gemeldete Nebenwirkung bei der Anwendung von Finerenon in klinischen Studien war Hyperkaliämie. Häufig kam es zu Hyponatriämie, Hyperurikämie, Hypotonie, Pruritus (Juckreiz) und einer verminderten glomerulären Filtrationsrate.
Wechselwirkungen
Bei der Anwendung von Finerenon sind folgende Wechselwirkungen mit anderen Arzneimitteln und sonstige Wechselwirkungen zu beachten:
- Starke CYP3A4-Inhibitoren: Die gleichzeitige Anwendung von Finerenon mit Itraconazol, Clarithromycin und anderen starken CYP3A4-Inhibitoren ist kontraindiziert, da dies die Finerenon-Exposition erhöht.
- Starke und moderate CYP3A4-Induktoren: Finerenon sollte nicht gleichzeitig mit Rifampicin und anderen starken CYP3A4-Induktoren oder mit Efavirenz und anderen moderaten CYP3A4-Induktoren angewendet werden, da dies die Plasmakonzentration von Finerenon verringert.
- Arzneimittel, die das Serumkalium erhöhen: Finerenon sollte nicht gleichzeitig mit kaliumsparenden Diuretika und anderen MRA angewendet werden, da dies das Hyperkaliämie-Risiko erhöht.
- Grapefruit: Grapefruits oder Grapefruitsaft sollten während der Behandlung mit Finerenon nicht verzehrt werden, da dies die Plasmakonzentration von Finerenon erhöht.
- Moderate CYP3A4-Inhibitoren: Bei gleichzeitiger Anwendung von Erythromycin oder Verapamil kann der Serumkalium-Spiegel ansteigen, daher wird eine Überwachung des Serumkaliums empfohlen.
- Schwache CYP3A4-Inhibitoren: Bei gleichzeitiger Anwendung von Fluvoxamin kann der Serumkalium-Spiegel ansteigen, daher wird eine Überwachung des Serumkaliums empfohlen.
- Kaliumergänzungsmittel und Trimethoprim/Sulfamethoxazol: Bei Anwendung von Finerenon zusammen mit diesen Mitteln ist eine Überwachung des Serumkaliums erforderlich. Unter Umständen muss Finerenon vorübergehend abgesetzt werden.
- Blutdrucksenkende Arzneimittel: Das Risiko für eine Hypotension steigt bei gleichzeitiger Anwendung von mehreren anderen blutdrucksenkenden Arzneimitteln, daher wird eine Überwachung des Blutdrucks empfohlen.
Kontraindikationen
Finerenon darf nicht angewendet werden bei:
- Überempfindlichkeit gegen den Wirkstoff
- Gleichzeitiger Behandlung mit starken CYP3A4-Inhibitoren
- Morbus Addison
Anwendungshinweise
Bei der Anwendung von Finerenon sind folgende besondere Warnhinweise und Vorsichtsmaßnahmen zu beachten:
- Hyperkaliämie: Beobachtet bei Patienten; engmaschige Überwachung bei Risikofaktoren wie niedriger eGFR.
- Behandlungsbeginn: Nicht starten bei Serumkalium > 5,0 mmol/l; mögliche Überwachung bei 4,8 bis 5,0 mmol/l.
- Überwachung: Serumkalium und eGFR 4 Wochen nach Beginn oder Dosiserhöhung prüfen.
- Begleitmedikation: Risikoerhöhung bei Medikamenten, die Serumkalium erhöhen; nicht kombinieren mit kaliumsparenden Diuretika.
- Nierenfunktion: Risikoerhöhung bei abnehmender Funktion; keine Behandlung bei eGFR < 25 ml/min/1,73 m2.
- Leberfunktion: Keine Behandlung bei schwerer Störung; mögliche Überwachung bei mittelschwerer Störung.
- Herzinsuffizienz: Ausgeschlossen von klinischen Phase-III-Studien bei reduzierter Ejektionsfraktion und Klasse II-IV.
- Substanzen, die Exposition beeinflussen: Serumkalium überwachen bei Anwendung mit CYP3A4-Inhibitoren; nicht kombinieren mit starken CYP3A4-Induktoren; kein Grapefruitsaft.
- Embryofetale Toxizität: Nicht anwenden während Schwangerschaft, es sei denn, Nutzen überwiegt Risiko; Verhütung erforderlich; Stillverbot.
- Sonstige Bestandteile: Nicht anwenden bei hereditärer Galactose-Intoleranz, Lactase-Mangel oder Glucose-Galactose-Malabsorption.
Wirkstoff-Informationen
- EMA: Fachinformation Kerendia
- Marcath, Lauren A. "Finerenone." Clinical Diabetes 39.3 (2021): 331-332.
- Rico-Mesa, Juan Simon, et al. "Mineralocorticoid receptor antagonists: a comprehensive review of finerenone." Current Cardiology Reports 22 (2020): 1-11.
Abbildung
Dr. Isabelle Viktoria Maucher; Adapted from “The Effect of Glucocorticosteroids and Mineralcorticosteroids in the heart”, by BioRender.com (2023)
-
Kerendia 10 mg Abacus Filmtabletten
Abacus Medicine A/S
-
Kerendia 10 mg axicorp Filmtabletten
axicorp Pharma B.V.
-
Kerendia 10 mg CC Pharma Filmtabletten
CC Pharma GmbH
-
Kerendia 10 mg Emra Filmtabletten
Emra-Med Arzneimittel GmbH
-
Kerendia 10 mg Eurim Filmtabletten
Eurim-Pharm Arzneimittel GmbH
-
Kerendia 10 mg Filmtabletten
Bayer Vital GmbH Geschäftsbereich Pharma
-
Kerendia 10 mg kohlpharma Filmtabletten
kohlpharma GmbH
-
Kerendia 10 mg Orifarm Filmtabletten
Orifarm GmbH
-
Kerendia 20 mg Abacus Filmtabletten
Abacus Medicine A/S
-
Kerendia 20 mg CC Pharma Filmtabletten
CC Pharma GmbH
-
Kerendia 20 mg Emra Filmtabletten
Emra-Med Arzneimittel GmbH
-
Kerendia 20 mg Eurim Filmtabletten
Eurim-Pharm Arzneimittel GmbH
-
Kerendia 20 mg Filmtabletten
Bayer Vital GmbH Geschäftsbereich Pharma
-
Kerendia 20 mg kohlpharma Filmtabletten
kohlpharma GmbH
-
Kerendia 20 mg Orifarm Filmtabletten
Orifarm GmbH
-
Kerendia® 40 mg Filmtabletten
Bayer Vital GmbH Geschäftsbereich Pharma














