Roflumilast
Roflumilast gehört zur Wirkstoffgruppe der Phosphodiesterase-4-Hemmer. Der Wirkstoff wird zur Behandlung der chronisch-obstruktiven Lungenerkrankung (COPD) eingesetzt.
Roflumilast: Übersicht

Anwendung
Der PDE-4-Hemmer Roflumilast wird zur fortdauernden Behandlung der schweren chronisch-obstruktiven Lungenerkrankung (COPD) bei Erwachsenen angewendet, bei denen in der Vergangenheit häufig Exazerbationen auftraten und die unter chronischer Bronchitis leiden.
Wirkmechanismus
Roflumilast ist ein Hemmstoff der Phosphodiesterase-4 (PDE-4). Der Wirkstoff entfaltet seinen antiphlogistischen Effekt, indem er die Spaltung der Phosphodiesterbindung durch das Enzym und damit den Abbau von zyklischem Adenosinmonophosphat (cAMP) zu Adenosinmonophosphat (AMP) verhindert. Die Isoform 4 der Phosphodiesterase wird in verschiedenen Entzündungszellen, wie zum Beispiel Makrophagen, neutrophilen und eosinophilen Leukozyten, exprimiert.
Über die Degradierung von cAMP durch die PDE-4 wird die Bildung pro- und anti-inflammatorischer Zytokine sowie die Zellproliferation reguliert. Die Inhibierung des Enzyms führt daher zu einem Anstieg der intrazellulären cAMP-Konzentration.
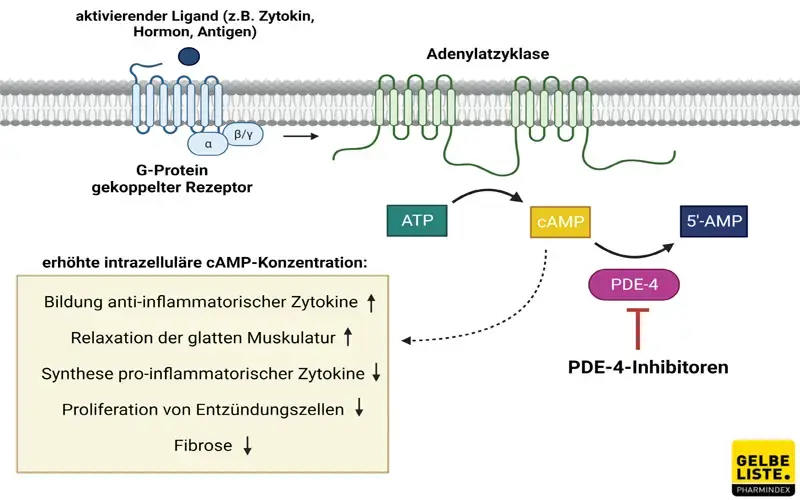
Eine Konsequenz des gestreigerten cAMP-Spiegels ist die Aktivierung der Proteinkinase A (PKA). Dies hat Einfluss auf folgende Signalwege in der Zelle:
- Die Phosphorylierung von CREB ("cAMP response element binding protein) und des Activating Transcription Factor 1 (ATF-1) führt zur Bildung anti-inflammatorischer Zytokine.
- Die Interaktion zwischen NFκB und dem CREB-Bindeprotein (CBP) wird beeinflusst. Dies hat zur Folge, dass die Bildung pro-inflammatorischer Zytokine unterdrückt wird.
- Die durch Bcl-6 (B-cell lymphoma 6 protein)-vermittelte Synthese proinflammatorischer Zytokine und die Proliferation von Entzündungszellen wird ebenfalls verhindert.
- Die Aktivierung der PKA resultiert zudem in der Relaxation der glatten Muskulatur und der Verlangsamung von fibrotischen Prozessen.
Neben der PKA wird durch die erhöhte cAMP-Konzentration auch das Epac-Protein (Isoform 1 und 2) aktiviert. Epac ist ein Guaninnukleotid-Austauschfaktor und ist nach der Bindung von cAMP in der Lage, die sogenannte Rap-GTPase in Gang zu bringen. Dadurch wird die Proliferation von Entzündungszellen sowie die Bildung proinflammatorischer Zytokine unterdrückt.
Roflumilast unterliegt einer intensiven Metabolisierung im menschlichen Körper. Der dabei entstehende aktive Hauptmetabolit ist Roflumilast-N-Oxid.
Pharmakokinetik
Resorption
- Die absolute Bioverfügbarkeit nach einmaliger oraler Gabe von 500 µg Roflumilast beträgt etwa 80%.
- Im nüchternen Zustand wurden maximale Plasmakonzentrationen in der Regel etwa eine Stunde nach Verarbreichung gemessen.
- Die maximale Konzentration des N-Oxid-Metaboliten wurde nach etwa acht Stunden erreicht.
- Die Aufnahme von Nahrung führt zu keiner Beeinflussung der Gesamt-PDE4-Inhibierungsaktivität, aber zu einer Verzögerung um eine Stunde bis zum Erreichen der maximalen Konzentrationen (tmax) von Roflumilast und zu einer Reduktion der Cmax um etwa 40%.
- Keinen Einfluss hat die Aufnahme von Nahrung dagegen auf die Cmax und tmax von Roflumilast-N-Oxid.
Verteilung
- Die Plasmaproteinbindung von Roflumilast und Roflumilast-N-Oxid beträgt etwa 99% bzw. 97%.
- Das Verteilungsvolumen bei einmaliger Gabe von 500 µg Roflumilast beträgt ungefähr 2,9 Liter/kg.
- Aufgrund seiner physiko-chemischen Eigenschaften verteilt sich der Wirkstoff leicht in Organen und Geweben einschließlich dem Fettgewebe.
- Einer frühen Distributionsphase mit ausgeprägter Verteilung ins Gewebe folgt sehr wahrscheinlich bedingt durch die Metabolisierung von Roflumilast zum Roflumilast-N-Oxid eine Eliminationsphase mit merklicher Umverteilung aus dem Fettgewebe.
- Studien mit radioaktiv markiertem Roflumilast an Ratten zeigten nur einen geringen Durchtritt durch die Blut-Hirn-Schranke.
- Es existieren keine Hinweise auf eine spezifische Akkumulation oder Retention des Wirkstoffes oder seinen Metaboliten in Organen oder im Fettgewebe.
Biotransformation
- Roflumilast wird intensiv durch Phase-I-Reaktionen durch das Cytochrom-P450-System und durch Phase-II-Reaktionen durch Konjugation metabolisiert.
- Roflumilast-N-Oxid ist der wichtigste im menschlichen Plasma beobachtete Metabolit.
- Die Plasma-AUC des N-Oxid-Metaboliten ist etwa zehnfach größer als die Plasma-AUC von Roflumilast. Daher wird der N-Oxid-Metabolit als die hauptbeitragende Substanz zur Gesamt-PDE4-Inhibierungsaktivität angesehen.
- Der Wirkstoff wird größtenteils durch CYP1A2 und CYP3A4 zum N-Oxid metabolisiert.
Elimination
- Die Plasma-Clearance nach einer intravenösen Kurzzeitinfusion von Roflumilast beträgt etwa 9,6 Liter/h.
- Nach oraler Gabe beträgt die mittlere effektive Plasmahalbwertszeit von Roflumilast etwa 17 Stunden und die seine N-Oxid-Metaboliten etwa 30 Stunden.
- Steady-state-Plasmakonzentrationen nach einmal täglicher Gabe wurden nach etwa vier Tagen (Roflumilast) bzw. sechs Tagen (Roflumilast-N-Oxid) erreicht.
- Nach oraler oder intravenöser Gabe von radioaktiv markiertem Roflumilast wurde ein radioaktiver Anteil von etwa 20% in den Fäzes und etwa 80% im Urin als inaktive Metaboliten wiedergefunden.
Die Pharmakokinetik von Roflumilast bzw. seinem N-Oxid-Metaboliten ist über einen Dosisbereich von 250 bis 1000 µg dosisproportional.
Dosierung
Die Dosierung von Roflumilast erfolgt in zwei Phasen: einer Anfangsdosis und einer Erhaltungsdosis.
Für die Anfangsdosis wird empfohlen, einmal täglich eine Tablette mit 250 µg Roflumilast für einen Zeitraum von 28 Tagen einzunehmen. Diese Anfangsdosis dient dazu, mögliche Nebenwirkungen und Therapieabbrüche zu reduzieren, die bei Beginn der Behandlung auftreten könnten. Es ist jedoch wichtig zu beachten, dass die 250 µg Dosis subtherapeutisch ist und daher ausschließlich als Anfangsdosis angewendet werden sollte.
Nach der 28-tägigen Behandlung mit der Anfangsdosis müssen die Patienten auf eine Erhaltungsdosis von einmal täglich einer Tablette mit 500 µg Roflumilast umgestellt werden. Es kann mehrere Wochen dauern, bis die volle Wirkung erreicht ist, weshalb der Wirkstoff in dieser Dosierung möglicherweise über einen längeren Zeitraum eingenommen werden muss.
Die Anwendung von Roflumilast in einer Dosis von 500 µg wurde in klinischen Studien mit einer Dauer von bis zu einem Jahr untersucht und ist für die Dauertherapie vorgesehen.
Nebenwirkungen
Am häufigsten (≥1/100 bis <1/10) traten als unerwünschte Arzneimittelwirkung Gewichtsverlust und verminderter Appetit, Schlafstörungen, Kopfschmerzen, Diarrhö, Übelkeit und Bauchschmerzen auf. In klinischen Studien sowie nach Markteinführung wurden seltene Fälle von suizidalen Gedanken und suizidalem Verhalten inklusive Suizid berichtet. Patienten und Pflegende sollten daher angehalten werden, den Arzt über solche Gedanken zu informieren.
Wechselwirkungen
Bei der Anwendung von Roflumilast sind folgende Wechselwirkungen zu beachten:
- CYP-Inhibitoren (z.B. Enoxacin, Cimetidin, Fluvoxamin) können zur Erhöhung der Wirkstoff-Exposition und zur andauernden Unverträglichkeit führen.
- CYP-Induktoren (z.B. Rifampicin, Phenobarbital, Carbamazepin, Phenytoin) können zu einer reduzierten therapeutischen Wirksamkeit von Roflumilast führen.
Kontraindikationen
Roflumilast besitzt folgende Kontraindikationen:
- Überempfindlichkeit gegen den Wirkstoff
- Mittelschwere bis schwere Leberfunktionsstörung
Schwangerschaft
In tierexperimentellen Studien wurde eine Reproduktionstoxizität festgestellt. Zudem passiert der Wirkstoff die Plazentaschranke. Die Anwendung von Roflumilast während der Schwangerschaft wird daher nicht empfohlen.
Frauen im gebärfähigen Alter sollten angewiesen werden, während der Behandlung mit Roflumilast eine zuverlässige Verhütungsmethode anzuwenden.
Stillzeit
Vorliegende pharmakokinetische Daten bei Tieren zeigen, dass Roflumilast und/oder seine Metaboliten in die Milch übergehen. Roflumilast sollte daher während der Stillzeit nicht angewendet werden.
Verkehrstüchtigkeit
Roflumilast hat keinen Einfluss auf die Verkehrstüchtigkeit und die Fähigkeit zum Bedienen von Maschinen.
Anwendungshinweise
- Roflumilast ist nicht als Notfallarzneimittel zur Therapie des akuten Bronchospasmus indiziert.
- Sie sollten Ihr Körpergewicht regelmäßig überprüfen. Informieren Sie Ihren Arzt, wenn Sie während der Einnahme von Roflumilast einen unbeabsichtigten Gewichtsverlust bemerken, der nicht auf eine Diät oder ein Trainings-Programm zurückzuführen ist.
- Aufgrund nicht ausreichender entsprechender Erfahrungen sollte die Therapie mit Roflumilast bei Patienten mit den folgenden Erkrankungen nicht begonnen bzw. eine bestehende Behandlung beendet werden: schwere immunologische Erkrankungen (z. B. HIV-Infektion, multiple Sklerose, Lupus erythematodes, progressive multifokale Leukoenzephalopathie), schwere akute Infektionskrankheiten sowie Krebserkrankungen (ausgenommen Basalzellkarzinomen); dies gilt auch für Patienten, die mit Immunsuppressiva (d.h. Methotrexat, Azathioprin, Infliximab, Etanercept oder oralen Kortikosteroiden zur Langzeitanwendung, ausgenommen systemische Kortikosteroide zur kurzzeitigen Anwendung) behandelt werden. Die Erfahrungen bei Patienten mit latenten Infektionen wie Tuberkulose, viraler Hepatitis, viraler Herpesinfektion und Herpes zoster sind begrenzt. Patienten mit Herzinsuffizienz (NYHA-Grad 3 und 4) wurden nicht untersucht, deshalb wird bei diesen Patienten eine Therapie Roflumilast nicht empfohlen.
- Während der ersten Wochen der Behandlung mit Roflumilast können Symptome wie Durchfall, Übelkeit, Bauchschmerzen oder Kopfschmerzen auftreten. Sprechen Sie bitte mit Ihrem Arzt, wenn diese nicht innerhalb der ersten Wochen der Behandlung abklingen.
- Roflumilast wird nicht empfohlen bei Patienten, die in der Vorgeschichte Depressionen in Verbindung mit Selbsttötungsgedanken oder –verhalten zeigten. Während der Einnahme können weiterhin Schlafstörungen, Angstzustände, Nervosität oder depressive Verstimmungen auftreten. Weisen Sie Ihren Arzt vor der Einnahme von Roflumilast darauf hin, falls Sie an diesen Symptomen leiden oder Sie andere Arzneimittel nehmen, denn diese könnten die Wahrscheinlichkeit des Auftretens der oben genannten Nebenwirkungen erhöhen. Weisen Sie oder der Pflegende Ihren Arzt ebenso umgehend darauf hin, wenn Sie möglicherweise Stimmungs- oder Verhaltensänderungen oder Selbsttötungsgedanken haben.
- Das Arzneimittel sollte nicht bei Kindern und Jugendlichen unter 18 Jahren angewendet werden.
- Es liegen keine klinischen Daten zu einer begleitenden Theophyllin-Dauertherapie vor, daher wird diese nicht empfohlen.
- Nebenwirkungen wie Durchfall, Übelkeit, Bauchschmerzen oder Kopfschmerzen treten hauptsächlich während der ersten Wochen der Therapie auf und klingen meistens im Verlauf der weiteren Behandlung ab. Bei einer andauernden Unverträglichkeit sollte die Therapie mit Roflumilast überprüft werden. Dies kann bei bestimmten Patientengruppen der Fall sein, die einer höheren Exposition ausgesetzt sind, z. B. Nichtraucherinnen mit schwarzer Hautfarbe oder bei Patienten, die gleichzeitig mit CYP1A2/2C19/3A4-Inhibitoren (wie Fluvoxamin und Cimetidin) oder dem CYP1A2/3A4-Inhibitor Enoxacin behandelt werden.
Wirkstoff-Informationen
- EMA-Produktinformation zu Daxas (Roflumilast)
- Li et al. (2018): Phosphodiesterase-4 Inhibitors for the Treatment of Inflammatory Diseases. Frontiers in Pharmacology, DOI: https://doi.org/10.3389/fphar.2018.01048
- Mulhall et al. (2015): Phosphodiesterase 4 inhibitors for the treatment of chronic obstructive pulmonary disease: A review of current and developing drugs. Expert Opinion on Investigational Drugs, DOI: 10.1517/13543784.2015.1094054
- Sehrawat et al. (2008): Role of Epac1, an Exchange Factor for Rap GTPases, in Endothelial Microtubule Dynamics and Barrier Function. Molecular Biology of the Cell, DOI: https://doi.org/10.1091/mbc.e06-10-0972
Abbildung:
Anika Mifka adapted from Li et al. (2018): Phosphodiesterase-4 Inhibitors for the Treatment of Inflammatory Diseases. Frontiers in Pharmacology, DOI: https://doi.org/10.3389/fphar.2018.01048; Mulhall et al. (2015): Phosphodiesterase 4 inhibitors for the treatment of chronic obstructive pulmonary disease: A review of current and developing drugs. Expert Opinion on Investigational Drugs, DOI: 10.1517/13543784.2015.1094054
-
Daxas® 250 Mikrogramm Tabletten
AstraZeneca GmbH
-
Daxas 500 Mikrogramm 101 Carefarm Filmtabletten
1 0 1 Carefarm GmbH
-
Daxas 500 Mikrogramm Abacus Filmtabletten
Abacus Medicine A/S
-
Daxas 500 Mikrogramm axicorp Filmtabletten
axicorp Pharma GmbH
-
Daxas 500 Mikrogramm Beragena Filmtabletten
Docpharm GmbH
-
Daxas 500 Mikrogramm CC Pharma Filmtabletten
CC Pharma GmbH
-
Daxas 500 Mikrogramm Emra Filmtabletten
Emra-Med Arzneimittel GmbH
-
Daxas 500 Mikrogramm Eurim Filmtabletten
Eurim-Pharm Arzneimittel GmbH
-
Daxas® 500 Mikrogramm Filmtabletten
AstraZeneca GmbH
-
Daxas 500 Mikrogramm Gerke Filmtabletten
Pharma Gerke Arzneimittelvertriebs GmbH
-
Daxas 500 Mikrogramm kohlpharma Filmtabletten
kohlpharma GmbH
-
Daxas 500 Mikrogramm Mpa Pharma Filmtabletten
Mpa Pharma GmbH
-
Roflum HEXAL® 500 Mikrogramm Filmtabletten
Hexal AG
-
RoflumilaPUREN 250 Mikrogramm Tabletten
PUREN Pharma GmbH & Co. KG
-
RoflumilaPUREN 500 Mikrogramm Tabletten
PUREN Pharma GmbH & Co. KG
-
Roflumilast Abdi 500 Mikrogramm Filmtabletten
Abdi Farma GmbH
-
Roflumilast Accord 500 Mikrogramm Filmtabletten
Accord Healthcare GmbH
-
Roflumilast AL 500 Mikrogramm Filmtabletten
ALIUD PHARMA® GmbH
-
Roflumilast beta 500 Mikrogramm Filmtabletten
betapharm Arzneimittel GmbH
-
Roflumilast ELPEN 500 Mikrogramm Filmtabletten
ELPEN Pharmaceutical Co. Inc.
-
Roflumilast Heumann 250 Mikrogramm Tabletten
Heumann Pharma GmbH & Co. Generica KG
-
Roflumilast Heumann 500 Mikrogramm Filmtabletten
Heumann Pharma GmbH & Co. Generica KG
-
Roflumilast Heumann 500 Mikrogramm Filmtabletten Heunet
Heunet Pharma GmbH











