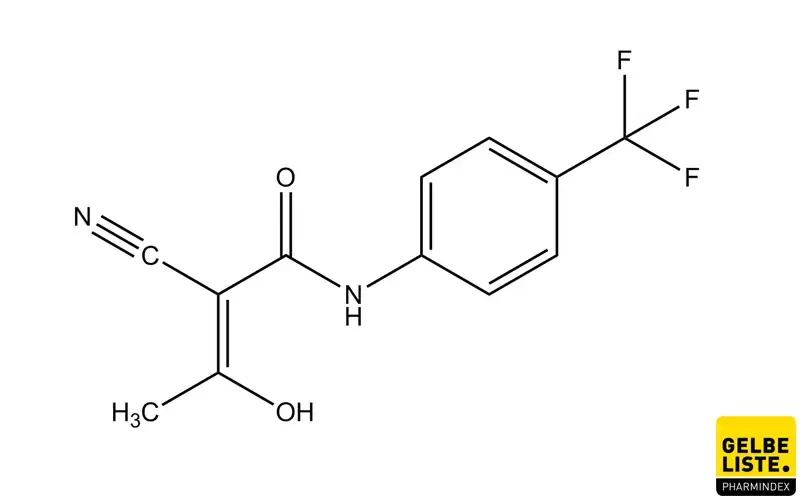
Teriflunomid
Teriflunomid ist ein selektiver Immunmodulator mit antiproliferativer und entzündungshemmender Wirkung, der hauptsächlich in der Behandlung der schubförmig remittierenden Multiplen Sklerose eingesetzt wird. Es inhibiert spezifisch das Enzym Dihydroorotat-Dehydrogenase, was zu einer Reduktion der Pyrimidinsynthese führt und somit die Aktivität und Proliferation von T- und B-Lymphozyten begrenzt.
Teriflunomid: Übersicht
Anwendung
Teriflunomid ist der Hauptmetabolit von Leflunomid und für die Behandlung der schubförmig remittierenden Multiplen Sklerose (RRMS) zugelassen, um die Häufigkeit der Schübe zu reduzieren und das Fortschreiten der körperlichen Behinderung zu verlangsamen.
Wirkmechanismus
Teriflunomid wirkt als selektiver Inhibitor der mitochondrialen Dihydroorotat-Dehydrogenase (DHODH), einem Schlüsselenzym im de novo Pyrimidinsyntheseweg. Diese Hemmung führt zu einer reduzierten Produktion von Pyrimidinnukleotiden, die für die DNA-Synthese und somit für die Proliferation von Lymphozyten essenziell sind.
Indem Teriflunomid die Expansion aktivierter T- und B-Lymphozyten begrenzt, ohne die Funktionen der ruhenden Lymphozyten wesentlich zu beeinträchtigen, moduliert es selektiv das Immunsystem. Dies resultiert in einer verminderten Immunreaktion gegen die Myelinscheiden im Zentralnervensystem, was die Entzündungsaktivität und die Entwicklung neuer Läsionen bei Multipler Sklerose reduziert. Folglich trägt Teriflunomid zur Verringerung der Schubrate und zur Verlangsamung der Krankheitsprogression bei schubförmig remittierender Multipler Sklerose bei.
Dosierung
Erwachsene:
- Empfohlene Dosis: 14 mg einmal täglich
Kinder und Jugendliche (ab 10 Jahren):
- Körpergewicht > 40 kg: 14 mg einmal täglich
- Körpergewicht ≤ 40 kg: 7 mg einmal täglich
- Verfügbarkeit von Tabletten in geringerer Stärke (7 mg) für Patienten ≤ 40 kg
- Bei Erreichen eines stabilen Körpergewichts von mehr als 40 kg: Umstellung auf 14 mg täglich
- Einnahme: Mit oder ohne Nahrung möglich
Besondere Patientengruppen:
- Ältere Patienten (ab 65 Jahren): Vorsichtige Anwendung aufgrund begrenzter Daten zu Sicherheit und Wirksamkeit
- Patienten mit eingeschränkter Nierenfunktion: Keine Dosisanpassung erforderlich für Patienten mit leichter bis schwerer Beeinträchtigung, die sich keiner Dialyse unterziehen
- Patienten mit schwerer Nierenfunktionsbeeinträchtigung, die dialysepflichtig sind: Nicht untersucht und kontraindiziert
- Patienten mit eingeschränkter Leberfunktion: Keine Dosisanpassung erforderlich bei leichter und mittelschwerer Beeinträchtigung. Kontraindiziert bei schwerer Beeinträchtigung der Leberfunktion
Nebenwirkungen
Zu den häufigen Nebenwirkungen, die während einer Therapie mit Teriflunomid auftreten können, zählen:
- Infektionen und parasitäre Erkrankungen: Grippe, Infektion der oberen Atemwege, Harnwegsinfektion, Bronchitis, Sinusitis, Pharyngitis, Zystitis, virale Gastroenteritis, Herpesvirus-Infektionen, Zahninfektion, Laryngitis, Tinea pedis
- Neutropenie, Anämie
- Leichte allergische Reaktionen
- Angst
- Parästhesie, Ischialgie, Karpaltunnelsyndrom
- Palpitationen
- Hypertonie
- Oberbauchschmerzen, Erbrechen, Zahnschmerzen
- Gamma-Glutamyltransferase (GGT) erhöht, Aspartat-Aminotransferase erhöht
- Exanthem, Akne
- Schmerzen des Muskel- und Skelettsystems, Myalgie, Arthralgie
- Pollakisurie
- Menorrhagie
- Schmerz, Asthenie
- Gewichtsabnahme
- Erniedrigte Neutrophilenzahlund Leukozytenzahl
- erhöhte Kreatinin-Phosphokinasewerte
Wechselwirkungen
Pharmakokinetische Wechselwirkungen:
- Teriflunomid wird hauptsächlich durch Hydrolyse verarbeitet, wobei Oxidation eine untergeordnete Rolle spielt.
- Starke Induktoren von Cytochrom-P450 (CYP) und Transportern wie Rifampicin können die Wirkung von Teriflunomid um 40% verringern. Ähnliche Vorsicht gilt für Carbamazepin, Phenobarbital, Phenytoin und Johanniskraut.
- Die Anwendung von Colestyramin oder Aktivkohle kann, sofern keine beschleunigte Elimination beabsichtigt ist, die Teriflunomid-Konzentration im Blut signifikant senken.
Wechselwirkungen mit spezifischen Medikamenten:
- Teriflunomid kann die Wirkung von CYP2C8-Substraten wie Repaglinid erhöhen, was eine vorsichtige Anwendung solcher Medikamente während der Teriflunomid-Behandlung erfordert.
- Die Exposition gegenüber oralen Kontrazeptiva kann durch Teriflunomid erhöht werden, was bei der Auswahl dieser Medikamente berücksichtigt werden sollte.
- Teriflunomid könnte ein schwacher Induktor von CYP1A2 sein, was die Wirksamkeit von CYP1A2-Substraten wie Coffein verringern kann.
- Bei gleichzeitiger Anwendung von Teriflunomid und Warfarin ist eine engmaschige Überwachung der INR-Werte empfohlen, da Teriflunomid die INR-Peaks um 25% senken kann.
- Teriflunomid hemmt den organischen Anionen-Transporter 3 (OAT3), was die Wirkung von OAT3-Substraten wie Cefaclor erhöhen kann.
- Die gleichzeitige Anwendung von Teriflunomid mit Substraten von BCRP und/oder OATP1B1/B3 kann die Exposition gegenüber diesen Medikamenten erhöhen, was eine Dosisanpassung erforderlich machen könnte.
Kontraindikationen
Teriflunomid darf nicht angewendet werden bei:
- Überempfindlichkeit gegen den Wirkstoff
- Patienten mit schwerer Beeinträchtigung der Leberfunktion (Child-Pugh-Stadium C)
- Schwangeren oder Frauen im gebärfähigen Alter, die während der Behandlung mit Teriflunomid und so lange, wie die Plasmaspiegel über 0,02 mg/l liegen, keine zuverlässige Verhütungsmethode anwenden. Eine Schwangerschaft muss vor Beginn der Behandlung ausgeschlossen werden
- Stillenden Frauen
- Patienten mit schwer beeinträchtigtem Immunstatus, z. B. erworbenem Immunschwächesyndrom (AIDS)
- Patienten mit signifikant beeinträchtigter Knochenmarkfunktion oder signifikanter Anämie, Leukopenie, Neutropenie oder Thrombozytopenie.
- Patienten mit schwerer aktiver Infektion, bis diese sich zurückgebildet hat
- Patienten mit schweren Nierenfunktionsstörungen, die sich Dialysen unterziehen, da die klinische Erfahrung bei dieser Patientengruppe unzureichend ist
- Patienten mit schwerer Hypoproteinämie, z. B. beim nephrotischen Syndrom
Schwangerschaft
Da Teriflunomid schwerwiegende Schädigungen des Ungeborenen verursachen kann, wenn es während der Schwangerschaft angewendet wird, ist der Wirkstoff während der Schwangerschaft kontraindiziert.
Frauen in gebärfähigem Alter müssen darauf hingewiesen werden, dass nach Absetzen der Therapie eine Wartezeit von 2 Jahren erforderlich ist, bevor sie schwanger werden dürfen. Ist eine Wartezeit von bis zu etwa 2 Jahren mit verlässlichem Empfängnisschutz nicht praktikabel, kann die vorsorgliche Einleitung von Auswaschmaßnahmen ratsam sein.
Verkehrstüchtigkeit
Teriflunomid hat keinen oder einen vernachlässigbaren Einfluss auf die Verkehrstüchtigkeit und die Fähigkeit zum Bedienen von Maschinen.
Anwendungshinweise
Bei der Anwendung von Teriflunomid sind folgende Vorsichtsmaßnahmen und Überwachungen wichtig, um die Sicherheit der Patienten zu gewährleisten:
Vor der Behandlung
- Überprüfung von Blutdruck, Alaninaminotransferase (ALT/SGPT) und einem großen Blutbild.
Während der Behandlung
- Regelmäßige Kontrolle des Blutdrucks.
- Überwachung der Leberenzyme, besonders in den ersten 6 Monaten, dann regelmäßig. Bei Patienten mit vorbestehender Lebererkrankung oder bei Anwendung von potenziell leberschädigenden Medikamenten ist besondere Vorsicht geboten.
- Bei Anzeichen von Leberschäden (z.B. Übelkeit, Erbrechen, Bauchschmerzen) sollte die Behandlung überdacht und gegebenenfalls ein beschleunigtes Eliminationsverfahren angewendet werden.
- Überwachung des großen Blutbilds bei Anzeichen von Infektionen.
Beschleunigte Elimination
- Teriflunomid wird langsam ausgeschieden, ohne beschleunigte Elimination kann dies bis zu 2 Jahre dauern.
- Ein beschleunigtes Eliminationsverfahren kann jederzeit nach Beendigung der Behandlung angewendet werden.
Leberwirkungen
- Erhöhungen der Leberenzyme sind häufig, besonders in den ersten 6 Monaten.
- Bei Anzeichen von Leberschäden ist eine engmaschige Überwachung und möglicherweise ein Abbruch der Behandlung erforderlich.
Blutdruck
- Blutdruckerhöhungen können auftreten und sollten vor und während der Behandlung überwacht werden.
Infektionen
- Der Beginn der Behandlung sollte bei schweren aktiven Infektionen verschoben werden.
- Unter Behandlung mit Teriflunomid wurden Fälle von Herpesvirus-Infektionen (z. B. oralen Herpes und Herpes Zoster berichtet, die zum Teil einen schweren Verlauf aufgewiesen haben (einschließlich herpetischer Meningoenzephalitis und disseminiertem Herpes).
- Bei Entwicklung einer schweren Infektion jeglicher Art während der Behandlung kann ein Abbruch notwendig sein.
Wirkstoff-Informationen
- Fachinformation Teriflunomid-ratiopharm
- Warnke, Clemens, et al. "Teriflunomide for treatment of multiple sclerosis." Der Nervenarzt 84 (2013): 724-731.
- Bar-Or, Amit, et al. "Teriflunomide and its mechanism of action in multiple sclerosis." Drugs 74 (2014): 659-674.
- Umsetzung des Durchführungsbeschlusses der Europäischen Kommission zum PSUR Single Assessment betreffend die Zulassungen für Humanarzneimittel mit dem Wirkstoff Teriflunomid vom 26.07.2024, abgerufen am 29.01.2025
-
Aubagio 7 mg Abacus Filmtabletten
Abacus Medicine A/S
-
AUBAGIO® 7 mg Filmtabletten
Sanofi-Aventis Deutschland GmbH
-
Aubagio 14 mg Abacus Filmtabletten
Abacus Medicine A/S
-
Aubagio 14 mg axicorp B.V. Filmtabletten
axicorp Pharma B.V.
-
Aubagio 14 mg CC Pharma Filmtabletten
CC Pharma GmbH
-
Aubagio 14 mg Eurim Filmtabletten
Eurim-Pharm Arzneimittel GmbH
-
Aubagio 14 mg European Filmtabletten
European Pharma B.V.
-
Aubagio 14 mg Fd Pharma Filmtabletten
FD Pharma GmbH
-
AUBAGIO® 14 mg Filmtabletten
Sanofi-Aventis Deutschland GmbH
-
Aubagio 14 mg kohlpharma Filmtabletten
kohlpharma GmbH
-
Aubagio 14 mg Orifarm Filmtabletten
Orifarm GmbH
-
Aubagio 14 mg Originalis Filmtabletten
Originalis B.V.
-
Aubagio 14 mg Paranova Filmtabletten
Paranova Pack A/S
-
Teriflago® 14 mg Filmtabletten
TAD Pharma GmbH
-
Teriflunomid - 1 A Pharma® 14 mg Filmtabletten
1 A Pharma GmbH
-
Teriflunomid 123 Acurae Pharma® 14 mg Filmtabletten
123 Acurae Pharma GmbH
-
Teriflunomid Abdi 14 mg Filmtabletten
Abdi Farma GmbH
-
Teriflunomid Accord 14 mg Filmtabletten
Accord Healthcare GmbH
-
Teriflunomid AL 14 mg Filmtabletten
ALIUD PHARMA® GmbH
-
Teriflunomid Amarox 7 mg Filmtabletten
Amarox Pharma GmbH
-
Teriflunomid Amarox 14 mg Filmtabletten
Amarox Pharma GmbH
-
Teriflunomid Aurobindo 14 mg Filmtabletten
PUREN Pharma GmbH & Co. KG
-
Teriflunomid beta 14 mg Filmtabletten
betapharm Arzneimittel GmbH
-
Teriflunomid Devatis 14 mg Filmtabletten
Devatis GmbH
-
Teriflunomid Glenmark 14 mg Filmtabletten
Glenmark Arzneimittel GmbH
-
Teriflunomid Heumann 14 mg Filmtabletten
Heumann Pharma GmbH & Co. Generica KG
-
Teriflunomid HEXAL® 14 mg Filmtabletten
Hexal AG
-
Teriflunomid Mylan 14 mg 101 Carefarm Filmtabletten
1 0 1 Carefarm GmbH
-
Teriflunomid Mylan 14 mg Abacus Filmtabletten
Abacus Medicine A/S
-
Teriflunomid Mylan 14 mg Filmtabletten
Viatris Healthcare GmbH
-
Teriflunomid neuraxpharm 14 mg Filmtabletten
neuraxpharm Arzneimittel GmbH
-
Teriflunomid PUREN 14 mg Filmtabletten
PUREN Pharma GmbH & Co. KG
-
Teriflunomid-ratiopharm® 14 mg Filmtabletten
ratiopharm GmbH
-
Teriflunomid STADA® 14 mg Filmtabletten
STADAPHARM GmbH
-
Teriflunomid Viatris 14 mg BB Farma Filmtabletten
BB Farma S.R.L.
-
Teriflunomid Vivanta 14 mg Filmtabletten
Vivanta Generics s.r.o
-
Teriflunomid Zentiva 14 mg Filmtabletten
Zentiva Pharma GmbH
-
TerifluViatris 14 mg Filmtabletten
Viatris Healthcare GmbH














