Daratumumab
Daratumumab ist ein monoklonaler Antikörper gegen CD38, der für verschiedene Stadien des multiplen Myeloms, für schwelendes multiples Myelom mit hohem Progressionsrisiko sowie für die systemische AL-Amyloidose in Kombinationstherapie zugelassen ist.
Daratumumab : Übersicht
Anwendung
Daratumumab ist indiziert bei Erwachsenen:
- Multiples Myelom: in Kombinationen (Lenalidomid+Dexamethason; Bortezomib+Melphalan+Prednison; Bortezomib+Lenalidomid+Dexamethason; Bortezomib+Thalidomid+Dexamethason; Pomalidomid+Dexamethason; Bortezomib+Dexamethason) in den jeweils zugelassenen Situationen (neu diagnostiziert – mit/ohne ASZT-Eignung; ≥1 Vortherapie; refraktär gegenüber Lenalidomid etc.) sowie als Monotherapie nach Vorbehandlung mit Proteasom-Inhibitor und Immunmodulator.
- Schwelendes multiples Myelom (hohes Progressionsrisiko) als Monotherapie.
- Systemische Leichtketten-(AL)-Amyloidose in Kombination mit Cyclophosphamid, Bortezomib und Dexamethason.
Anwendungsart
Daratumumab wird ausschließlich subkutan injiziert: 15 ml (1 800 mg) über ca.3–5 Min in das subkutane Bauchgewebe ~7,5 cm rechts/links des Nabels; Injektionsstellen rotieren; nicht in gerötete/indurierte/narbige Areale; bei Schmerzen Applikationsgeschwindigkeit reduzieren oder Restdosis kontralateral injizieren. Keine Ko-Applikation anderer SC-Arzneimittel an derselben Stelle.
Anwendungshinweise
Folgende Warnhinweise und Vorsichtsmaßnahmen sind bei der Anwendung von Daratumumab zu beachten:
- Injektionsbedingte Reaktionen: Bei subkutaner Gabe können Reaktionen auftreten, insbesondere bei der ersten Injektion. Diese reichen von milden Symptomen (z. B. Übelkeit, Schüttelfrost, Husten) bis hin zu schwerwiegenden Ereignissen. Eine Prämedikation (z. B. mit Kortikosteroiden, Antipyretika, Antihistaminika) ist erforderlich. Die Patienten sollten nach der ersten Gabe überwacht werden.
- Beeinflussung serologischer Tests: Daratumumab kann den indirekten Antiglobulin-Test (Coombs-Test) beeinflussen, da es an CD38 auf Erythrozyten bindet. Dies kann Blutgruppenbestimmungen und Antikörper-Screenings stören. Vor Therapiebeginn sollte ein vollständiger Blutgruppennachweis inklusive Antikörpersuchtest erfolgen.
- Beeinträchtigung der elektrophoretischen Nachweismethoden: Daratumumab ist ein monoklonaler IgGκ-Antikörper und kann in Immunfixations- und Serum-Elektrophorese-Assays als M-Protein erscheinen, was die Bewertung des Therapieansprechens beeinflussen kann.
- Neutropenie und Thrombozytopenie: Häufig treten hämatologische Toxizitäten auf, insbesondere in Kombination mit anderen Wirkstoffen. Regelmäßige Blutbildkontrollen sind notwendig. Bei ausgeprägter Zytopenie kann eine Dosisreduktion oder Therapieunterbrechung erforderlich sein.
- Infektionen: Patienten unter Daratumumab-Therapie haben ein erhöhtes Risiko für bakterielle, virale und opportunistische Infektionen. Eine antivirale Prophylaxe gegen Herpes-Zoster-Reaktivierung wird empfohlen.
- Reaktivierung von Hepatitis B: Vor Therapiebeginn muss der HBV-Status bestimmt werden. Patienten mit positiver Serologie benötigen engmaschige virologische Kontrolle. Bei Reaktivierung ist die Therapie sofort zu unterbrechen.
- Chronisch obstruktive Lungenerkrankung (COPD): Bei COPD-Patienten ist das Risiko für Atemwegsreaktionen erhöht. Eine prophylaktische Gabe von Bronchodilatatoren und Inhalationssteroiden sollte erwogen werden.
- Beeinflussung der Fruchtbarkeit: Es liegen keine Daten zur Fertilität beim Menschen vor, jedoch zeigten Tierstudien eine mögliche Beeinträchtigung männlicher Fortpflanzungsorgane.
- Herz-Kreislauf-Komplikationen: Bei Kombinationstherapien mit bekannten kardiotoxischen Substanzen (z. B. Carfilzomib) sind kardiovaskuläre Nebenwirkungen möglich. Eine engmaschige Überwachung wird empfohlen.
Wirkmechanismus
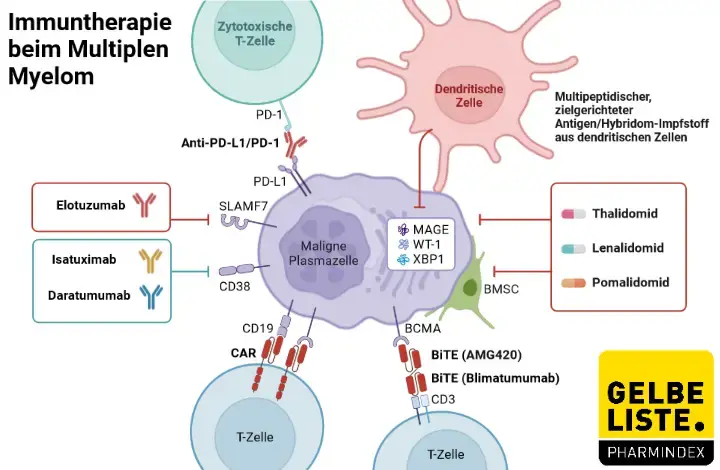
Der monoklonale Antikörper Daratumumab bindet gezielt an das CD38-Protein, das auf der Oberfläche von malignen Plasmazellen und anderen Zelltypen exprimiert wird. Diese Bindung löst die Zerstörung der Tumorzellen (Tumorzelllyse) über mehrere immunologische Mechanismen aus, darunter die komplementabhängige Zytotoxizität, die antikörperabhängige zellvermittelte Zytotoxizität sowie die Phagozytose. Darüber hinaus entfaltet Daratumumab immunmodulatorische Effekte, die sich in einer Zunahme von CD4+- und CD8+-T-Zellen sowie einer erhöhten T-Zell-Klonalität zeigen.
Die subkutane Formulierung enthält zusätzlich rekombinante humane Hyaluronidase (rHuPH20), welche durch den vorübergehenden Abbau von Hyaluronan im Gewebe die Verabreichung des Wirkstoffs unter die Haut erleichtert.
Pharmakokinetik
Resorption
- Die subkutane Bioverfügbarkeit von Daratumumab beträgt ca. 70 %.
- Maximale Serumkonzentrationen werden ca. 5 Tage nach der Injektion erreicht.
Verteilung
- Das Verteilungsvolumen im steady-state liegt bei etwa 4,7 L.
- Daratumumab verteilt sich primär im intravasalen Raum.
Metabolisierung
- Daratumumab wird wie endogene IgG-Antikörper über zelluläre katabolische Prozesse in Aminosäuren abgebaut.
- Es erfolgt keine Metabolisierung über Leberenzyme.
Elimination
- Die terminale Halbwertszeit beträgt ca. 18 Tage.
- Die Clearance ist nicht dosisproportional, sondern wird durch Zielantigen-vermittelte Elimination beeinflusst.
Besondere Hinweise
- Bei Patienten mit Nieren- oder Leberfunktionsstörung sind keine Dosisanpassungen erforderlich.
- Es liegen keine Daten zur Anwendung bei Kindern und Jugendlichen unter 18 Jahren vor.
- Bei einem Körpergewicht über 120 kg kann die Wirksamkeit reduziert sein.
Dosierung
Die Dosierung von Daratumumab richtet sich nach Indikation, Kombination und Behandlungsphase:
- Standarddosis: 1 800 mg subkutan, verabreicht über 3–5 Minuten.
- Initial wöchentlich (z. B. Wochen 1–8), danach alle zwei Wochen (z. B. Wochen 9–24), anschließend alle vier Wochen bis zur Progression.
- Für jede Kombination (z. B. D-VMP, D-Rd, D-VTd, D-VRd, D-Pd, D-VCd) gelten spezifische Zyklenpläne laut Fachinformation.
Prä-/Postmedikation: Antihistaminikum, Antipyretikum, Kortikosteroid (Regimeabhängigkeit beachten); bei SMM an Tag 1 Zyklus 1 Leukotrien-Antagonist erwägen; antivirale Prophylaxe gegen Herpes-zoster in Erwägung ziehen. Postmedikation mit niedrig dosiertem Steroid nach FI.
Dosisanpassungen: Keine Reduktionen empfohlen; ggf. Applikation verzögern bei hämatologischer Toxizität. Versäumte Dosis baldmöglichst nachholen, Intervall beibehalten.
Nebenwirkungen
Häufige Nebenwirkungen (≥1/10) sind:
- Infektionen: Infektionen der oberen Atemwege, Pneumonie, COVID-19
- Hämatologisch: Neutropenie, Thrombozytopenie, Anämie
- Allgemein: Müdigkeit, Fieber, peripheres Ödem, Reaktionen an der Injektionsstelle
- Gastrointestinal: Diarrhö, Obstipation, Übelkeit
- Atemwege: Husten, Dyspnoe
- Nervensystem: Kopfschmerzen, periphere Neuropathie
- Immunologisch: Hypogammaglobulinämie, Infusionsreaktionen (IRRs)
Wechselwirkungen
Folgende Wechselwirkungen sind bei der Anwendung von Daratumumab zu beachten:
- Indirekter Coombs-Test: Daratumumab kann durch Bindung an CD38 auf Erythrozyten zu falsch positiven Testergebnissen führen.
- Interferenz mit Immunfixation: Daratumumab kann die Nachweisbarkeit von M-Protein durch Serum-Protein-Elektrophorese und Immunfixations-Assays beeinträchtigen.
- Pharmakokinetische Interaktionen: Keine klinisch relevanten Wechselwirkungen mit Kombinationspartnern wie Lenalidomid, Bortezomib, Dexamethason oder Cyclophosphamid.
Kontraindikation
Daratumumab darf nicht angewendet werden bei Überempfindlichkeit gegen Daratumumab oder einen der sonstigen Bestandteile.
Schwangerschaft
Die Anwendung von Daratumumab während der Schwangerschaft wird nicht empfohlen; Erfahrungen sind sehr begrenzt. Frauen im gebärfähigen Alter sollen während der Behandlung und bis 3 Monate danach zuverlässig verhüten. Eine Anwendung sollte nur erfolgen, wenn der potenzielle Nutzen das mögliche Risiko überwiegt.
Stillzeit
Es ist unbekannt, ob Daratumumab in die Muttermilch übergeht; ein Risiko für das Neugeborene/Kind kann nicht ausgeschlossen werden. Es ist individuell zu entscheiden, ob das Stillen zu unterbrechen ist oder die Therapie mit Daratumumab ausgesetzt/unterlassen wird, unter Abwägung von Nutzen für Kind und Mutter.
Alternativen
Als mögliche Alternativen zu Daratumumab kommen folgende Wirkstoffe infrage:
CD38-Antikörper:
Isatuximab – ebenfalls gegen CD38 gerichtet; zugelassen zur Behandlung des rezidivierten/refraktären multiplen Myeloms in Kombination mit Pomalidomid und Dexamethason (nach ≥2 Vortherapien) oder Carfilzomib und Dexamethason (ab ≥1 Vortherapie).
SLAMF7-Antikörper:
Elotuzumab – ein monoklonaler Antikörper gegen SLAMF7, zugelassen in Kombination mit Lenalidomid/Dexamethason oder Pomalidomid/Dexamethason bei rezidiviertem/refraktärem Myelom. Eine Monotherapie ist nicht vorgesehen.
Proteasom-Inhibitoren (PI):
Bortezomib, Carfilzomib, Ixazomib – essenzielle Bausteine in verschiedenen Kombinationstherapien beim multiplen Myelom.
Immunmodulatoren (IMiDs):
Lenalidomid, Pomalidomid, Thalidomid – weit verbreitet in der Erstlinientherapie und bei Rückfällen.
Alkylanzien:
Cyclophosphamid, Melphalan – insbesondere in nicht-transplantablen Situationen oder bei AL-Amyloidose.
Kortikosteroide:
Dexamethason, Prednison – universell eingesetzte Kombinationspartner in nahezu allen Therapieregimen.
Verkehrstüchtigkeit
Daratumumab hat keinen oder vernachlässigbaren Einfluss auf die Verkehrstüchtigkeit und das Bedienen von Maschinen; Fatigue kann auftreten und ist zu berücksichtigen.
- Fachinformation „DARZALEX 1 800 mg Injektionslösung“, Stand Juli 2025. DE-PL-0063.pdf
-
DARZALEX® 20 mg/ml Konzentrat zur Herstellung einer Infusionslösung, 5 ml
Janssen-Cilag GmbH
-
DARZALEX® 20 mg/ml Konzentrat zur Herstellung einer Infusionslösung, 20 ml
Janssen-Cilag GmbH
-
Darzalex 1800 mg Abacus Injektionslösung, 15 ml
Abacus Medicine A/S
-
DARZALEX® 1800 mg Injektionslösung, 15 ml
Janssen-Cilag GmbH














