Liraglutid
Liraglutid ist ein langwirksames Analogon des humanen Glucagon-like Peptide-1 (GLP-1), das zur Behandlung von Typ-2-Diabetes mellitus sowie zur Gewichtsreduktion bei Adipositas und übergewichtigem metabolischem Risikoprofil eingesetzt wird. Der Wirkstoff bindet an GLP-1-Rezeptoren und entfaltet dort blutzucker- sowie appetitregulierende Effekte.
Liraglutid: Übersicht
Anwendung
Liraglutid wird angewendet bei:
Typ-2-Diabetes mellitus
- Als Monotherapie, wenn Metformin ungeeignet ist.
- In Kombination mit anderen Antidiabetika, einschließlich Insulin, zur Verbesserung der Blutzuckerkontrolle bei Erwachsenen und Jugendlichen ab 10 Jahren.
Adipositas
- Bei Erwachsenen mit einem BMI ≥30 kg/m² (Adipositas) oder ≥27 kg/m² (Übergewicht) mit mindestens einer gewichtsbedingten Begleiterkrankung (z. B. Hypertonie, Dyslipidämie, Typ-2-Diabetes, obstruktives Schlafapnoesyndrom).
- Bei Jugendlichen (12–17 Jahre) mit Adipositas entsprechend alters- und geschlechtsbezogener Referenzdaten.
Anwendungsart
Liraglutid wird einmal täglich subkutan injiziert – unabhängig von Mahlzeiten – vorzugsweise in Bauch, Oberschenkel oder Oberarm. Eine Injektion zur gleichen Tageszeit wird empfohlen.
Wirkmechanismus
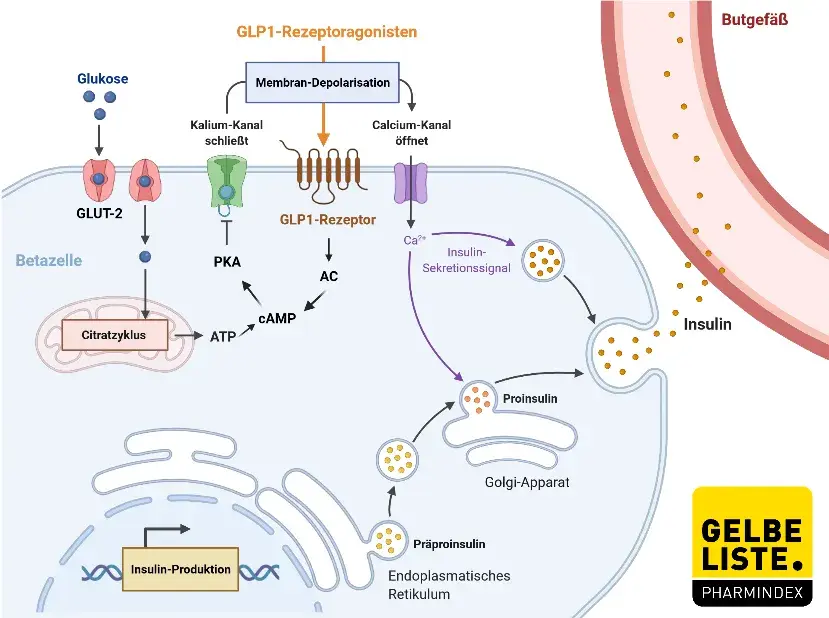
Liraglutid ist ein langwirksames Analogon des humanen Glucagon-like Peptide-1 (GLP-1), das eine 97%ige Aminosäuresequenzhomologie zu endogenem GLP-1 aufweist. Es bindet spezifisch an den GLP-1-Rezeptor, einen membrangebundenen G-Protein-gekoppelten Rezeptor, der unter anderem in Pankreas, ZNS und gastrointestinalem Trakt exprimiert wird. Die Aktivierung dieses Rezeptors führt zu einer glukoseabhängigen Stimulation der Insulinsekretion aus den Betazellen des Pankreas sowie zu einer Hemmung der Glukagonsekretion aus den Alphazellen. Darüber hinaus verzögert Liraglutid die Magenentleerung und führt zu einer Reduktion des Appetits durch zentrale Wirkmechanismen im Hypothalamus. Diese Effekte führen zu einer verbesserten Blutzuckerkontrolle und – bei adipösen Patienten – zu einer klinisch relevanten Gewichtsreduktion. Das Hypoglykämierisiko ist bei Monotherapie gering, da die Insulinfreisetzung glukoseabhängig erfolgt.
Pharmakokinetik
Resorption
- Resorption erfolgt langsam nach subkutaner Injektion
- Maximale Plasmakonzentration nach 8–12 Stunden
Verteilung
- Verteilungsvolumen ca. 11–17 l
- Plasmaproteinbindung >98 %
Metabolisierung
- Liraglutid wird wie endogenes GLP-1 enzymatisch abgebaut
- Es entstehen keine aktiven Metaboliten
Elimination
- Plasmahalbwertszeit: ca. 13 Stunden
- Elimination erfolgt über Metabolismus, nicht renal
Besondere Hinweise
- Keine Dosisanpassung bei älteren Patienten erforderlich
- Bei mäßiger Nieren- oder Leberfunktionsstörung ist keine Dosisanpassung notwendig; bei schwerer Einschränkung Vorsicht geboten
- Nicht empfohlen bei Kindern unter 10 Jahren (Diabetes) bzw. unter 12 Jahren (Adipositas)
Dosierung
Die Dosierung von Liraglutid richtet sich nach der Indikation:
Typ-2-Diabetes
• Initial 0,6 mg/Tag
• Steigerung auf 1,2 mg/Tag nach mindestens einer Woche
• Bei Bedarf Erhöhung auf 1,8 mg/Tag zur besseren Blutzuckerkontrolle
• Maximaldosis: 1,8 mg/Tag
Adipositas
• Initial 0,6 mg/Tag, wöchentliche Steigerung in 0,6-mg-Schritten
• Ziel: 3,0 mg/Tag ab Woche 5
• Behandlung abbrechen, wenn nach 12 Wochen unter 3,0 mg keine Gewichtsreduktion von ≥5 % erreicht wurde
Nebenwirkungen
Häufige Nebenwirkungen (≥1/10) sind:
- Gastrointestinal: Übelkeit, Erbrechen, Diarrhö, Obstipation
- Zentralnervös: Kopfschmerzen, Müdigkeit
- Stoffwechsel: Hypoglykämie (v. a. bei Kombination mit Insulin/SU), Appetitverlust
- Reaktionen an der Injektionsstelle
- Erhöhte Pankreasenzyme
- Gallenerkrankungen
Wechselwirkungen
Folgende Wechselwirkungen sind bei der Anwendung von Liraglutid zu beachten:
- Verzögerte Magenentleerung: Kann die Resorption gleichzeitig verabreichter Arzneimittel (z. B. Paracetamol, orale Kontrazeptiva) beeinflussen
- Insulin / Sulfonylharnstoffe: Risiko für Hypoglykämien erhöht – ggf. Dosisanpassung notwendig
- Nicht empfohlen mit anderen GLP-1-Analoga
Kontraindikationen
Liraglutid darf nicht angewendet werden bei Überempfindlichkeit gegen Liraglutid oder einen der sonstigen Bestandteile.
Schwangerschaft
Liraglutid soll während der Schwangerschaft nicht angewendet werden. Tierexperimentelle Studien zeigten Reproduktionstoxizität. Patientinnen mit Kinderwunsch sollten auf eine geeignete Alternative umgestellt werden.
Stillzeit
Es ist nicht bekannt, ob Liraglutid in die Muttermilch übergeht. Aufgrund mangelnder Erfahrung soll der Wirkstoff in der Stillzeit nicht angewendet werden.
Verkehrstüchtigkeit
Liraglutid beeinflusst die Verkehrstüchtigkeit nicht direkt. Bei gleichzeitiger Anwendung mit blutzuckersenkenden Medikamenten (z. B. Insulin) ist das Risiko für Hypoglykämien zu berücksichtigen.
Anwendungshinweise
Folgende Warnhinweise und Vorsichtsmaßnahmen sind bei der Anwendung von Liraglutid zu beachten:
- Aspirationsrisiko bei Narkose: Bei GLP-1-Rezeptoragonisten wurde über Aspirationspneumonien im Zusammenhang mit Vollnarkose oder tiefer Sedierung berichtet. Aufgrund verzögerter Magenentleerung ist das Risiko von Restmageninhalt zu berücksichtigen.
- Cholelithiasis und Cholezystitis: Unter Liraglutid kann das Risiko für Gallensteine und Gallenblasenentzündung erhöht sein. Eine stationäre Behandlung oder Cholezystektomie kann erforderlich werden. Patienten sind über typische Symptome aufzuklären.
- Rückverfolgbarkeit: Die Bezeichnung und Chargennummer des Arzneimittels sollten zur lückenlosen Rückverfolgbarkeit dokumentiert werden.
- Herzinsuffizienz: Bei NYHA-Stadium IV liegen keine klinischen Daten vor. Liraglutid wird bei diesen Patienten nicht empfohlen.
- Besondere Patientengruppen: Die Anwendung wird nicht empfohlen bei Patienten ≥75 Jahren, mit schwerer Leber- oder Nierenfunktionsstörung, mit endokrinen Ursachen der Adipositas, Essstörungen oder gleichzeitiger Behandlung mit anderen Gewichtsreduktionspräparaten.
- Entzündliche Darmerkrankungen und Gastroparese: Die Anwendung wird bei diesen Patienten nicht empfohlen, da gastrointestinale Nebenwirkungen verstärkt auftreten können.
- Pankreatitis: Bei Verdacht auf akute Pankreatitis ist Liraglutid sofort abzusetzen. Eine Wiederaufnahme der Therapie nach bestätigter Pankreatitis ist kontraindiziert.
- Schilddrüsenerkrankungen: Schilddrüsenbedingte unerwünschte Ereignisse (z. B. Struma) wurden insbesondere bei Patienten mit Vorerkrankung beobachtet. Vorsicht ist geboten.
- Herzfrequenz: Eine klinisch relevante Erhöhung der Herzfrequenz wurde beobachtet. Bei Symptomen wie Palpitationen ist regelmäßige Kontrolle empfohlen; bei anhaltender Erhöhung sollte Liraglutid abgesetzt werden.
- Dehydrierung: Gastrointestinale Nebenwirkungen können zur Dehydrierung führen. Patienten sind über eine ausreichende Flüssigkeitszufuhr zu informieren.
- Hypoglykämie bei Typ-2-Diabetes: Bei gleichzeitiger Gabe von Insulin oder Sulfonylharnstoffen besteht ein erhöhtes Hypoglykämierisiko. Dosisanpassung dieser Medikamente kann erforderlich sein.
- Kinder und Jugendliche: In der pädiatrischen Anwendung wurden klinisch signifikante Hypoglykämien beobachtet. Eine entsprechende Aufklärung ist erforderlich.
- Hyperglykämie bei insulinpflichtigem Diabetes: Saxenda® darf nicht als Insulinersatz verwendet werden. Ein abruptes Absetzen von Insulin kann zur diabetischen Ketoazidose führen.
Alternativen
Als mögliche Alternativen zu Liraglutid kommen folgende Wirkstoffe infrage:
Für Typ-2-Diabetes:
- GLP-1-Rezeptoragonisten: Semaglutid, Dulaglutid, Exenatid
- SGLT2-Inhibitoren: Empagliflozin, Dapagliflozin
- DPP-4-Inhibitoren: Sitagliptin, Linagliptin
- Basalinsuline: Insulin glargin, Insulin degludec
Für Adipositas:
- GLP-1-Analoga: Semaglutid (2,4 mg s.c./Woche)
- Zentrale Wirkstoffe: Naltrexon/Bupropion
- Lipasehemmer: Orlistat
- Chirurgische Maßnahmen: Bariatrische Verfahren bei therapierefraktärer Adipositas
Wirkstoff-Informationen
- Fachinformation Victoza® 6 mg/ml Injektionslösung, Stand Januar 2023
- Fachinformation Saxenda® 6 mg/ml Injektionslösung, Stand August 2023
-
DIAVIC 6 mg/ml Injektionslösung in einem Fertigpen
Basics GmbH
-
Ladiazyl 6 mg/ml Injektionslösung im Fertigpen
Biocon Biologics Germany GmbH
-
Liraglutid Cipla 6 mg/ml Injektionslösung im Fertigpen
Cipla Europe NV
-
Lobezyl 6 mg/ml Injektionslösung im Fertigpen
Biocon Biologics Germany GmbH
-
Nevolat 6 mg/ml Injektionslösung im Fertigpen
Zentiva Pharma GmbH
-
Saxenda 6 mg/ml 2care4 Injektionslösung im Fertigpen
2care4 ApS
-
Saxenda 6 mg/ml 101 Carefarm Injektionslösung im Fertigpen
1 0 1 Carefarm GmbH
-
Saxenda 6 mg/ml axicorp Injektionslösung im Fertigpen
axicorp Pharma B.V.
-
Saxenda 6 mg/ml CC Pharma Injektionslösung in einem Fertigpen
CC Pharma GmbH
-
Saxenda 6 mg/ml Eurim Injektionslösung in einem Fertigpen
Eurim-Pharm Arzneimittel GmbH
-
Saxenda® 6 mg/ml Injektionslösung im Fertigpen
Novo Nordisk Pharma GmbH
-
Saxenda 6 mg/ml kohlpharma Injektionslösung in einem Fertigpen
kohlpharma GmbH
-
Saxenda 6 mg/ml Orifarm Injektionslösung im Fertigpen
Orifarm GmbH
-
Saxenda 6 mg/ml Paranova Injektionslösung in einem Fertigpen
Paranova Pack A/S
-
Saxenda 6 mg/ml PB Pharma Injektionslösung in einem Fertigpen
PB Pharma GmbH
-
Victoza 6 mg/ml 1 4U Pharma Injektionslösung in einem Fertigpen
1 4 U Pharma GmbH
-
Victoza 6 mg/ml Abacus Injektionslösung in einem Fertigpen
Abacus Medicine A/S
-
Victoza 6 mg/ml axicorp Injektionslösung in einem Fertigpen
axicorp Pharma B.V.
-
Victoza 6 mg/ml Emra Injektionslösung in einem Fertigpen
Emra-Med Arzneimittel GmbH
-
Victoza 6 mg/ml Eurim Injektionslösung in einem Fertigpen
Eurim-Pharm Arzneimittel GmbH
-
Victoza® 6 mg/ml Injektionslösung in einem Fertigpen
Novo Nordisk Pharma GmbH
-
Victoza 6 mg/ml kohlpharma Injektionslösung in einem Fertigpen
kohlpharma GmbH
-
Victoza 6 mg/ml Orifarm Injektionslösung in einem Fertigpen
Orifarm GmbH
-
Victoza 6 mg/ml Originalis Injektionslösung in einem Fertigpen
Originalis B.V.
-
Victoza 6 mg/ml PB Pharma Injektionslösung in einem Fertigpen
PB Pharma GmbH














