Mepolizumab
Mepolizumab ist ein humanisierter monoklonaler Antikörper, der mit hoher Affinität und Spezifität an humanes Interleukin 5 (IL-5) bindet.
Mepolizumab: Übersicht
Anwendung
Mepolizumab (Nucala) ist ein monoklonaler Antikörper, der zur Behandlung folgender Ergrankungen indiziert ist:
- Schweres eosinophiles Asthma: als Zusatzbehandlung bei schwerem refraktärem eosinophilem Asthma bei Erwachsenen, Jugendlichen und Kindern ab 6 Jahren
- Chronische Rhinosinusitis mit Nasenpolypen (Chronic rhinosinusitis with nasal polyps, CRSwNP): als Zusatztherapie mit intranasalen Kortikosteroiden zur Behandlung von erwachsenen Patienten mit schwerer CRSwNP, die mit systemischen Kortikosteroiden und/oder chirurgischem Eingriff nicht ausreichend kontrolliert werden kann.
- Eosinophile Granulomatose mit Polyangiitis (EGPA): als Zusatzbehandlung für Patienten ab 6 Jahren mit schubförmig remittierender oder refraktärer eosinophiler Granulomatose mit Polyangiitis (EGPA).
- Hypereosinophiles Syndrom (HES): als Zusatzbehandlung bei erwachsenen Patienten mit unzureichend kontrolliertem hypereosinophilem Syndrom ohne erkennbare, nicht-hämatologische sekundäre Ursache.
Wirkmechanismus
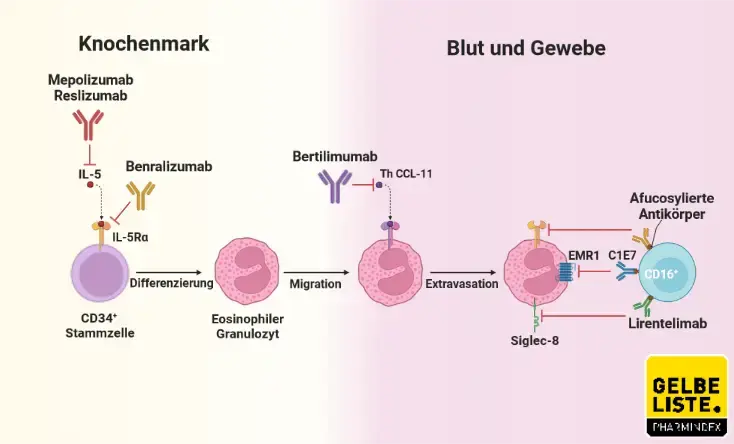
Mepolizumab bindet spezifisch an das Zytokin Interleukin-5 (IL-5) und neutralisiert dieses. Infolgedessen wird die Interaktion zwischen IL-5 und dem IL-5-Rezeptor (IL-5Rα) unterbunden, die für die Differenzierung, Reifung, Rekrutierung und Aktivierung von humanen Eosinophilen elementar ist. Dadurch wird die Überlebensrate und Aktivität von Eosinophilen reduziert.
In der Pathogenese von eosinophilem Asthma spielen Th2-Zellen eine Schlüsselrolle. Diese differenzieren sich aus naiven T-Helferzellen unter IL-4-Einfluss und produzieren neben IL-5 unter anderem auch die Zytokine IL-4 und IL-13.
Während die Zytokine IL-4 und IL-13 in B-Zellen die Bildung von IgE-Antikörpern stimulieren, vermittelt IL-5 die Differenzierung, Reifung, Rekrutierung und Aktivierung von humanen Eosinophilen. Aus diesem Grund stellt die IL-5/IL-5R-Interaktion ein vielversprechendes Target bei eosinophilem Asthma dar.
Dosierung
Bei der Behandlung von schwerem eosinophilem Asthma beträgt die empfohlene Dosis für Erwachsene und Jugendliche ab 12 Jahren 100 mg Mepolizumab, subkutan verabreicht einmal alle 4 Wochen. Kinder im Alter von 6 bis 11 Jahren erhalten 40 mg, subkutan verabreicht einmal alle 4 Wochen.
Bei der Behandlung chronischer Rhinosinusitis mit Nasenpolypen beträgt die empfohlene Dosis für Erwachsene 100 mg Mepolizumab, subkutan verabreicht einmal alle 4 Wochen.
Bei der Behandlung der Eosinophilen Granulomatose mit Polyangiitis beträgt die empfohlene Dosis für Erwachsene und Jugendliche ab 12 Jahren 300 mg Mepolizumab, subkutan verabreicht einmal alle 4 Wochen. Kinder im Alter von 6 bis 11 Jahren mit einem Gewicht von ≥ 40 kg erhalten 200 mg, subkutan verabreicht einmal alle 4 Wochen. Kinder im Alter von 6 bis 11 Jahren mit einem Gewicht von < 40 kg erhalten 100 mg, subkutan verabreicht einmal alle 4 Wochen.
Bei der Behandlung des Hypereosinophilen Syndroms beträgt die empfohlene Dosis für Erwachsene 300 mg Mepolizumab, subkutan verabreicht einmal alle 4 Wochen.
Nebenwirkungen
Trotz eines guten Sicherheitsprofils kann es bei der Anwendung von Mepolizumab aufgrund seiner Wirkung auf das Immunsystem zu vermehrten Infektionen, wie z. B. Herpes-Zoster kommen. Die häufigsten während der Behandlung berichteten Nebenwirkungen sind;
- Kopfschmerzen
- Reaktionen an der Injektionsstelle
- Rückenschmerzen
Kontraindikationen
Mepolizumab darf nicht bei Überempfindlichkeit gegen den Wirkstoff angewendet werden.
Alternativen
Ein weiterer Anti-IL-5-Antikörper ist Reslizumab. Darüber hinaus befindet sich der Anti-IL-5Rα-Antikörper Benralizumab auf dem Markt.
- EMA: Fachinformation Nucala
- Freissmuth et al., Pharmakologie und Toxikologie, 2020, Springer
- Mutschler et al., Mutschler Arzneimittelwirkungen, 2019, Wissenschaftliche Verlagsgesellschaft Stuttgart
- NVL Asthma (4. Auflage)
Abbildung
Adapted from „Antibody Targeting in Eosinophil-Associated Diseases”, by BioRender.com
-
Nucala 40 mg Injektionslösung in einer Fertigspritze
GlaxoSmithKline GmbH & Co. KG
-
Nucala 100 mg Abacus Injektionslösung im Fertigpen
Abacus Medicine A/S
-
Nucala 100 mg Abacus Injektionslösung in einer Fertigspritze
Abacus Medicine A/S
-
Nucala 100 mg Abacus Pulver zur Herstellung einer Injektionslösung
Abacus Medicine A/S
-
Nucala 100 mg ACA Injektionslösung im Fertigpen
A.C.A. Müller ADAG Pharma AG
-
Nucala 100 mg axicorp Injektionslösung im Fertigpen
axicorp Pharma B.V.
-
Nucala 100 mg axicorp Injektionslösung in einer Fertigspritze
axicorp Pharma B.V.
-
Nucala 100 mg axicorp Pulver zur Herstellung einer Injektionslösung
axicorp Pharma B.V.
-
Nucala 100 mg CC-Pharma Injektionslösung im Fertigpen
CC Pharma GmbH
-
Nucala 100 mg CC Pharma Injektionslösung in einer Fertigspritze
CC Pharma GmbH
-
Nucala 100 mg CC Pharma Pulver zur Herstellung einer Injektionslösung
CC Pharma GmbH
-
Nucala 100 mg Eurim Injektionslösung im Fertigpen
Eurim-Pharm Arzneimittel GmbH
-
Nucala 100 mg Eurim Injektionslösung in einer Fertigspritze
Eurim-Pharm Arzneimittel GmbH
-
Nucala 100 mg Eurim Pulver zur Herstellung einer Injektionslösung
Eurim-Pharm Arzneimittel GmbH
-
Nucala 100 mg Injektionslösung im Fertigpen
GlaxoSmithKline GmbH & Co. KG
-
Nucala 100 mg Injektionslösung in einer Fertigspritze
GlaxoSmithKline GmbH & Co. KG
-
Nucala 100 mg kohlpharma Injektionslösung im Fertigpen
kohlpharma GmbH
-
Nucala 100 mg kohlpharma Injektionslösung in einer Fertigspritze
kohlpharma GmbH
-
Nucala 100 mg kohlpharma Pulver zur Herstellung einer Injektionslösung
kohlpharma GmbH
-
Nucala 100 mg Medicopharm Injektionslösung in einer Fertigspritze
Medicopharm AG
-
Nucala 100 mg Orifarm Injektionslösung im Fertigpen
Orifarm GmbH
-
Nucala 100 mg Orifarm Injektionslösung in einer Fertigspritze
Orifarm GmbH
-
Nucala 100 mg Orifarm Pulver zur Herstellung einer Injektionslösung
Orifarm GmbH
-
Nucala 100 mg Paranova Injektionslösung im Fertigpen
Paranova Pack A/S
-
Nucala 100 mg Paranova Injektionslösung in einer Fertigspritze
Paranova Pack A/S
-
Nucala 100 mg Paranova Pulver zur Herstellung einer Injektionslösung
Paranova Pack A/S
-
Nucala 100 mg Pulver zur Herstellung einer Injektionslösung
GlaxoSmithKline GmbH & Co. KG














