Pembrolizumab
Pembrolizumab ist ein monoklonaler Antikörper und gehört zur Wirkstoffgruppe der PD-1-Inhibitoren. Es wird zur Behandlung einer Vielzahl von Krebserkrankungen eingesetzt, darunter fortgeschrittenes Melanom, nicht-kleinzelliges Bronchialkarzinom, Hodgkin-Lymphom, Urothelkarzinom sowie Tumoren im Kopf- und Halsbereich.
Pembrolizumab: Übersicht
Anwendung
Der Checkpoint-Inhibitor Pembrolizumab besitzt folgende Anwendungsgebiete:
Melanom
- Monotherapie: Behandlung des fortgeschrittenen (nicht resezierbaren oder metastasierenden) Melanoms bei Kindern und Jugendlichen ab 12 Jahren und Erwachsenen.
- Adjuvante Therapie: Behandlung des Melanoms in den Tumorstadien IIB, IIC oder III nach vollständiger Resektion bei Kindern und Jugendlichen ab 12 Jahren und Erwachsenen.
Nicht-kleinzelliges Lungenkarzinom (NSCLC)
- Neoadjuvante und adjuvante Therapie: Kombination mit Platin-basierter Chemotherapie für resezierbares NSCLC mit hohem Rezidivrisiko bei Erwachsenen.
- Adjuvante Therapie: Monotherapie nach vollständiger Resektion und Platin-basierter Chemotherapie für NSCLC mit hohem Rezidivrisiko bei Erwachsenen.
- Erstlinienbehandlung: Monotherapie für metastasierendes NSCLC mit PD-L1-exprimierenden Tumoren (TPS ≥ 50%) ohne EGFR- oder ALK-positive Tumormutationen bei Erwachsenen.
- Erstlinienbehandlung: Kombination mit Pemetrexed und Platin-Chemotherapie für metastasierendes nicht-plattenepitheliales NSCLC ohne EGFR- oder ALK-positive Tumormutationen bei Erwachsenen.
- Erstlinienbehandlung: Kombination mit Carboplatin und entweder Paclitaxel oder nab-Paclitaxel für metastasierendes plattenepitheliales NSCLC bei Erwachsenen.
- Zweitlinienbehandlung: Monotherapie für lokal fortgeschrittenes oder metastasierendes NSCLC mit PD-L1-exprimierenden Tumoren (TPS ≥ 1%) nach vorheriger Chemotherapie bei Erwachsenen. Patienten mit EGFR- oder ALK-positiven Tumormutationen sollten vorher eine gezielte Therapie erhalten haben.
Klassisches Hodgkin-Lymphom (HL)
- Monotherapie: Behandlung des rezidivierenden oder refraktären klassischen Hodgkin-Lymphoms bei Kindern und Jugendlichen ab 3 Jahren und Erwachsenen nach Versagen einer autologen Stammzelltransplantation oder nach mindestens zwei vorangegangenen Therapien, wenn eine autologe Stammzelltransplantation nicht in Frage kommt.
Urothelkarzinom
- Monotherapie: Behandlung des lokal fortgeschrittenen oder metastasierenden Urothelkarzinoms nach vorheriger Platin-basierter Therapie bei Erwachsenen.
- Monotherapie: Behandlung des lokal fortgeschrittenen oder metastasierenden Urothelkarzinoms bei Erwachsenen, die nicht für eine Cisplatin-basierte Therapie geeignet sind und deren Tumoren PD-L1 mit einem kombinierten positiven Score (CPS) ≥ 10 exprimieren.
Plattenepithelkarzinom der Kopf-Hals-Region (HNSCC)
- Erstlinienbehandlung: Monotherapie oder Kombination mit Platin- und 5-Fluorouracil (5-FU)-Chemotherapie für metastasierendes oder nicht resezierbares rezidivierendes HNSCC bei Erwachsenen mit PD-L1-exprimierenden Tumoren (CPS ≥ 1).
- Zweitlinienbehandlung: Monotherapie für rezidivierendes oder metastasierendes HNSCC mit PD-L1-exprimierenden Tumoren (TPS ≥ 50%) und Fortschreiten während oder nach vorheriger Platin-basierter Therapie bei Erwachsenen.
Nierenzellkarzinom (RCC)
- Erstlinienbehandlung: Kombination mit Axitinib für fortgeschrittenes Nierenzellkarzinom bei Erwachsenen.
- Erstlinienbehandlung: Kombination mit Lenvatinib für fortgeschrittenes Nierenzellkarzinom bei Erwachsenen.
- Adjuvante Therapie: Monotherapie für Nierenzellkarzinom mit erhöhtem Rezidivrisiko nach Nephrektomie oder nach Nephrektomie und Resektion metastasierter Läsionen bei Erwachsenen.
Tumoren mit hochfrequenter Mikrosatelliteninstabilität (MSI-H) oder Mismatch-Reparatur-Defizienz (dMMR)
Kolorektalkarzinom (CRC)
- Erstlinienbehandlung: Monotherapie für metastasierendes Kolorektalkarzinom.
- Zweitlinienbehandlung: Behandlung des nicht resezierbaren oder metastasierenden Kolorektalkarzinoms nach vorheriger Fluoropyrimidin-basierter Kombinationstherapie.
Nicht-kolorektale Karzinome
- Endometriumkarzinom: Fortgeschrittenes oder rezidivierendes Endometriumkarzinom nach Platin-basierter Therapie, wenn eine kurative Behandlung nicht möglich ist.
- Magen-, Dünndarm- oder biliäres Karzinom: Behandlung nach mindestens einer vorherigen Therapie bei nicht resezierbarem oder metastasierendem Karzinom.
Ösophaguskarzinom
- Erstlinienbehandlung: Kombination mit Platin- und Fluoropyrimidin-basierter Chemotherapie für lokal fortgeschrittenes nicht resezierbares oder metastasierendes Ösophaguskarzinom bei Erwachsenen mit PD-L1-exprimierenden Tumoren (CPS ≥ 10).
Triple-negatives Mammakarzinom (TNBC)
- Neoadjuvante und adjuvante Therapie: Kombination mit Chemotherapie für lokal fortgeschrittenes oder frühes triple-negatives Mammakarzinom mit hohem Rezidivrisiko bei Erwachsenen.
- Zweitlinienbehandlung: Kombination mit Chemotherapie für lokal rezidivierendes nicht resezierbares oder metastasierendes triple-negatives Mammakarzinom mit PD-L1-exprimierenden Tumoren (CPS ≥ 10) bei Erwachsenen, die keine vorherige Chemotherapie für die metastasierte Erkrankung erhalten haben.
Endometriumkarzinom (EC)
- Zweitlinienbehandlung: Kombination mit Lenvatinib für fortgeschrittenes oder rezidivierendes Endometriumkarzinom nach Platin-basierter Therapie, wenn eine kurative Behandlung nicht möglich ist.
Zervixkarzinom
- Zweitlinienbehandlung: Kombination mit Chemotherapie mit oder ohne Bevacizumab für persistierendes, rezidivierendes oder metastasierendes Zervixkarzinom mit PD-L1-exprimierenden Tumoren (CPS ≥ 1).
Adenokarzinom des Magens oder des gastroösophagealen Übergangs (GEJ)
- Erstlinienbehandlung: Kombination mit Trastuzumab sowie Fluoropyrimidin- und Platin-basierter Chemotherapie für lokal fortgeschrittenes nicht resezierbares oder metastasierendes HER2-positives Adenokarzinom des Magens oder des gastroösophagealen Übergangs bei Erwachsenen mit PD-L1-exprimierenden Tumoren (CPS ≥ 1).
- Erstlinienbehandlung: Kombination mit Fluoropyrimidin- und Platin-basierter Chemotherapie für lokal fortgeschrittenes nicht resezierbares oder metastasierendes HER2-negatives Adenokarzinom des Magens oder des gastroösophagealen Übergangs bei Erwachsenen mit PD-L1-exprimierenden Tumoren (CPS ≥ 1).
Biliäres Karzinom (BTC)
- Erstlinienbehandlung: Kombination mit Gemcitabin und Cisplatin für lokal fortgeschrittenes nicht resezierbares oder metastasierendes biliäres Karzinom bei Erwachsenen.
Anwendungsart
Pembrolizumab ist zur intravenösen Anwendung bestimmt und muss als Infusion über 30 Minuten gegeben werden.
Wirkmechanismus
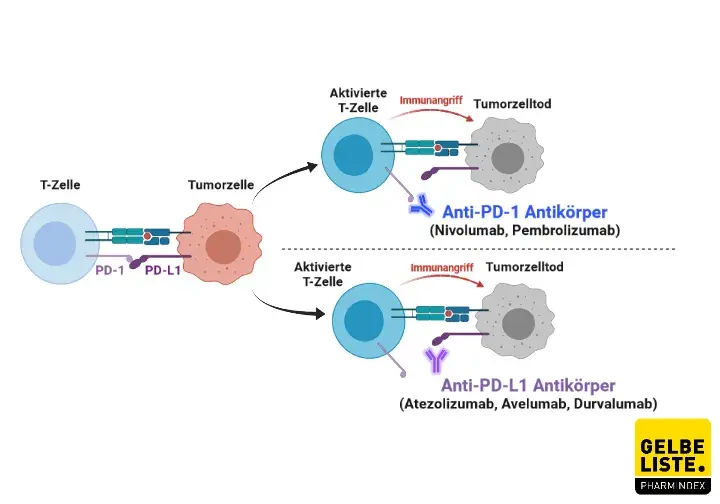
Pembrolizumab ist ein humanisierter monoklonaler Antikörper, der an den PD-1 (Programmed cell death) Rezeptor bindet und damit die Interaktion mit seinen Liganden PD-L1 (programmed cell death ligand) und PD-L2 verhindert.
Der PD-1-Rezeptor ist ein negativer Regulator der T-Zell-Aktivität, der an der Kontrolle der T-Zell-Immunreaktion beteiligt ist. Der Rezeptor wird hauptsächlich auf der Oberfläche aktivierter T-Zellen exprimiert . Binden an ihn die Liganden PD-L1 und PD-L2, wird die zytotoxische T-Zell-Immunantwort gehemmt und so überschießende Immunreaktionen verhindert. Diesen negativen Rückkopplungsmechanismus missbrauchen allerdings Tumorzellen, indem sie ebenfalls die beiden Liganden exprimieren. In der Folge wird das Immunsystem ausgebremst und daran gehindert, die Krebszellen zu attackieren.
Durch die Hemmung der Bindung des PD-1-Rezeptors an seine Liganden PD-L1 und PD-L2 verstärkt Pembrolizumab so die T-Zell-Reaktion einschließlich der Immunreaktion gegen den Tumor.
Pembrolizumab wird auch als Checkpoint-Inhibitor bezeichnet, da das Immuntherapeutikum das körpereigene Immunsystem wieder in die Lage versetzt, selbst verstärkt gegen den Krebs zu kämpfen, indem es wichtige Schaltstellen, sogenannte Checkpoints, blockiert.
Pharmakokinetik
- Resorption: Pembrolizumab wird intravenös gegeben und ist daher sofort und vollständig bioverfügbar.
- Verteilung: Das Verteilungsvolumen im Steady State ist gering (~6,0 l; CV: 20%). Pembrolizumab bindet nicht spezifisch an Plasmaproteine.
- Biotransformation: Pembrolizumab wird über unspezifische Stoffwechselwege abgebaut; der Metabolismus trägt nicht zur Ausscheidung bei.
- Elimination: Nach Erreichen des Steady State ist die Ausscheidung um etwa 23% geringer als bei der Initialdosis. Die terminale Halbwertszeit beträgt 22 Tage (32%).
- Linearität/Nicht-Linearität: Die Exposition von Pembrolizumab nimmt dosisproportional zu. Steady-State-Konzentrationen werden nach 16 Wochen erreicht, mit einer systemischen Akkumulation um das 2,1-Fache.
Besondere Patientengruppen:
- Einschränkung der Nierenfunktion: Keine klinisch bedeutsamen Unterschiede in der Ausscheidung bei Patienten mit leichter oder moderater Nierenfunktionsstörung im Vergleich zu Patienten mit normaler Nierenfunktion.
- Einschränkung der Leberfunktion: Keine klinisch bedeutsamen Unterschiede in der Ausscheidung bei Patienten mit leichter oder moderater Leberfunktionsstörung im Vergleich zu Patienten mit normaler Leberfunktion.
- Patienten mit klassischem HL: Bei Gabe von 200 mg Pembrolizumab alle 3 Wochen wurden bis zu 40% höhere mediane Steady-State-Talspiegel beobachtet als bei anderen Tumorarten.
Dosierung
- Erwachsene: Empfohlene Dosis: 200 mg alle 3 Wochen oder 400 mg alle 6 Wochen als intravenöse Gabe über 30 Minuten.
- Kinder und Jugendliche: Monotherapie bei klassischem HL (ab 3 Jahren) oder Melanom (ab 12 Jahren): 2 mg/kg Körpergewicht (bis zu einem Maximum von 200 mg) alle 3 Wochen als intravenöse Gabe über 30 Minuten.
- Kombinationstherapie: Fachinformationen der begleitenden Therapeutika beachten.
Behandlungsdauer
- Allgemein: Bis Fortschreiten der Krebserkrankung oder unzumutbare Toxizität.
- Adjuvante Behandlung (Melanom, NSCLC, RCC): Bis Rezidiv, unzumutbare Toxizität oder bis zu einem Jahr.
- Neoadjuvante Behandlung (resezierbares NSCLC): 4 Dosen von 200 mg alle 3 Wochen oder 2 Dosen von 400 mg alle 6 Wochen.
- Adjuvante Behandlung (resezierbares NSCLC): 13 Dosen von 200 mg alle 3 Wochen oder 7 Dosen von 400 mg alle 6 Wochen.
- Neoadjuvante Behandlung (TNBC): 8 Dosen von 200 mg alle 3 Wochen oder 4 Dosen von 400 mg alle 6 Wochen.
- Adjuvante Behandlung (TNBC): 9 Dosen von 200 mg alle 3 Wochen oder 5 Dosen von 400 mg alle 6 Wochen.
Nebenwirkungen
Häufigste Nebenwirkungen unter Monotherapie
- Ermüdung/Fatigue
- Diarrhö
- Übelkeit
Schwere Nebenwirkungen
- Immunvermittelte Nebenwirkungen und schwere infusionsbedingte Reaktionen: Besonders relevant in adjuvanten und metastasierten Settings.
Häufigste Nebenwirkungen in Kombination mit Chemotherapie
- Anämie
- Übelkeit
- Ermüdung/Fatigue
- Diarrhö
- Obstipation
- Erbrechen
- Verminderter Appetit
- Neutropenie
Häufigste Nebenwirkungen in Kombination mit Tyrosinkinase-Inhibitoren (TKI)
- Diarrhö
- Hypertonie
- Hypothyreose
- Ermüdung/Fatigue
- Verminderter Appetit
- Übelkeit
- Arthralgie
Schweregrad 3-5 Nebenwirkungen bei spezifischen Patientengruppen
- NSCLC: unter Kombinationstherapie, unter Chemotherapie
- HNSCC: unter Kombinationstherapie, unter Chemotherapie
- Ösophaguskarzinom: unter Kombinationstherapie, unter Chemotherapie
- TNBC: unter Kombinationstherapie, unter Chemotherapie
- Zervixkarzinom: unter Kombinationstherapie, unter Chemotherapie
- Magenkarzinom: unter Kombinationstherapie, unter Chemotherapie
- Biliäres Karzinom: unter Kombinationstherapie, unter Chemotherapie
Immunvermittelte Nebenwirkungen
- Pneumonitis
- Kolitis
- Hepatitis: Überwachen und ggf. Kortikosteroide
- Nephritis: Überwachen und ggf. Kortikosteroide
- Endokrinopathien: Überwachen und Hormonsubstitution
Hautreaktionen
- Schwere Hautreaktionen einschließlich Stevens-Johnson-Syndrom (SJS) und toxische epidermale Nekrolyse (TEN)
Systemische Nebenwirkungen
- Fieber, Ödeme, grippeähnliche Symptome
Wechselwirkungen
Es wurden keine formalen pharmakokinetischen Wechselwirkungsstudien mit Pembrolizumab durchgeführt. Da Pembrolizumab durch katabolischen Abbau aus dem Blutkreislauf eliminiert wird, sind keine Wechselwirkungen mit anderen Arzneimitteln zu erwarten.
Die systemische Anwendung von Kortikosteroiden oder Immunsuppressiva vor Beginn der Therapie mit Pembrolizumab sollte vermieden werden, da sie die pharmakodynamische Aktivität und Wirksamkeit von Pembrolizumab beeinträchtigen können.
Nach Beginn der Therapie mit Pembrolizumab können systemische Kortikosteroide oder andere Immunsuppressiva jedoch zur Behandlung von immunvermittelten Nebenwirkungen eingesetzt werden. Zudem können Kortikosteroide als Prämedikation zur Vorbeugung von Übelkeit und Erbrechen sowie zur Linderung von chemotherapiebedingten Nebenwirkungen verwendet werden, wenn Pembrolizumab in Kombination mit Chemotherapie angewendet wird.
Kontraindikationen
Pembrolizumab darf nicht angewendet werden bei Überempfindlichkeit gegen den Wirkstoff.
Schwangerschaft
Daten zur Anwendung von Pembrolizumab bei Schwangeren liegen nicht vor. Modelle mit trächtigen Mäusen zeigten, dass die Blockierung des PD-L1-Signalwegs die feto-maternale Toleranz stört und zu einer Erhöhung der Abortrate führt. Diese Ergebnisse deuten auf ein potenzielles Risiko hin, dass die Gabe von Pembrolizumab während der Schwangerschaft, basierend auf dem Wirkmechanismus, eine fötale Beeinträchtigung, einschließlich erhöhter Abort- und Totgeburtsraten, verursachen kann. Es ist bekannt, dass humane Immunglobuline vom G4-Typ (IgG4) plazentagängig sind. Daher besteht die Möglichkeit, dass Pembrolizumab, als IgG4-Antikörper, von der Mutter auf den sich entwickelnden Fötus übertragen werden kann. Pembrolizumab sollte während der Schwangerschaft nicht angewendet werden, es sei denn, der klinische Zustand der Frau erfordert eine Behandlung mit Pembrolizumab.
Stillzeit
Es ist nicht bekannt, ob Pembrolizumab in die Muttermilch übergeht. Da Antikörper bekanntlich in die Muttermilch übergehen können, kann ein Risiko für das Neugeborene bzw. den Säugling nicht ausgeschlossen werden. Eine Entscheidung muss darüber getroffen werden, ob das Stillen zu unterbrechen ist, oder ob auf die Behandlung mit Pembrolizumab verzichtet werden soll/die Behandlung mit Pembrolizumab zu unterbrechen ist. Dabei ist sowohl der Nutzen des Stillens für das Kind als auch der Nutzen der Therapie mit Pembrolizumab für die stillende Patientin zu berücksichtigen.
Verkehrstüchtigkeit
Pembrolizumab hat einen geringen Einfluss auf die Verkehrstüchtigkeit und die Fähigkeit zum Bedienen von Maschinen, da bei einigen Patienten nach Gabe von Pembrolizumab über Schwindel und Müdigkeit/Erschöpfung berichtet wurde.
Anwendungshinweise
Folgende Warnhinweise und Vorsichtsmaßnahmen sind bei der Anwendung von Pembrolizumab zu beachten:
- Rückverfolgbarkeit: Bezeichnung und Chargenbezeichnung des Arzneimittels müssen eindeutig dokumentiert werden.
- Bestimmung des PD-L1-Status: Eine validierte Methode zur Bestimmung des PD-L1-Status des Tumors ist erforderlich.
- Immunvermittelte Nebenwirkungen: Schwere immunvermittelte Nebenwirkungen, einschließlich tödlicher Fälle, traten auf. Diese sind oft reversibel und durch Therapieunterbrechung und Kortikosteroide beherrschbar. Sie können auch nach der letzten Dosis auftreten.
- Immunvermittelte Pneumonitis: Patienten auf Anzeichen und Symptome überwachen, radiologisch bestätigen und andere Ursachen ausschließen. Kortikosteroide bei Grad ≥ 2 Ereignissen. Therapie bei Grad-2-Pneumonitis unterbrechen, bei Grad-3 oder Grad-4 dauerhaft absetzen.
- Immunvermittelte Kolitis: Patienten auf Anzeichen und Symptome überwachen und andere Ursachen ausschließen. Kortikosteroide bei Grad ≥ 2 Ereignissen. Therapie bei Grad-2- oder Grad-3-Kolitis unterbrechen, bei Grad-4 dauerhaft absetzen.
- Immunvermittelte Hepatitis: Überwachen Sie Leberfunktion und Anzeichen einer Hepatitis. Kortikosteroide bei Grad-2- und Grad-3-Ereignissen. Therapie entsprechend des Schweregrads der Leberenzymerhöhung unterbrechen oder absetzen.
- Immunvermittelte Nephritis: Überwachen Sie Nierenfunktion und schließen Sie andere Ursachen aus. Kortikosteroide ab Grad ≥ 2 Ereignissen. Therapie bei Grad-2 unterbrechen, bei Grad-3 oder Grad-4 dauerhaft absetzen.
- Immunvermittelte Endokrinopathien: Überwachen Sie auf Endokrinopathien wie Nebenniereninsuffizienz und Schilddrüsenfunktionsstörungen. Kortikosteroide und Hormonsubstitution können erforderlich sein. Therapie bei Grad-2 unterbrechen, bei Grad-3 oder Grad-4 dauerhaft absetzen.
- Immunvermittelte Hautreaktionen: Überwachen Sie auf schwere Hautreaktionen. Kortikosteroide bei schweren Reaktionen. Therapie bei Grad-3 unterbrechen, bei Grad-4 dauerhaft absetzen. Bei Verdacht auf SJS oder TEN Therapie unterbrechen und bei Bestätigung dauerhaft absetzen.
- Organtransplantation: Die Behandlung kann das Risiko einer Organabstoßung erhöhen. Nutzen-Risiko-Abwägung erforderlich.
- Stammzelltransplantationen (allo-HSZT): Bei Patienten nach Pembrolizumab-Therapie wurden GVHD und VOD beobachtet. Risiko transplantationsbedingter Komplikationen sorgfältig abwägen.
- Infusionsbedingte Reaktionen: Schwere Reaktionen wie Überempfindlichkeit und Anaphylaxie wurden berichtet. Bei Grad-3 oder Grad-4 dauerhaft absetzen. Bei Grad-1 oder Grad-2 unter engmaschiger Überwachung fortsetzen.
- Kombination mit Chemotherapie: Bei Patienten ≥ 75 Jahren mit Vorsicht anwenden.
- Erkrankungsspezifische Vorsichtsmaßnahmen: Besondere Vorsicht bei Patienten mit Urothelkarzinom nach Platin-basierter Therapie.
- Von klinischen Studien ausgeschlossene Patienten: Patienten mit schweren Autoimmunerkrankungen, aktiven ZNS-Metastasen und anderen schwerwiegenden Erkrankungen waren ausgeschlossen. Anwendung nur nach sorgfältiger Abwägung.
- Patientenkarte: Patienten müssen über die Risiken der Therapie informiert werden und die Patientenkarte erhalten.
Wirkstoff-Informationen
- Fachinformation Keytruda
- Poole, Raewyn M. "Pembrolizumab: first global approval." Drugs 74.16 (2014): 1973-1981.
- Choueiri, Toni K., et al. "Overall survival with adjuvant pembrolizumab in renal-cell carcinoma." New England Journal of Medicine 390.15 (2024): 1359-1371.
- Balan, Lavinia, et al. "Clinical Outcomes and Molecular Predictors of Pembrolizumab (Keytruda) as a PD-1 Immune Checkpoint Inhibitor in Advanced and Metastatic Cervical Cancer: A Systematic Review and Meta-Analysis." Biomedicines 12.5 (2024): 1109.