Febuxostat
Febuxostat ist ein Wirkstoff aus der Gruppe der Xanthinoxidasehemmer (Urikostatika), der zur Senkung erhöhter Harnsäurespiegel bei chronischer Hyperurikämie und damit assoziierten Erkrankungen eingesetzt wird.
Febuxostat: Übersicht
Anwendung
Der urikostatische Wirkstoff Febuxostat (Adenuric) ist indiziert zur Behandlung der chronischen Hyperurikämie bei Erkrankungen, die bereits zu Uratablagerungen geführt haben (einschließlich eines aus der Krankengeschichte bekannten oder aktuell vorliegenden Gichtknotens und/oder einer Gichtarthritis).
Anwendungsart
Febuxostat ist als Filmtablette (80 und 120 mg) erhältlich und zur Anwendung bei Erwachsenen bestimmt. Die Einnahme kann nahrungsunabhängig erfolgen.
Wirkmechanismus
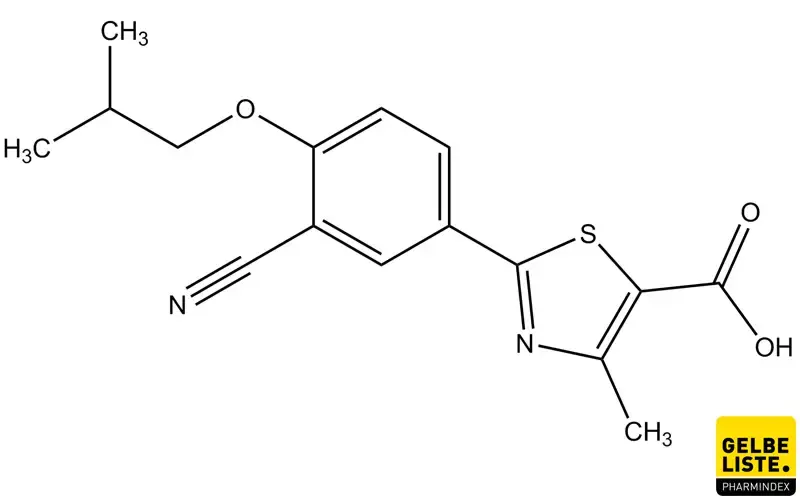
Febuxostat ist ein 2-Aryl-Thiazol-Derivat, dessen pharmakologische Wirkung auf der selektiven Hemmung des Enzyms Xanthinoxidase (XO) beruht. Das Enzym XO katalysiert die Bildung von Harnsäure, dem Endprodukt des Purin-Metabolismus beim Menschen.
Harnsäure entsteht im Rahmen der Reaktionskaskade Hypoxanthin → Xanthin → Harnsäure. Beide Reaktionsschritte dieser Kaskade werden durch das Enzym XO katalysiert. Durch Inhibition des Enzyms (Febuxostat hemmt sowohl die oxidierten als auch die reduzierten Formen von XO) liegen vermehrt Hypoxanthin und Xanthin vor, die im Vergleich zu Harnsäure besser wasserlöslich sind und besser renal eliminiert werden können. Im Gegensatz zu anderen Xanthinoxidasehemmern wie Allopurinol oder Oxipurinol (aktiver Allopurinol-Metabolit) ist Febuxostat kein Purin-Derivat.
Wirkstoffe aus der Gruppe der Xanthinoxidasehemmer werden den Urikostatika zugeordnet, da sie die Bildung von Harnsäure reduzieren.
Pharmakokinetik
Allgemein
- Bei gesunden Probanden erhöhen sich die maximalen Plasmakonzentrationen (cmax) und die AUC von Febuxostat nach Applikation einfacher und multipler Dosen von 10 mg bis 120 mg dosisproportional.
- Für Dosen zwischen 120 mg und 300 mg wird für Febuxostat ein Anstieg der AUC beobachtet, der größer als der dosisproportionale Anstieg ist.
- Es erfolgt keine erkennbare Akkumulation bei der 1x täglichen Anwendung von 10 mg bis 240 mg Febuxostat alle 24 Stunden.
- Febuxostat hat eine scheinbare mittlere terminale Eliminationshalbwertzeit (t½) von etwa 5 bis 8 Stunden.
- Im Allgemeinen stimmen die durch Analysen geschätzten pharmakokinetischen Parameter von Febuxostat bei Patienten mit Hyperurikämie und Gicht mit denen überein, die bei gesunden Probanden erhoben wurden (dies spricht dafür, dass gesunde Probanden repräsentativ für die pharmakokinetische/pharmakodynamische Bewertung in der Patientenpopulation mit Gicht sind).
Resorption
- Febuxostat wird rasch (tmax 1,0-1,5 h) und gut resorbiert (mindestens 84%).
- Nach der Einnahme einfacher oder multipler oraler Dosen von 80 und 120 mg 1x täglich beträgt die cmax etwa 2,8-3,2 μg/mL und 5,0-5,3 μg/mL.
- Nach der Einnahme multipler oraler Dosen von 80 mg 1x täglich oder einer einmaligen Dosis von 120 mg zusammen mit einer fettreichen Mahlzeit tritt eine Senkung der cmax um 49% bzw. 38% sowie ein Rückgang der AUC um 18% bzw. 16% auf (jedoch wurde keine klinisch signifikante Veränderung im prozentualen Rückgang der Serumharnsäurekonzentration beobachtet, sofern dies geprüft wurde).
Verteilung
- Das scheinbare Steady-State-Verteilungsvolumen (Vss/F) von Febuxostat liegt im Bereich von 29 bis 75 L nach Einnahme von Dosen von 10-300 mg.
- Die Plasmaproteinbindung von Febuxostat beträgt etwa 99,2% (primäre Bindung an Albumin) und ist über die Konzentrationsbreite, die mit Dosen von 80 und 120 mg erreicht wird, konstant.
- Die Plasmaproteinbindung der aktiven Metaboliten liegt im Bereich von etwa 82% bis 91%.
Metabolismus
- Febuxostat wird weitgehend durch Konjugation über das Uridindiphosphatglucuronosyltransferase (UDPGT)-Enzymsystem sowie durch Oxidation über das Cytochrom P450 (CYP)-System verstoffwechselt.
- Vier pharmakologisch wirksame Hydroxylmetaboliten wurden ermittelt, von denen drei im menschlichen Plasma nachzuweisen sind.
- In-vitro-Studien zeigen, dass diese oxidativen Metaboliten vorwiegend durch CYP1A1, CYP1A2, CYP2C8 oder CYP2C9 gebildet werden, und, dass Febuxostat-Glukuronid hauptsächlich durch UGT 1A1, 1A8 und 1A9 entsteht.
Elimination
- Febuxostat wird sowohl über die Leber als auch über die Nieren eliminiert.
- Nach Einnahme einer 80-mg-Dosis von Febuxostat finden sich etwa 49% der Dosis im Urin als unverändertes Febuxostat (3%), Acylglukuronid des Wirkstoffs (30%), dessen bekannte oxidative Metaboliten und ihrer Konjugate (13%) sowie als weitere unbekannte Metaboliten (3%) wieder.
- Neben der Ausscheidung über den Urin finden sich auch etwa 45% der Dosis im Stuhl als unverändertes Febuxostat (12%), Acylglukuronid des Wirkstoffs (1%), dessen bekannte oxidative Metaboliten und ihrer Konjugate (25%) sowie als weitere unbekannte Metaboliten (7%) wieder.
Patientenindividuelle Pharmakokinetik
- Nierenfunktionseinschränkung: Nach der Einnahme multipler Dosen von 80 mg Febuxostat bei Patienten mit leichter, mittelschwerer oder schwerer Nierenfunktionseinschränkung verändert sich die cmax von Febuxostat nicht im Verhältnis zu Probanden mit normaler Nierenfunktion. Die mittlere Gesamt-AUC von Febuxostat nimmt um etwa das 1,8-Fache von 7,5 μg×h/mL in der Gruppe mit normaler Nierenfunktion auf 13,2 μg×h/mL in der Gruppe mit schwerer Nierendysfunktion zu. Die cmax und AUC der aktiven Metaboliten erhöhen sich um das bis zu 2- bzw. 4-Fache (bei Patienten mit leichter oder mittelschwerer Nierenfunktionseinschränkung ist jedoch keine Dosisanpassung erforderlich).
- Leberfunktionseinschränkung: Nach Einnahme multipler Dosen von 80 mg Febuxostat bei Patienten mit leichter (Child-Pugh-Klassifikation A) oder mittelschwerer (Child-Pugh-Klassifikation B) Leberfunktionseinschränkung verändert sich die cmax und AUC von Febuxostat und dessen Metaboliten nicht signifikant im Vergleich zu Probanden mit normaler Leberfunktion. Es wurden keine Studien bei Patienten mit schwerer Leberfunktionseinschränkung (Child-Pugh-Klassifikation C) durchgeführt.
- Geschlecht: Nach Einnahme multipler Dosen von Febuxostat sind cmax und AUC bei Frauen um 24% bzw. 12% höher als bei Männern (allerdings sind die gewichtskorrigierten cmax- und AUC-Werte für die Geschlechter ähnlich, weshalb keine geschlechtsspezifische Dosisanpassung erforderlich ist).
Dosierung
- Empfohlene Tagesdosis: 1x täglich 80 mg unabhängig von der Nahrungsaufnahme
- Wenn der Serumharnsäurespiegel nach 2-4 Wochen immer noch > 6 mg/dL (357 μmol/L) beträgt, kann eine Dosiserhöhung auf 1x täglich 120 mg in Betracht gezogen werden.
- Febuxostat wirkt ausreichend schnell, sodass bereits nach 2 Wochen der Serumharnsäurespiegel erneut getestet werden kann.
- Therapeutisches Ziel ist die dauerhafte Senkung des Serumharnsäurespiegels auf unter 6 mg/dL (357 μmol/L).
- Gegen Gichtanfälle wird eine Prophylaxe von mindestens 6 Monaten empfohlen.
- Die empfohlene Dosis bei Patienten mit leichter Leberfunktionseinschränkung beträgt 80 mg (für Patienten mit mittelschwerer Leberfunktionseinschränkung liegen nur begrenzt Daten vor).
Nebenwirkungen
Die bei Gichtpatienten häufigsten Nebenwirkungen, die in klinischen Studien, in Sicherheitsstudien nach der Zulassung und durch Erfahrungen nach Markteinführung berichtet wurden, umfassen:
- Akute Gichtanfälle (wurden häufig kurz nach Beginn der Therapie und während der ersten Monate beobachtet, wobei die Häufigkeit von akuten Gichtanfällen mit zunehmender Dauer der Behandlung abnimmt und eine Prophylaxe für akute Gichtanfälle empfohlen wird)
- Leberfunktionsstörungen
- Durchfall
- Übelkeit
- Kopfschmerzen,
- Schwindelgefühl/Benommenheit
- Dyspnoe
- Hautausschlag
- Pruritus
- Arthralgie
- Myalgie
- Schmerzen in einer Extremität
- Ödeme
- Abgeschlagenheit
Diese Nebenwirkungen waren vorwiegend leicht oder mittelschwer ausgeprägt.
Seltene schwerwiegende Überempfindlichkeitsreaktionen gegenüber Febuxostat (einige davon im Zusammenhang mit systemischen Symptomen) und seltene Fälle plötzlichen Herztods traten nach Markteinführung auf.
Wechselwirkungen
Febuxostat kann potenziell mit unterschiedlichen Wirkstoffen wechselwirken.
Diese umfassen:
- Mercaptopurin/Azathioprin: Aufgrund des Wirkmechanismus von Febuxostat (XO-Hemmung) wird die gleichzeitige Anwendung nicht empfohlen. Die Hemmung der XO durch Febuxostat kann zu erhöhten Plasmakonzentrationen der beiden Arzneistoffe und somit zu myelotoxischen Wirkungen führen. Bei gleichzeitiger Anwendung von Febuxostat sollte die Dosis von Mercaptopurin/Azathioprin auf 20% oder weniger der zuvor verordneten Dosis reduziert werden. Die Dosisanpassung, welche auf Basis einer Modellierungs- und Simulationsanalyse von Daten aus einer präklinischen Studie an Ratten vorgeschlagen wurde, ist durch die Ergebnisse einer klinischen Arzneimittelwechselwirkungsstudie an gesunden Probanden, die 100 mg Azathioprin allein bzw. eine reduzierte Dosis von Azathioprin (25 mg) in Kombination mit Febuxostat (40 oder 120 mg) erhielten, als geeignet bestätigt worden. Wechselwirkungsstudien zu Febuxostat und einer anderen zytotoxischen Chemotherapie wurden nicht durchgeführt. Zur Sicherheit von Febuxostat während einer anderen zytotoxischen Therapie liegen keine Daten vor.
- Rosiglitazon/CYP2C8-Substrate: Febuxostat zeigt in vitro eine schwache Hemmung von CYP2C8. In einer Studie an gesunden Probanden hatte die Gabe von 120 mg Febuxostat 1x täglich zusammen mit einer oralen Einzeldosis von 4 mg Rosiglitazon keine Auswirkung auf die Pharmakokinetik von Rosiglitazon und seinem Metaboliten N-desmethyl-Rosiglitazon, was darauf hindeutet, dass Febuxostat kein Inhibitor des CYP2C8-Enzyms in vivo ist. Daher wird nicht damit gerechnet, dass bei der Verabreichung von Febuxostat zusammen mit Rosiglitazon oder anderen CYP2C8-Substraten eine Dosisanpassung für diese Präparate erforderlich wird.
- Theophyllin: Eine Wechselwirkungsstudie mit Febuxostat wurde bei gesunden Probanden durchgeführt, um beurteilen zu können, ob die XO-Hemmung (wie bei anderen XO-Hemmern berichtet) zu einem Anstieg des zirkulierenden Theophyllinspiegels führen kann. Die Ergebnisse der Studie zeigten, dass die Gabe von 80 mg Febuxostat 1× täglich zusammen mit einer Einzeldosis von 400 mg Theophyllin keine Auswirkung auf die Pharmakokinetik oder Sicherheit von Theophyllin hatten. Daher ist keine besondere Vorsicht geboten, wenn 80 mg Febuxostat und Theophyllin zusammen angewendet werden (für 120 mg Febuxostat liegen keine Daten vor).
- Naproxen und sonstige Hemmer der Glucuronidierung: Die Metabolisierung von Febuxostat erfolgt Uridinglucuronosyltransferase (UGT)-abhängig. Wirkstoffe, die die Glucuronidierung hemmen (wie NSAR und Probenecid), könnten theoretisch die Elimination von Febuxostat beeinträchtigen. Bei Probanden war die gleichzeitige Gabe von Febuxostat und Naproxen 250 mg 2x täglich mit einem Anstieg der Febuxostatexposition (cmax 28%, AUC 41% und t½ 26%) assoziiert. In klinischen Studien stand die Anwendung von Naproxen oder anderen NSAR/COX-2-Hemmern nicht in Zusammenhang mit einer klinisch signifikanten Zunahme von unerwünschten Ereignissen. Febuxostat kann demnach zusammen mit Naproxen angewendet werden, ohne dass für Febuxostat oder Naproxen Dosisanpassungen vorgenommen werden müssen.
- Induktoren der Glucuronidierung: Wirkstarke Induktoren der UGT-Enzyme könnten möglicherweise zu einer verstärkten Metabolisierung und herabgesetzten Wirksamkeit von Febuxostat führen. Daher wird 1-2 Wochen nach Behandlungsbeginn mit einem wirkstarken Induktor der Glucuronidierung eine Kontrolle der Serumharnsäure empfohlen. Umgekehrt kann die Beendigung einer Induktor-Behandlung zu erhöhten Plasmaspiegeln von Febuxostat führen.
- Desipramin/CYP2D6-Substrate: Es konnte gezeigt werden, dass Febuxostat in vitro ein schwacher CYP2D6-Hemmer ist. In einer Studie mit Probanden bewirkten 120 mg Febuxostat 1× täglich eine mittlere 22%ige Zunahme der AUC von Desipramin (einem CYP2D6-Substrat), was auf eine mögliche schwache inhibitorische Wirkung von Febuxostat auf das CYP2D6-Enzym in vivo hinweist. Demnach wird nicht erwartet, dass die gleichzeitige Anwendung von Febuxostat mit anderen CYP2D6-Substraten eine Dosisanpassung für diese Substanzen erfordert.
- Antazida: Es konnte gezeigt werden, dass die gleichzeitige Einnahme eines Antazidums, das Magnesiumhydroxid und Aluminiumhydroxid enthält, die Aufnahme von Febuxostat (um etwa 1 Stunde) verzögert und einen Rückgang der cmax um 32%, jedoch keine signifikante Veränderung der AUC bewirkt. Daher kann Febuxostat ungeachtet einer möglichen Einnahme von Antazida angewendet werden.
Kontraindikationen
Febuxostat darf nicht angewendet werden bei Überempfindlichkeit gegen den Wirkstoff oder sonstige Bestandteile des Arzneimittels.
Schwangerschaft
Daten über eine sehr begrenzte Anzahl von exponierten Schwangerschaften lassen nicht auf Nebenwirkungen von Febuxostat auf die Schwangerschaft oder die Gesundheit des Fetus/Neugeborenen schließen. Tierexperimentelle Studien lassen ebenfalls nicht auf direkte oder indirekte schädliche Auswirkungen auf Schwangerschaft, embryonale/fetale Entwicklung oder Geburt schließen. Das potenzielle Risiko für den Menschen ist allerdings nicht bekannt, weshalb Febuxostat während der Schwangerschaft nicht angewendet werden sollte.
Stillzeit
Es ist nicht bekannt, ob Febuxostat beim Menschen in die Muttermilch übergeht. Tierexperimentelle Studien haben einen Übergang von Febuxostat in die Muttermilch und eine Beeinträchtigung der Entwicklung der gesäugten Jungtiere gezeigt. Ein Risiko für den gestillten Säugling kann daher nicht ausgeschlossen werden, weshalb Febuxostat während der Stillzeit nicht angewendet werden sollte.
Verkehrstüchtigkeit
Schläfrigkeit, Schwindel, Parästhesie und verschwommenes Sehen können im Zusammenhang mit der Anwendung von Febuxostat auftreten. Daher sollten Patienten beim Steuern eines Fahrzeuges, Bedienen von Maschinen oder bei der Ausübung gefährlicher Tätigkeiten vorsichtig sein, bis sie sich einigermaßen
sicher sein können, dass Febuxostat ihre Leistung nicht nachteilig beeinflusst.
Weitere Informationen können der jeweiligen Fachinformation entnommen werden.
Anwendungshinweise
Kardiovaskuläre Erkrankungen
- Bei Patienten mit bestehenden schweren kardiovaskulären Erkrankungen (z.B. Myokardinfarkt, Schlaganfall oder instabile Angina pectoris) wurde während der Entwicklungsphase des Arzneimittels und in einer Studie nach Erteilung der Zulassung (CARES) eine höhere Anzahl von tödlichen kardiovaskulären Ereignissen unter Febuxostat im Vergleich zu Allopurinol beobachtet.
- In einer weiteren Studie nach Erteilung der Zulassung (FAST) war Febuxostat in Bezug auf die Inzidenz tödlicher und nicht-tödlicher kardiovaskulärer Ereignisse Allopurinol jedoch nicht unterlegen.
- Die Behandlung dieser Patientengruppe sollte mit Vorsicht erfolgen und diese Patienten sollten regelmäßig überwacht werden.
- Patienten mit hämatologischen Malignomen, die sich einer Chemotherapie mit einem mittleren bis hohen Risiko für ein Tumorlyse-Syndrom unterziehen und mit Febuxostat behandelt werden, sollten (wenn klinisch erforderlich) bezüglich ihrer Herzfunktion überwacht werden.
Arzneimittelallergie/-überempfindlichkeit
- Nach Markteinführung wurde selten über schwerwiegende allergische Reaktionen/Überempfindlichkeitsreaktionen berichtet (darunter das lebensbedrohliche Stevens-Johnson-Syndrom, toxische epidermale Nekrolyse und akute anaphylaktische Reaktionen/Schock).
- In den meisten Fällen traten diese Reaktionen während des ersten Monats der Therapie mit Febuxostat auf (einige, aber nicht alle dieser Patienten berichteten über Nierenfunktionseinschränkungen und/oder vorangegangene Überempfindlichkeit gegen Allopurinol).
- Schwere Überempfindlichkeitsreaktionen, einschließlich Arzneimittelwirkung mit Eosinophilie und systemischen Symptomen (DRESS), waren in einigen Fällen mit Fieber, hämatologischer, renaler oder hepatischer Beteiligung verbunden.
- Die Anzeichen und Symptome von allergischen Reaktionen/Überempfindlichkeitsreaktionen sollten Patienten mitgeteilt werden (außerdem sollten Patienten auf solche Symptome hin streng überwacht werden).
- Die Febuxostat-Behandlung sollte beim Auftreten von allergischen Reaktionen/Überempfindlichkeitsreaktionen, einschließlich Stevens-Johnson-Syndrom, sofort abgebrochen werden, da ein frühes Absetzen mit einer besseren Prognose assoziiert wird.
- Wenn beim Patienten allergische Reaktionen/Überempfindlichkeitsreaktionen, einschließlich Stevens-Johnson-Syndrom und einer akuten anaphylaktischen Reaktion/Schock, aufgetreten sind, darf die Febuxostat-Behandlung bei diesem Patienten zu keinem Zeitpunkt wieder aufgenommen werden.
Akute Gichtanfälle (Gichtschub)
- Mit der Febuxostat-Behandlung sollte erst nach vollständigem Abklingen des akuten Gichtanfalls begonnen werden.
- Während des Behandlungsbeginns kann es zu einem akuten Gichtanfall kommen, weil durch die Senkung des Serumharnsäurespiegels zunächst Harnsäureablagerungen im Gewebe mobilisiert werden können.
- Bei Beginn der Febuxostat-Behandlung wird daher eine Anfallsprophylaxe mit einem nichtsteroidalen Antirheumatikum (NSAR) oder mit Colchicin über mindestens 6 Monate empfohlen.
- Wenn es während der Febuxostat-Behandlung zu einem akuten Gichtanfall kommt, darf die Behandlung nicht abgesetzt werden.
- Der Gichtanfall sollte mit einer individuell auf den Patienten zugeschnittenen Begleittherapie behandelt werden.
- Die kontinuierliche Weiterbehandlung mit Febuxostat senkt die Häufigkeit und Intensität von Gichtanfällen.
Xanthinablagerung
- Bei Patienten mit stark erhöhter Harnsäurebildungsrate (z.B. bei malignen Erkrankungen und deren Behandlung, Lesch-Nyhan-Syndrom) kann die absolute Konzentration von Xanthin im Urin in seltenen Fällen so weit ansteigen, dass es zu einer Ablagerung im Harntrakt kommt (dies wurde im Rahmen der klinischen Zulassungsstudie mit Febuxostat beim Tumorlyse-Syndrom nicht beobachtet).
- Da zu Febuxostat keine Erfahrungen vorliegen, wird die Anwendung bei Patienten mit Lesch-Nyhan-Syndrom nicht empfohlen.
Mercaptopurin/Azathioprin
- Die Anwendung von Febuxostat wird nicht empfohlen bei Patienten, die gleichzeitig mit Mercaptopurin/Azathioprin behandelt werden, da die Hemmung der Xanthinoxidase durch Febuxostat erhöhte Plasmakonzentrationen von Mercaptopurin/Azathioprin verursachen kann, die zu einer schweren Toxizität führen könnten.
- Kann die Kombination dennoch nicht vermieden werden, wird eine Reduktion der Dosis von Mercaptopurin/Azathioprin auf 20% oder weniger der zuvor verordneten Dosis empfohlen, um mögliche hämatologische Wirkungen zu vermeiden.
- Die Patienten müssen engmaschig überwacht werden und die Dosis von Mercaptopurin/Azathioprin sollte anschließend auf Grundlage der Bewertung der therapeutischen Wirkung und des Auftretens eventueller toxischer Wirkungen angepasst werden.
Organtransplantatempfänger
- Da es bei Organtransplantatempfängern keine Erfahrungen gibt, wird die Anwendung von Febuxostat in dieser Patientengruppe nicht empfohlen.
Leber- und/oder Schilddrüsenerkrankungen
- In der kombinierten Auswertung der klinischen Studien der Phase 3 wurden leichte Erhöhungen der Leberfunktionswerte bei mit Febuxostat behandelten Patienten beobachtet (5,0%), weshalb empfohlen wird, vor Beginn der Febuxostat-Behandlung und im weiteren Verlauf je nach klinischem Befund einen Leberfunktionstest durchzuführen.
- Erhöhte TSH-Werte (> 5,5 μIE/mL) wurden bei Patienten unter Langzeitbehandlung mit Febuxostat (5,5%) in offenen Langzeit-Verlängerungsstudien beobachtet.
- Vorsicht ist geboten, wenn Febuxostat bei Patienten mit veränderter Schilddrüsenfunktion zur Anwendung kommen soll.
Alternativen
Die medikamentösen Therapiealternativen richten sich nach dem Indikationsgebiet und sind darüber hinaus abhängig von patientenindividuellen Faktoren wie dem Alter der Patienten, Komorbiditäten oder dem Schweregrad der Erkrankung. Die Pharmakotherapie der chronischen Hyperurikämie und damit assoziierten Erkrankungen bietet ein bestimmtes Spektrum an alternativen Wirkstoffen. Dabei wird im Allgemeinen zwischen Wirkstoffen zur Therapie des akuten Gichtanfalls und Wirkstoffen zur Harnsäure-senkenden Therapie unterschieden.
Therapie des akuten Gichtanfalls
- NSAR
- Colchicin
- Glucocorticoide
- Anti-IL-1β-Antikörper wie Canakinumab
Harnsäure-senkende Therapie
- Urikostatika (Senkung der Harnsäurebildung): Andere Xanthinoxidasehemmer wie Allopurinol
- Urikosurika (Steigerung der Harnsäureausscheidung): Benzbromaron und Probenecid
- Urikolytika (Steigerung des Harnsäureabbaus): Rasburicase (rekombinantes Uratoxidase-Enzym , das die Oxidation von Harnsäure zum gut wasserlöslichen Allantoin katalysiert)
Wirkstoff-Informationen
- EMA: Fachinformation Adenuric
- Freissmuth et al., Pharmakologie und Toxikologie, 2020, Springer
- Mutschler et al., Mutschler Arzneimittelwirkungen, 2019, Wissenschaftliche Verlagsgesellschaft Stuttgart
- AWMF: S2e-Leitlinie Gichtarthritis (in Überarbeitung, Stand 2016)
-
Adenuric 80 mg Abacus Filmtabletten
Abacus Medicine A/S
-
Adenuric 80 mg ACA Filmtabletten
A.C.A. Müller ADAG Pharma AG
-
Adenuric 80 mg B2B Medical Filmtabletten
B2B Medical GmbH
-
Adenuric 80 mg CC Pharma Filmtabletten
CC Pharma GmbH
-
Adenuric 80 mg docpharm Filmtabletten
Docpharm GmbH
-
Adenuric 80 mg Eurim Filmtabletten
Eurim-Pharm Arzneimittel GmbH
-
ADENURIC 80 mg Filmtabletten
Berlin-Chemie AG
-
Adenuric 80 mg kohlpharma Filmtabletten
kohlpharma GmbH
-
Adenuric 80 mg Orifarm Filmtabletten
Orifarm GmbH
-
Adenuric 80 mg Originalis Filmtabletten
Originalis B.V.
-
Adenuric 80mg Mpa Pharma Filmtabletten
Mpa Pharma GmbH
-
Adenuric 120 mg Abacus Filmtabletten
Abacus Medicine A/S
-
Adenuric 120 mg ACA Filmtabletten
A.C.A. Müller ADAG Pharma AG
-
Adenuric 120 mg BB Farma Filmtabletten
BB Farma S.R.L.
-
Adenuric 120 mg CC Pharma Filmtabletten
CC Pharma GmbH
-
Adenuric 120 mg Fd Pharma Filmtabletten
FD Pharma GmbH
-
ADENURIC 120 mg Filmtabletten
Berlin-Chemie AG
-
Adenuric 120 mg Gerke Filmtabletten
Pharma Gerke Arzneimittelvertriebs GmbH
-
Adenuric 120 mg kohlpharma Filmtabletten
kohlpharma GmbH
-
Febuxodor® 80 mg Filmtabletten
TAD Pharma GmbH
-
Febuxodor® 120 mg Filmtabletten
TAD Pharma GmbH
-
Febuxostat - 1 A Pharma® 80 mg Filmtabletten
1 A Pharma GmbH
-
Febuxostat - 1 A Pharma® 120 mg Filmtabletten
1 A Pharma GmbH
-
Febuxostat AbZ 80 mg Filmtabletten
AbZ Pharma GmbH
-
Febuxostat AbZ 120 mg Filmtabletten
AbZ Pharma GmbH
-
Febuxostat AL 80 mg Filmtabletten
ALIUD PHARMA® GmbH
-
Febuxostat AL 120 mg Filmtabletten
ALIUD PHARMA® GmbH
-
Febuxostat Aristo 80 mg Filmtabletten
Aristo Pharma GmbH
-
Febuxostat Aristo 120 mg Filmtabletten
Aristo Pharma GmbH
-
Febuxostat AXiromed 80 mg Filmtabletten
Medical Valley Invest AB
-
Febuxostat AXiromed 120 mg Filmtabletten
Medical Valley Invest AB
-
Febuxostat beta 80 mg Filmtabletten
betapharm Arzneimittel GmbH
-
Febuxostat beta 120 mg Filmtabletten
betapharm Arzneimittel GmbH
-
Febuxostat GeneVida 80 mg Filmtabletten
GeneVida GmbH
-
Febuxostat GeneVida 120 mg Filmtabletten
GeneVida GmbH
-
Febuxostat Heumann 80 mg Filmtabletten
Heumann Pharma GmbH & Co. Generica KG
-
Febuxostat Heumann 120 mg Filmtabletten
Heumann Pharma GmbH & Co. Generica KG
-
Febuxostat Indoco 80 mg Filmtabletten
HEC Pharm GmbH
-
Febuxostat Indoco 120 mg Filmtabletten
HEC Pharm GmbH
-
Febuxostat Mylan 80 mg Filmtabletten
Viatris Healthcare GmbH
-
Febuxostat Mylan 120 mg Filmtabletten
Viatris Healthcare GmbH
-
Febuxostat PUREN 80 mg Filmtabletten
PUREN Pharma GmbH & Co. KG
-
Febuxostat PUREN 120 mg Filmtabletten
PUREN Pharma GmbH & Co. KG
-
Febuxostat-ratiopharm® 80 mg Filmtabletten
ratiopharm GmbH
-
Febuxostat-ratiopharm® 120 mg Filmtabletten
ratiopharm GmbH
-
Febuxostat STADA® 80 mg Filmtabletten
STADAPHARM GmbH
-
Febuxostat STADA® 120 mg Filmtabletten
STADAPHARM GmbH
-
Febuxostat Vivanta 80 mg Filmtabletten
Vivanta Generics s.r.o
-
Febuxostat Vivanta 120 mg Filmtabletten
Vivanta Generics s.r.o
-
Febuxostat Zentiva 80 mg Filmtabletten
Zentiva Pharma GmbH













