Budesonid
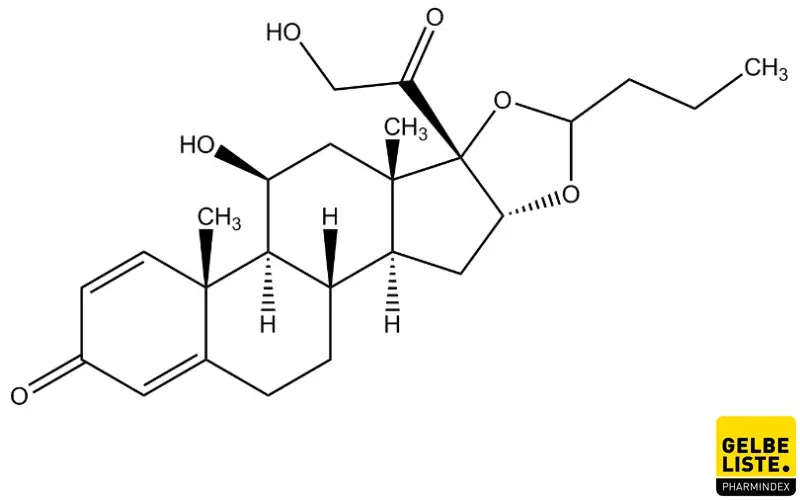
Budesonid ist ein Glukokortikoid mit ausgeprägter entzündungshemmender Wirkung, das in der Therapie von chronisch-entzündlichen Erkrankungen wie Asthma bronchiale, COPD, verschiedenen Formen der Kolitis und bei allergischem Schnupfen angewendet wird.
Budesonid: Übersicht
Anwendung
Budesonid ist für die Behandlung verschiedener Erkrankungen indiziert, die von chronisch-entzündlichen Darmerkrankungen bis hin zu Atemwegserkrankungen reichen:
- Asthma bronchiale: Zur Langzeitkontrolle und Prävention von Symptomen des Asthma bronchiale bei Erwachsenen und Kindern.
- Chronisch obstruktive Lungenerkrankung (COPD): Als Teil einer Kombinationstherapie zur Verringerung der Häufigkeit von Exazerbationen der COPD.
- Nicht-infektiöse Rhinitis, einschließlich allergischer Rhinitis (Heuschnupfen): Zur Behandlung der Nasensymptome.
- Nasenpolypen: Zur Reduktion von Nasenpolypen und der damit verbundenen Symptome.
- Chronisch-entzündliche Darmerkrankungen (CED): Dazu gehören Morbus Crohn und Colitis ulcerosa für die Behandlung bestimmter Patientengruppen.
- Autoimmunhepatitis: Ein weniger häufiges Anwendungsgebiet, bei dem Budesonid zur Kontrolle der Entzündung der Leber eingesetzt wird.
- Eosinophile Ösophagitis: Für die Behandlung von Entzündungen und damit verbundenen Symptomen der Speiseröhre.
- Mikroskopische Kolitis: Zur Behandlung von wässriger Diarrhö und Entzündung des Dickdarms.
Wirkmechanismus
Budesonid ist ein nicht-halogeniertes Glukokortikoid. Es wirkt primär antiphlogistisch, indem es an Glukokortikoid-Rezeptoren bindet. Dabei ist die Bindungs-Affinität von Budesonid ungefähr 15-mal stärker als die von Prednisolon. Budesonid beeinflusst zahlreiche Zelltypen wie Mastzellen, Eosinophile, Neutrophile, Makrophagen und Lymphozyten. Zudem hemmt der Wirkstoff (abhängig von Applikation und Wirkort) die antigenstimulierte Ausschüttung zahlreicher proinflammatorischer Signalmoleküle wie Interleukine, RANTES, TNF-α, IFN-γ und GM-CSF oder Eotaxin-3. Infolge kommt es zu einer signifikanten Abnahme der entzündungsbedingten Infiltration der Schleimhäute von Magen, Darm, Speiseröhre oder Atemwegen.
Pharmakokinetik
Die Pharmakokinetik von Budesonid richtet sich nach Art und Applikationsform (beispielsweise als Aerosol, Rektalschaum, Nasenspray, Schmelztablette oder magensaftresistente Hartkapsel) des Arzneimittels. Grundsätzlich bindet der Wirkstoff in hohem Maß an Plasmaproteine und wird gut im Gewebe verteilt. Nach oraler Gabe beträgt die systemische Verfügbarkeit etwa 10 Prozent. Budesonid wird hauptsächlich über CYP3A4, eine Untergruppe des Cytochrom-P-450-Systems, metabolisiert. Die durchschnittliche terminale Eliminationshalbwertszeit liegt nach oraler Gabe bei circa 3 bis 4 Stunden. Die mittlere Clearance für Budesonid beträgt etwa 10 l/min.
Dosierung
Budesonid ist in verschiedenen Formen für die orale, rektale, inhalative und nasale Anwendung verfügbar. Die Dosierung variiert je nach Erkrankung und Darreichungsform:
Orale Anwendung:
- Morbus Crohn und kollagene Kolitis: Empfohlen wird täglich 9 mg, vorzugsweise morgens, für 8 Wochen.
- Colitis ulcerosa: 9 mg täglich für bis zu 8 Wochen.
- Steroidabhängiger Morbus Crohn: Standarddosis von 6 mg täglich.
- Mikroskopische Kolitis: 9 mg täglich für 8 Wochen.
- Autoimmunhepatitis: Anfangsdosis von 9 mg täglich, aufgeteilt in drei Dosen; Erhaltungsdosis von 6 mg täglich in zwei Dosen.
- Eosinophile Ösophagitis: 2 mg täglich, verteilt auf zwei Dosen zu je 1 mg, für 6 bis 12 Wochen.
- Absetzen der Behandlung: Budesonid sollte schrittweise über bis zu zwei Wochen ausgeschlichen werden.
Rektale Anwendung:
- Colitis ulcerosa: 2 mg täglich als Rektalsuspension oder Rektalschaum für bis zu 8 Wochen.
Inhalative Anwendung:
- Asthma bronchiale: Dosierung variiert; bis zu 800 µg zweimal täglich für Erwachsene und Jugendliche, 400 µg zweimal täglich für Kinder.
- COPD: 200-400 µg zweimal täglich für Erwachsene.
- Suspension für Vernebler: 0,5-2 mg zweimal täglich, abhängig vom Alter und Zustand.
Nasale Anwendung:
- Allergischer Schnupfen und Nasenpolypen: Standarddosis variiert zwischen 50 µg und 128 µg pro Nasenloch, abhängig von Alter und spezifischer Bedingung.
Nebenwirkungen
Die Nebenwirkungen von Budesonid richten sich nach Art und Ort der Applikation. Bei oraler, inhalativer oder nasaler Anwendung kommt es häufig zu lokalen oralen und oropharyngealen Candidosen. Nachfolgend werden beispielhaft die typischen systemischen Nebenwirkungen aufgelistet.
Sehr häufig:
- Cushing-Syndrom, zum Beispiel mit Vollmondgesicht
- Stammfettsucht
- verminderter Glukosetoleranz
- Diabetes mellitus
- Hypertonie
- Natriumretention mit Ödembildung
- vermehrter Kaliumausscheidung
- Inaktivität bzw. Atrophie der Nebennierenrinde
- Striae rubrae
- Steroidakne
- Störung der Sexualhormonsekretion wie Amenorrhoe, Hirsutismus und/oder Impotenz
Häufig:
- Dyspepsie
- Erhöhung des Infektionsrisikos
- Muskel- und Gelenkschmerzen, Muskelschwäche und –zuckungen
- Osteoporose
- Kopfschmerzen
- Depressionen, Gereiztheit, Euphorie
- allergisches Exanthem, Petechien, Kontaktdermatitis
- verzögerte Wundheilung
Gelegentlich:
- Magen- oder Zwölffingerdarmgeschwür
- psychomotorische Hyperaktivität, Angst
Selten:
- Glaukom, Katarakt, verschwommenes Sehen
- Pankreatitis
- Osteonekrose
- Aggression
- Ekchymosen
Wechselwirkungen
Folgende Wechselwirkungen sind bei der Anwendung von Budesonid zu beachten:
- Budesonid kann bei gemeinsamer Gabe von Herzglykosiden die Glykosidwirkung durch einen hypokaliämischen Effekt verstärken. Die gleichzeitige Gabe von Saluretika erhöht möglicherweise das Risiko einer erhöhten Kaliumausscheidung.
- Bei einer gleichzeitigen Behandlung mit CYP3A-Inhibitoren einschließlich Cobicistat-haltiger Produkte muss mit einem erhöhten Risiko systemischer Nebenwirkungen gerechnet werden. Die Kombination sollte besser vermieden werden - es sei denn, der Nutzen überwiegt das erhöhte Risiko systemischer Glukokortikoid-Effekte. In diesem Fall sollten die Patienten hinsichtlich systemischer Glukokortikoidnebenwirkungen überwacht werden.
- Die gleichzeitige orale Gabe von einmal täglich 200 mg Ketoconazol kann die Plasmakonzentrationen von Budesonid um das 6-fache erhöhen. Bei Einnahme von Ketoconazol etwa 12 Stunden nach der Einnahme von Budesonid wurden erhöhte Konzentrationen um circa das 3-fache beobachtet. Noch erlaubt die Datenlage keine Dosierungsempfehlung. Deshalb wird diese Kombination auch nicht empfohlen.
- Wahrscheinlich können auch andere starke CYP3A4-Inhibitoren wie Ritonavir, Itraconazol, Clarithromycin und Grapefruitsaft die Plasmakonzentration von Budesonid erhöhen. Eine gleichzeitige Anwendung ist deshalb zu vermeiden.
- CYP3A4-Induktoren wie Carbamazepin und Rifampicin können sowohl die systemische als auch die lokale Verfügbarkeit von Budesonid verringern. Mitunter muss die Budesonid-Dosierung angepasst werden.
- Die gleichzeitige Gabe von Budesonid und Cimetidin in einer üblichen Dosierung hat einen geringen Effekt und wirkt sich klinisch vermutlich nicht relevant auf das pharmakokinetische Verhalten von Budesonid aus. Die gleichzeitige Gabe von Omeprazol soll die Pharmakokinetik von Budesonid ebenfalls nicht beeinflussen.
- Wirkstoffe, die durch CYP3A4 metabolisiert werden, konkurrieren mit Budesonid. Weist die konkurrierende Substanz eine höhere Affinität zu CYP3A4 auf, sind erhöhte Budesonid-Plasmakonzentrationen möglich. Bindet Budesonid stärker an CYP3A4, ist mit einem Anstieg des Plasmaspiegels der konkurrierenden Substanz zu rechnen. Möglicherweise muss die Dosis der konkurrierenden Substanz oder die von Budesonid angepasst werden.
- Wechselwirkungen mit steroidbindenden Kunstharzen, wie Colestyramin und mit Antazida können nicht ausgeschlossen werden. Bei gleichzeitiger Einnahme von Budesonid könnte dessen Wirkung abgeschwächt werden. Daher sollten diese Präparate nicht gleichzeitig eingenommen werden. Empfohlen wird ein zeitlicher Abstand von mindestens 2 Stunden.
- Da Budesonid die Nebennierenrindenfunktion unterdrücken kann, sind falsche Ergebnisse bei einem ACTH-Stimulationstest zur Diagnose einer Hypophyseninsuffizienz möglich. In der Regel werden unter Budesonid niedrige Werte gemessen.
- Bei Frauen, die gleichzeitig Östrogene oder orale Kontrazeptiva eingenommen haben, sind erhöhte Plasmaspiegel und eine verstärkte Wirkung von Glukokortikoiden wie Budesonid möglich.
Kontraindikationen
Budesonid darf nicht bei Überempfindlichkeit gegen den Wirkstoff angewendet werden. Je nach Applikationsform verbietet sich auch die Anwendung bei schwerer Leberfunktionsstörung wie Leberzirrhose.
Schwangerschaft
In Tierstudien verursachte Budesonid in hohen Dosen Anomalien in der Entwicklung des Fötus. Die klinische Relevanz für den Menschen ist unklar.
Eine Anwendung von Budesonid oral sowie rektal in der Schwangerschaft sollte vermieden werden, es sei denn, es liegen überzeugende Gründe für die Behandlung vor. Es liegen nur wenige Daten zum Ausgang der Schwangerschaft bei Anwendung von oral verabreichtem Budesonid beim Menschen vor, jedoch ist die Bioverfügbarkeit nach oraler Gabe niedrig.
Die Daten zur inhalativen Anwendung von Budesonid bei einer sehr großen Anzahl von exponierten Schwangerschaften ergaben keine Hinweise auf ein erhöhtes Nebenwirkungsrisiko für den Fötus und Neugeborene. Sowohl für Fetus als auch Mutter ist eine adäquate Asthmatherapie während der Schwangerschaft sehr wichtig. Vor der Anwendung von Budesonid während der Schwangerschaft ist jedoch eine Nutzen-Risiko-Abwägung erforderlich. Eine inhalative Anwendung sollte so kurz wie möglich erfolgen, zudem ist die geringste wirksame Dosis an Budesonid einzusetzen.
Nasales Budesonid sollte in der Schwangerschaft, vor allem im ersten Trimester, nur nach ärztlicher Anweisung eingesetzt werden.
Stillzeit
Budesonid geht in die Muttermilch über. Eine inhalative Erhaltungstherapie mit Budesonid bei stillenden Frauen mit Asthma führt zu einer vernachlässigbaren systemischen Exposition von gestillten Säuglingen. Die Plasmaproben-Konzentrationen von Budesonid bei Säuglingen lagen jedoch alle unter der Bestimmungsgrenze. Basierend auf Daten zu inhalativem Budesonid und der Tatsache, dass Budesonid innerhalb der therapeutischen Dosisintervalle nach nasaler, inhalativer, oraler und rektaler Verabreichung lineare pharmakokinetische Eigenschaften aufweist, ist eine niedrige Exposition des Säuglings bei therapeutischen Dosen von Budesonid zu erwarten. Diese Daten unterstützen die weitere orale sowie rektale Anwendung von Budesonid während der Stillzeit. Die Entscheidung für das Stillen oder Abstillen bzw. über einen Verzicht auf Budesonid muss sorgfältig gegen den Nutzen des Stillens für das Kind und den Nutzen der Therapie für die Mutter abgewogen werden.
Verkehrstüchtigkeit
Budesonid nasal bzw. inhalativ hat keinen oder einen zu vernachlässigenden Einfluss auf die Verkehrstüchtigkeit und die Fähigkeit zum Bedienen von Maschinen. Bei der oralen sowie rektalen Anwendung sollte berücksichtigt werden, dass gelegentlich Müdigkeit auftreten kann.
Anwendungshinweise
Folgende Warnhinweise und Vorsichtsmaßnahmen sind bei der Anwendung von Budesonid zu beachten:
- Besondere Überwachung: Bei Erkrankungen wie Tuberkulose, Hypertonie, Diabetes, Osteoporose, peptischem Ulkus, Glaukom und Katarakt, insbesondere bei Langzeitanwendung in hohen Dosen, ist Vorsicht geboten aufgrund erhöhter Risiken für systemische Nebenwirkungen.
- Infektionsrisiko: Budesonid kann die Immunantwort schwächen, wodurch das Risiko für Infektionen steigt. Atypische Symptome von schweren Infektionen können verschleiert sein, einschließlich Sepsis und Tuberkulose.
- Windpocken: Patienten unter Budesonid sollten Kontakt zu Personen mit Windpocken oder Herpes zoster vermeiden. Nicht immune Patienten benötigen bei Exposition eine passive Immunisierung.
- Masern: Exponierte Patienten mit geschwächtem Immunsystem sollten postexpositionell Immunglobulin erhalten.
- Impfstoffe: Dauerhaft mit Budesonid behandelte Patienten sollten keine Lebendimpfstoffe erhalten. Die Wirksamkeit anderer Impfstoffe könnte reduziert sein.
- Leberfunktion: Bei fortgeschrittener primär biliärer Zirrhose oder stark eingeschränkter Leberfunktion kann die systemische Verfügbarkeit von Budesonid erhöht sein. Die Behandlung muss sorgfältig abgewogen werden.
- Sehstörungen: Sehprobleme können auftreten und erfordern eine augenärztliche Untersuchung zur Abklärung möglicher Ursachen wie Katarakt oder Glaukom.
- Stresssituationen: Da Budesonid die Stressreaktion beeinträchtigen kann, sollte bei Operationen oder ähnlichem Stress eine adäquate systemische Glukokortikoidtherapie erfolgen.
Wirkstoff-Informationen
- Fachinformation, Budenofalk Hartkapseln
- Fachinformation, Budenofalk Rektalschaum
- Fachinformation, Budenofalk Granulat
- Fachinformation, Cortiment
- Fachinformation, Entocort Kapseln
- Fachinformation, Entocort Tabletten
- Fachinformation, Jorveza
- Fachinformation, Budapp
- Fachinformation, Budesonid acis Nasenspray
- Fachinformation, Budiair
- Fachinformation, Miflonide
- Fachinformation, Pulmicort
-
Fachinformation, Novopulmon
-
Entocort rektal 2,3 mg, Eurim Tabletten und Flüssigkeit zur Herstellung einer Rektalsuspension
Eurim-Pharm Arzneimittel GmbH
-
Entocort® rektal 2,3 mg, Tabletten und Flüssigkeit zur Herstellung einer Rektalsuspension
Tillotts Pharma GmbH
-
Intesticort 3 mg 2care4 magensaftresistente Hartkapseln
2care4 ApS
-
Intesticort 3 mg Abacus magensaftresistente Hartkapseln
Abacus Medicine A/S
-
Intesticort 3 mg axicorp B.V. magensaftresistente Hartkapseln
axicorp Pharma B.V.
-
Intesticort 3 mg CC Pharma magensaftresistente Hartkapseln
CC Pharma GmbH
-
Intesticort 3 mg Emra magensaftresistente Hartkapseln
Emra-Med Arzneimittel GmbH
-
Intesticort 3 mg Eurim magensaftresistente Hartkapseln
Eurim-Pharm Arzneimittel GmbH
-
Intesticort 3 mg kohlpharma magensaftresistente Hartkapseln
kohlpharma GmbH
-
Intesticort 3 mg Orifarm magensaftresistente Hartkapseln
Orifarm GmbH
-
Intestifalk 3 mg ACA magensaftresistente Hartkapseln
A.C.A. Müller ADAG Pharma AG
-
Intestifalk 3 mg docpharm magensaftresistente Hartkapseln
Docpharm GmbH
-
Intestifalk 3 mg Emra magensaftresistente Hartkapseln
Emra-Med Arzneimittel GmbH
-
Intestifalk 3 mg Eurim magensaftresistente Hartkapseln
Eurim-Pharm Arzneimittel GmbH
-
Intestifalk 3 mg kohlpharma magensaftresistente Hartkapseln
kohlpharma GmbH
-
Intestifalk 3 mg Mpa Pharma magensaftresistente Hartkapseln
Mpa Pharma GmbH
-
Intestifalk Emra Rektalschaum
Emra-Med Arzneimittel GmbH
-
Intestifalk kohlpharma Rektalschaum
kohlpharma GmbH
-
Intestifalk Uno 9 mg Abacus magensaftresistentes Granulat
Abacus Medicine A/S
-
Intestifalk Uno 9 mg Eurim magensaftresistentes Granulat
Eurim-Pharm Arzneimittel GmbH
-
Intestifalk Uno 9 mg kohlpharma magensaftresistentes Granulat
kohlpharma GmbH
-
Intestifalk Uno 9mg Emra magensaftresistentes Granulat
Emra-Med Arzneimittel GmbH
-
Jorveza 0,5 mg Ebb Medical Schmelztabletten
Ebb Medical Ab
-
Jorveza 0,5 mg kohlpharma Schmelztabletten
kohlpharma GmbH
-
Jorveza 0,5 mg Orifarm Schmelztabletten
Orifarm GmbH
-
Jorveza® 0,5 mg Schmelztabletten
Dr. Falk Pharma GmbH
-
Jorveza 1 mg Abacus Schmelztabletten
Abacus Medicine A/S
-
Jorveza 1 mg CC Pharma Schmelztabletten
CC Pharma GmbH
-
Jorveza 1 mg Emra Schmelztabletten
Emra-Med Arzneimittel GmbH
-
Jorveza 1 mg Eurim Schmelztabletten
Eurim-Pharm Arzneimittel GmbH
-
Jorveza 1 mg kohlpharma Schmelztabletten
kohlpharma GmbH
-
Jorveza 1 mg Orifarm Schmelztabletten
Orifarm GmbH
-
Jorveza® 1 mg Schmelztabletten
Dr. Falk Pharma GmbH
-
Kinpeygo 4 mg Aaragon Hartkapseln mit veränderter Wirkstofffreisetzung
Aaragon Pharma S.R.O.
-
Kinpeygo 4 mg Abacus Hartkapseln mit veränderter Wirkstofffreisetzung
Abacus Medicine A/S
-
Kinpeygo 4 mg Eurim Hartkapseln mit veränderter Wirkstofffreisetzung
Eurim-Pharm Arzneimittel GmbH
-
Kinpeygo® 4 mg Hartkapseln mit veränderter Wirkstofffreisetzung
STADAPHARM GmbH
-
Kinpeygo 4 mg kohlpharma Hartkapseln mit veränderter Wirkstofffreisetzung
kohlpharma GmbH
-
Kinpeygo 4 mg Medicopharm Hartkapseln mit veränderter Wirkstofffreisetzung
Medicopharm AG
-
Larbex® Steri-Neb® 0,5 mg/2 ml Suspension für einen Vernebler
Teva GmbH
-
Miflonide Breezhaler 200 Mikrogramm Emra Hartkapseln mit Pulver zur Inhalation
Emra-Med Arzneimittel GmbH
-
Miflonide® Breezhaler® 200 Mikrogramm Hartkapseln mit Pulver zur Inhalation
Novartis Pharma GmbH
-
Miflonide Breezhaler 400 Mikrogramm Emra Hartkapseln mit Pulver zur Inhalation
Emra-Med Arzneimittel GmbH
-
Miflonide Breezhaler 400 Mikrogramm Eurim Hartkapseln mit Pulver zur Inhalation
Eurim-Pharm Arzneimittel GmbH
-
Miflonide® Breezhaler® 400 Mikrogramm Hartkapseln mit Pulver zur Inhalation
Novartis Pharma GmbH
-
Novopulmon® 200 Mikrogramm Novolizer®
Viatris Healthcare GmbH
-
Novopulmon® 400 Mikrogramm Novolizer®
Viatris Healthcare GmbH
-
Pulmelia® 194 Mikrogramm/5,5 Mikrogramm einzeldosiertes Pulver zur Inhalation
ELPEN Pharmaceutical Co. Inc.
-
Pulmelia® 380 Mikrogramm/11 Mikrogramm einzeldosiertes Pulver zur Inhalation
ELPEN Pharmaceutical Co. Inc.
-
Pulmicort 0,5 mg/2 ml 1 4U Pharma Suspension für einen Vernebler
1 4 U Pharma GmbH














