Über Camzyos
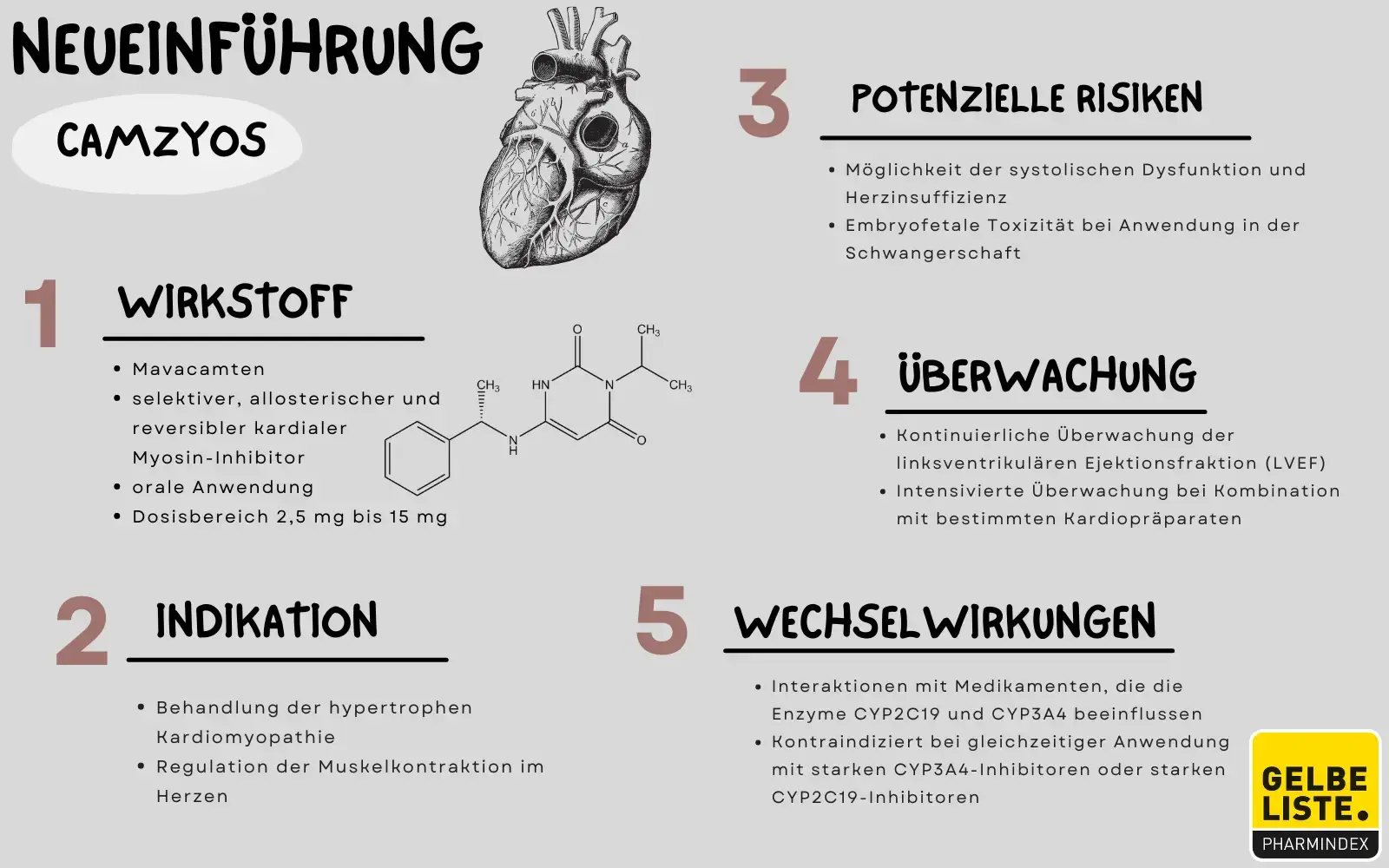
- Camzyos (Mavacamten) ist ein Myosin-Inhibitor, der die übermäßige Kontraktionsfähigkeit der Herzmuskelzellen bei Patienten mit obstruktiver hypertropher Kardiomyopathie direkt moduliert.
- Es wird oral eingenommen, wobei die empfohlene Anfangsdosis bei 2,5 mg täglich liegt und die Höchstdosis einmal täglich 5 mg beträgt.
Gegenanzeigen
- Überempfindlichkeit gegen Wirkstoff oder sonstige Bestandteile.
- Schwangerschaft und Frauen im gebärfähigen Alter ohne zuverlässige Empfängnisverhütung.
- Gleichzeitige Behandlung mit starken CYP3A4-Inhibitoren bei "angsamen CYP2C19-Metabolisierern und unbestimmtem CYP2C19-Phänotyp.
- Gleichzeitige Behandlung mit einer Kombination aus starkem CYP2C19-Inhibitor und starkem CYP3A4-Inhibitor.
Nebenwirkungen
Die häufigsten Nebenwirkungen sind Schwindel, Dyspnoe, systolische Dysfunktion und Synkope.
Wechselwirkungen
Wechselwirkungen sind möglich mit Medikamenten, die die Enzyme CYP2C19 und CYP3A4 beeinflussen.
Studienlage
- Die Zulassung von Camzyos basiert auf den Daten der Phase-III-Studien EXPLORER-HCM und VALOR-HCM, die beide positive Ergebnisse zeigten.
- EXPLORER-HCM-Studie: 251 Patienten mit symptomatischer obstruktiver HCM. 37% der mit Mavacamten Behandelten erreichten den primären Endpunkt (Verbesserung von pVO2 und NYHA-Klasse), verglichen mit 17% im Placeboarm.
- VALOR-HCM-Studie: 112 Patienten, die für eine septale Reduktionstherapie (SRT) in Frage kamen. 82% der mit Mavacamten behandelten Patienten waren nach 16 Wochen nicht länger für eine chirurgische Intervention geeignet. Im Vergleich, 17,9% der mit Camzyos Behandelten und 76,8% der Patienten im Placeboarm waren für eine SRT geeignet oder entschieden sich dafür.