Alirocumab
Alirocumab (Handelsname: Praluent, Hersteller: Sanofi-Aventis) hat von der EU-Kommission im September 2015 die Zulassung für die Behandlung von Erwachsenen mit erhöhten Cholesterinwerten (primäre Hypercholesterolämie und gemischte Dyslipidämie) erhalten. Das Medikament soll zusätzlich zu einer Ernährungsumstellung verordnet werden.
Alirocumab: Übersicht
Anwendung
Alirocumab (Handelsname: Praluent, Hersteller: Sanofi-Aventis) hat von der EU-Kommission im September 2015 die Zulassung für die Behandlung von Erwachsenen mit erhöhten Cholesterinwerten (primäre Hypercholesterolämie und gemischte Dyslipidämie) erhalten. Das Medikament soll zusätzlich zu einer Ernährungsumstellung verordnet werden.
Darüber hinaus ist der Antikörper angezeigt zur Reduktion des kardiovaskulären Risikos durch Verringerung der LDL-C-Werte bei Erwachsenen mit bestehender atherosklerotischer kardiovaskulärer
Erkrankung:
- in Kombination mit einer maximal verträglichen Statin-Therapie mit oder ohne andere lipidsenkende Therapieprinzipien oder
- als Monotherapie oder in Kombination mit anderen lipidsenkenden Therapieprinzipien bei Patienten mit einer Statin-Unverträglichkeit oder wenn Statine kontraindiziert sind
Anwendungsart
Alirocumab wird subkutan in Oberschenkel, Bauch oder Oberarm injiziert.
Wirkmechanismus
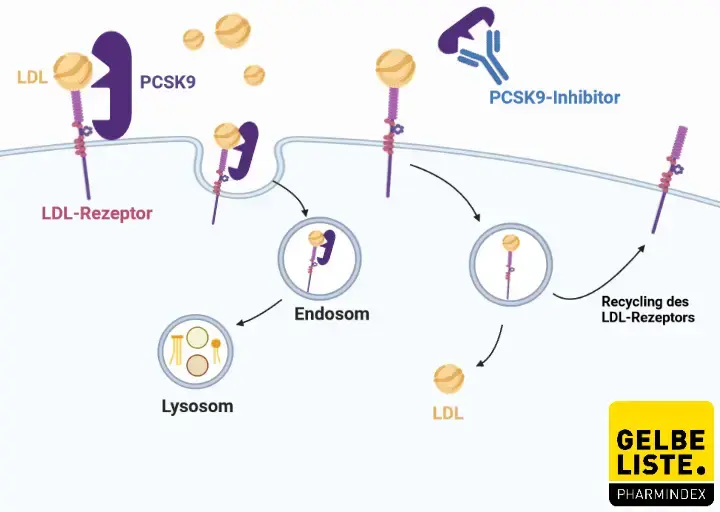
Alirocumab ist ein monoklonaler Antikörper aus der Wirkstoffgruppe der PCSK9-Inhibitoren (Proprotein-Convertase-Subtilisin/Kexin Typ 9). Das Enzym PCSK9 ist wesentlich daran beteiligt, dass LDL-Cholesterin und seine Rezeptoren auf der Oberfläche von Leberzellen abgebaut werden. Dadurch gelangt weniger LDL-Cholesterin in die Zellen.
Indem Alirocumab die Aktivität von PCSK9 blockiert, wird mehr LDL-Cholesterin in die Zellen aufgenommen und erhöhte Cholesterinwerte im Blut können sinken.
Alirocumab war 2015 der zweite PCSK9-Inhibitor, der in Europa zur Therapie der Hypercholesterinämie zugelassen wurde. Kurz zuvor war Evolocumab (Handelsname: Repatha, Hersteller: Amgen) auf den Markt gekommen.
Dosierung
Die empfohlene Anfangsdosis für Alirocumab beträgt 75 mg subkutan einmal alle zwei Wochen. Patienten, bei denen eine stärkere LDL-C-Senkung erforderlich ist (> 60%), können mit einer subkutanen Injektion von 150 mg alle zwei Wochen oder 300 mg alle vier Wochen (monatlich) beginnen.
Nebenwirkungen
Die häufigsten Nebenwirkungen von Alirocumab sind Schmerzen und Rötungen am Injektionsort, Infektionen der oberen Atemwege, Juckreiz (Pruritus), Kopfschmerzen, Gelenkschmerzen, Übelkeit, schmerzende Arme oder Beine und Müdigkeit.
Wechselwirkungen
Da es sich bei Alirocumab um ein biologisches Arzneimittel handelt, werden keine pharmakokinetischen Effekte von Alirocumab auf andere Arzneimittel und keine Wirkung auf das Cytochrom-P450-Enzymsystem erwartet.
Kontraindikation
Alirocumab darf bei Überempfindlichkeit gegen den Wirkstoff nicht angewendet werden.
Schwangerschaft
Die Anwendung von Alirocumab während der Schwangerschaft wird nicht empfohlen, es sei denn, der klinische Zustand der Mutter erfordert diese Behandlung.
Stillzeit
Da Auswirkungen von Alirocumab auf das gestillte Kindunbekannt sind, muss eine Entscheidung darüber getroffen werden, ob das Stillen oder die Behandlung mit Alirocumab zu unterbrechen ist.
Verkehrstüchtigkeit
Alirocumab hat keinen oder einen zu vernachlässigenden Einfluss auf die Verkehrstüchtigkeit und die Fähigkeit zum Bedienen von Maschinen.
- EMA: Fachinformation Praluent
- Rosenson, R. S., Hegele, R. A., Fazio, S., & Cannon, C. P. (2018). The evolving future of PCSK9 inhibitors. Journal of the American College of Cardiology, 72(3), 314-329.
Abbildung
Created with Biorender
-
Praluent® 75 mg Injektionslösung im Fertigpen
Sanofi-Aventis Deutschland GmbH
-
Praluent® 150 mg Injektionslösung im Fertigpen
Sanofi-Aventis Deutschland GmbH
-
Praluent 150 mg Orifarm Injektionslösung in einem Fertigpen
Orifarm GmbH
-
Praluent 300 mg Abacus Injektionslösung im Fertigpen
Abacus Medicine A/S
-
Praluent® 300 mg Injektionslösung im Fertigpen
Sanofi-Aventis Deutschland GmbH













