Anifrolumab
Anifrolumab ist der erste in Europa zugelassene Interferonrezeptor-Antikörper zur Behandlung von systemischem Lupus erythematodes (SLE).
Anifrolumab : Übersicht
Anwendung
Anifrolumab (Saphnelo) ist ein vollständig humaner, monoklonaler IgG1κ-Antikörper, der selektiv an den Typ‑I‑Interferon‑Rezeptor (IFNAR) bindet und dadurch die nachgeschaltete Signalübertragung sowie die Expression entzündungsfördernder Gene hemmt. Durch die Blockade dieses zentralen immunologischen Signalwegs werden überschießende Interferon‑Antworten reduziert, die eine wesentliche Rolle in der Pathogenese des systemischem Lupus erythematodes (SLE) spielen.
Anifrolumab ist zugelassen als Add‑on‑Therapie bei erwachsenen Patienten mit moderatem bis schwerem, aktivem, autoantikörper‑positivem SLE, die trotz Standardtherapie weiterhin eine aktive Krankheitsaktivität aufweisen.
Zur Standardbehandlung des SLE gehören vor allem die Basistherapie mit Hydroxychloroquin oder Chloroquin sowie – abhängig vom Organbefall – NSAR, Glukokortikoide und krankheitsmodifizierende Substanzen wie Methotrexat, Leflunomid , Belimumab oder bei schweren Organmanifestationen Cyclophosphamid, Rituximab oder hochdosierte systemische Steroide.
Anwendungsart
Neben der i.v.-Infusion (300 mg) ist Anifrolumab ab Februar 2026 auch als subkutane wöchentliche Fertigspritze/Fertigpen (120 mg) erhältlich.
Über SLE
Systemischer Lupus erythematodes (SLE) ist eine chronische und komplexe multisystemische Autoimmunerkrankung, die Gelenke, Nieren, Haut, Schleimhäute und die Wände der Blutgefäße betreffen kann. SLE kann durch eine Reihe von Symptomen gekennzeichnet sein, darunter Schmerzen, Hautausschläge, Müdigkeit, Schwellungen an den Gelenken und Fieber. Mehr als 50% der Patienten mit SLE entwickeln dauerhafte Organschäden, die durch die Krankheit oder bestehende Behandlungen verursacht werden, was die Symptome verschlimmert und das Mortalitätsrisiko erhöht.
Die Behandlung von SLE ist aufgrund begrenzter Wirksamkeiten und schlechten Verträglichkeit der bisherigen Standardtherapien eine Herausforderung. Die Aktivierung des Typ-I-Interferon (IFN)-Systems scheint der zentrale pathogene Mediator bei SLE zu sein. Die Zellsignalisierung durch alle Typ-I-IFNs, einschließlich IFNα, IFNβ, IFNɛ, IFNκ und IFNω, wird durch den Typ I IFN-α/β/ω-Rezeptor (IFNAR) vermittelt, was zu einer IFN-stimulierten Gentranskription führt.
Wirkmechanismus
Anifrolumab ist ein humaner monoklonaler IgG1‑κ‑Antikörper, der mit hoher Spezifität und Affinität an die Untereinheit 1 des Typ‑I‑Interferonrezeptors (IFNAR1) bindet.
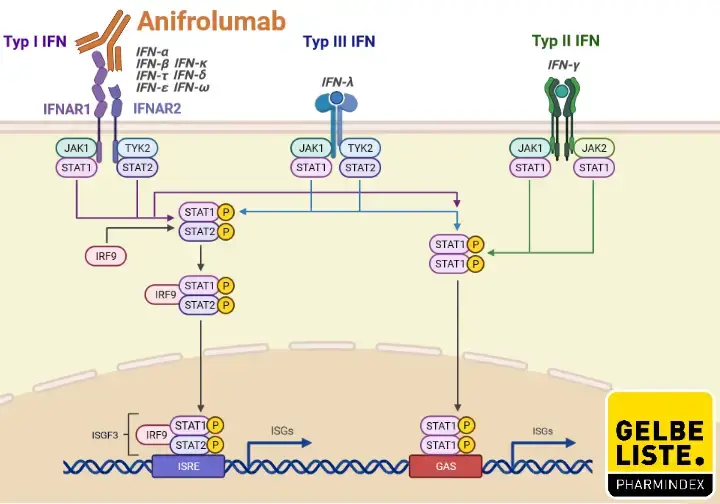
Normalerweise führt die Aktivierung von IFNAR1 und IFNAR2 zur Phosphorylierung der Signalproteine STAT1 und STAT2, die anschließend gemeinsam mit dem Interferon‑regulatorischen Faktor 9 (IRF9) in den Zellkern translozieren. Dort aktivieren sie das Interferon‑stimulated response element (ISRE), was die Expression zahlreicher entzündungsfördernder und immunmodulatorischer Gene auslöst und eine positive Rückkopplungsschleife verstärkt, die wiederum die Produktion weiterer Typ‑I‑Interferone fördert.
Durch die Bindung von Anifrolumab an IFNAR1 wird diese Typ‑I‑IFN‑Signaltransduktion gezielt blockiert. Zusätzlich führt Anifrolumab zur Internalisierung von IFNAR1, wodurch die Anzahl der Rezeptoren auf der Zelloberfläche weiter sinkt und weniger Bindungsstellen für Interferone zur Verfügung stehen.
Die Blockade der rezeptorvermittelten Typ‑I‑Interferon‑Signale hemmt die Expression interferon‑stimulierter Gene und damit nachgelagerte inflammatorische und immunologische Prozesse.
Dadurch wird unter anderem die Plasmazelldifferenzierung gehemmt und die Zusammensetzung peripherer T‑Zell‑Subpopulationen normalisiert. Insgesamt wird so das gestörte Gleichgewicht zwischen adaptiver und angeborener Immunität, das bei SLE charakteristischerweise fehlreguliert ist, wiederhergestellt.
Dosierung
Intravenös (i.v.):
- 300 mg alle 4 Wochen über 30 Minuten als Infusion
- Verwendung eines Infusionsschlauchs mit 0,2 bis 15 µm (In‑line‑ oder Add‑on‑)Filter mit geringer Proteinbindung; Nachspülen mit 25 ml 0,9 % NaCl.
- Infusionsgeschwindigkeit kann bei Reaktionen verlangsamt/unterbrochen werden.
- Verpasste i.v.‑Infusion möglichst bald nachholen, ≥ 14 Tage Mindestabstand zwischen Dosen.
Subkutan (s.c.):
- 120 mg 1× wöchentlich per Fertigspritze/Fertigpen (0,8 ml)
- Injektion in Oberschenkel/Abdomen (5‑cm‑Zone um den Nabel meiden; bei betreuter Anwendung auch Oberarm); Injektionsstellen rotieren (≥ 3 cm Abstand).
- Selbstinjektion nach Schulung möglich.
- Versäumte Dosis: sobald erinnert injizieren; neuen Wochenrhythmus starten oder am üblichen Tag fortsetzen (≥ 3 Tage Abstand einhalten).
Bei infusionsbedingten Reaktionen in der Anamnese kann vor der Infusion eine Prämedikation bestehend aus einem Antihistaminikum gegeben werden.
Wechsel zwischen intravenöser und subkutaner Anwendung
- i.v. → s.c.: erste s.c.-Injektion ca. 2 Wochen nach letzter i.v.-Dosis.
- s.c. → i.v.: erste i.v.-Infusion ca. 3–4 Wochen nach letzter s.c.-Dosis.
Aufbewahrung (s.c.)
- Lagerung im Kühlschrank (2–8 °C), nicht einfrieren oder schütteln, Lichtschutz beachten.
- Eine ungeöffnete Packung kann bis zu 7 Tage bei 20–25 °C gelagert werden.
- Vor Anwendung 60 Minuten bei Raumtemperatur liegen lassen.
Nebenwirkungen
Die am häufigsten berichteten Nebenwirkungen, die in den kontrollierten klinischen Studien mit Anifrolumab auftraten, waren:
- Infektionen der oberen Atemwege (31%)
- Bronchitis (10%)
- infusionsbedingte Reaktionen (9,4%), nur bei i.v.-Formulierung
- Herpes Zoster (6,1%)
Wechselwirkungen
Es wurden keine Studien zur Erfassung von Wechselwirkungen durchgeführt. Es ist aber nicht davon auszugehen, dass die Metabolisierung von Anifrolumab durch Leberenzyme oder die Ausscheidung über die Nieren erfolgt.
Bei einer chronischen Entzündung wird die Bildung einiger CYP450-Enzyme durch den Anstieg bestimmter Zytokine unterdrückt. Anifrolumab unterdrückt moderat die Spiegel einiger Zytokine. Die Auswirkungen auf die CYP450-Aktivität sind jedoch nicht bekannt.
Bei gleichzeitiger Anwendung von CYP-Substraten mit einer geringen therapeutischen Breite oder Wirkstoffen deren Dosis individuell angepasst wird (z. B. Warfarin), soll eine therapeutische Überwachung erfolgen.
Kontraindikationen
Anifrolumab darf nicht angewendet werden bei Überempfindlichkeit gegen den Wirkstoff oder einen der sonstigen Bestandteile des Arzneimittels.
Schwangerschaft
Bisher liegen nur sehr begrenzte Erfahrungen mit der Anwendung von Anifrolumab bei Schwangeren vor. Tierexperimentelle Studien sind nicht eindeutig in Bezug auf eine Reproduktionstoxizität. Die Anwendung von Anifrolumab während der Schwangerschaft und bei Frauen im gebärfähigen Alter, die nicht verhüten, wird deshalb nicht empfohlen, es sei denn der mögliche Nutzen rechtfertigt das potenzielle Risiko.
Stillzeit
Es ist nicht bekannt, ob Anifrolumab in die Muttermilch übergeht. Anifrolumab wurde in der Milch weiblicher Cynomolgus-Affen nachgewiesen. Da ein Risiko für das gestillte Kind kann nicht ausgeschlossen werden kann, muss eine Entscheidung darüber getroffen werden, ob das Stillen zu unterbrechen ist oder ob auf die Behandlung mit Anifrolumab verzichtet werden soll. Dabei soll sowohl der Nutzen des Stillens für das Kind als auch der Nutzen der Therapie für die Frau berücksichtigt werden.
Verkehrstüchtigkeit
Anifrolumab hat keinen oder einen zu vernachlässigenden Einfluss auf die Verkehrstüchtigkeit und die Fähigkeit zum Bedienen von Maschinen.
Anwendungshinweise
- Rückverfolgbarkeit: Zur Sicherstellung der Rückverfolgbarkeit biologischer Arzneimittel müssen Arzneimittelname und Chargennummer jeder verabreichten Anifrolumab‑Dosis eindeutig dokumentiert werden.
- Kombination mit anderen Biologika: Anifrolumab wurde nicht in Kombination mit anderen Biologika untersucht, einschließlich B‑Zell‑gerichteter Therapien.
→ Kombinationstherapien mit anderen Biologika werden nicht empfohlen. - Nicht untersuchte Patientengruppen: Schwerer aktiver Lupus des ZNS, schwere aktive Lupusnephritis. Für diese Gruppen liegen keine Wirksamkeits‑/Sicherheitsdaten vor.
- Überempfindlichkeitsreaktionen: Nach Gabe von Anifrolumab wurden schwere Überempfindlichkeitsreaktionen einschließlich Anaphylaxie beobachtet. In Studien traten sie bei 0,5–0,6 % der Patienten auf. Bei bestehender Allergie‑ oder Infusionsreaktions‑Anamnese kann eine Prämedikation (z. B. Antihistaminikum) sinnvoll sein. Bei Auftreten einer schweren Reaktion (z. B. Anaphylaxie) muss die Behandlung sofort abgebrochen und eine geeignete Therapie eingeleitet werden.
- Infektionsrisiko: Anifrolumab erhöht das Risiko für Atemwegsinfektionen sowie für Herpes Zoster; das Risiko ist bei gleichzeitiger Immunsuppression weiter erhöht. In Studien traten auch schwere bis tödliche Infektionen auf. Beginn einer Behandlung nicht, wenn eine aktive, klinisch relevante Infektion besteht. Vorsicht bei Patienten mit chronischen oder rezidivierenden Infektionen. Patienten sind anzuweisen, bei Infektionssymptomen sofort ärztliche Hilfe aufzusuchen. Bei Infektionen engmaschig überwachen; ggf. Therapie pausieren.
- Tuberkulose: Patienten mit unbehandelter latenter TBC sollen vor Therapiebeginn ggf. eine Anti‑TBC‑Behandlung erhalten. Anifrolumab darf nicht bei aktiver Tuberkulose angewendet werden.
- Impfen: Vor Therapiebeginn sollten alle empfohlenen Standardimpfungen abgeschlossen sein. Während der Behandlung dürfen Lebend‑ und attenuierte Lebendimpfstoffe nicht verabreicht werden.
- Malignome: Der Einfluss von Anifrolumab auf die Entwicklung von Malignomen ist unklar. In 52‑Wochen‑Studien wurden maligne Neoplasien bei 1,1 % der Anifrolumab‑Patienten und bei 0,5 % unter Placebo beobachtet. Bei bekannten Risikofaktoren sollte das Nutzen‑Risiko‑Verhältnis individuell geprüft werden. Bei neu auftretenden Malignomen ist die Fortsetzung der Therapie sorgfältig abzuwägen.
- Immunogenität: In den i.v.-Studien entwickelten 1,7 % der Patienten Anti‑Wirkstoff‑Antikörper (ADA). In der s.c.-Studie lag die ADA‑Rate bei 5,6 %; neutralisierende Antikörper wurden nicht nachgewiesen.
- EMA: Fachinformation Saphnelo, Stand: 18.12.2025.
- Furie R, Khamashta M, Merrill JT, et al. Anifrolumab, an Anti-Interferon-α Receptor Monoclonal Antibody, in Moderate-to-Severe Systemic Lupus Erythematosus. Arthritis Rheumatol. 2017;69(2):376-386. doi:10.1002/art.39962.
- BDI: Systemischer Lupus erythematodes: Wie wird der Systemische Lupus erythematodes behandelt?, abgerufen am 28.03.2022.
- AstraZeneca: Fachinformation Saphnelo® 120 mg Injektionslösung, Stand: Dezember 2025.
Abbildung
Adapted from „Interferon Pathway”, by BioRender.com.














