Avelumab
Avelumab ist ein monoklonaler Antikörper, der den PD-L1-Rezeptor blockiert und zur Behandlung von fortgeschrittenem Urothelkarzinom, Merkelzellkarzinom und in Kombination mit Axitinib für Nierenzellkarzinom zugelassen ist.
Avelumab: Übersicht
Anwendung
Avelumab (Bavencio) wird in der Onkologie für die Behandlung verschiedener Krebserkrankungen eingesetzt. Seine Hauptindikationen umfassen:
Metastasiertes Merkelzellkarzinom (MCC): Avelumab wird als Monotherapie bei Erwachsenen mit fortgeschrittenem Merkelzellkarzinom eingesetzt, einer seltenen und aggressiven Form von Hautkrebs.
Lokal fortgeschrittenes oder metastasiertes Urothelkarzinom (UC): Avelumab dient in der Erstlinien-Erhaltungstherapie nach einer platinbasierten Chemotherapie bei Erwachsenen, die unter dieser Behandlung keine Krankheitsprogression gezeigt haben.
Fortgeschrittenes Nierenzellkarzinom (RCC): In Kombination mit Axitinib wird Avelumab als Erstlinientherapie bei Erwachsenen mit fortgeschrittenem Nierenzellkarzinom angewendet.
Anwendungsart
- Bavencio wird nur als intravenöse Infusion verabreicht und darf nicht als intravenöse Druck- oder Bolusinjektion verwendet werden.
- Verdünnung: Mit Natriumchlorid 9 mg/ml (0,9%) oder 4,5 mg/ml (0,45%).
- Verabreichung: Über einen Zeitraum von 60 Minuten mit einem sterilen, nicht pyrogenen Inline- oder Zusatzfilter (Porengröße 0,2 Mikrometer).
Wirkmechanismus
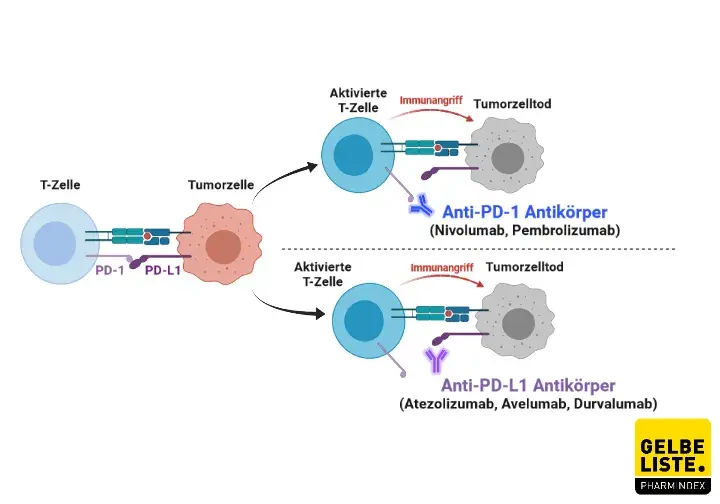
Avelumab bindet spezifisch an den PD-L1-Rezeptor auf Tumorzellen und blockiert dessen Interaktion mit dem PD-1-Rezeptor auf T-Zellen. Dadurch wird die durch Tumorzellen induzierte Immunsuppression aufgehoben, sodass die zytotoxischen T-Zellen Tumorzellen effizienter angreifen können. Zusätzlich kann Avelumab antikörperabhängige zelluläre Zytotoxizität (ADCC) induzieren, eine weitere immunvermittelte Zerstörung von Tumorzellen.
Pharmakokinetik
- Absorption: Intravenöse Gabe gewährleistet eine vollständige Bioverfügbarkeit.
- Verteilung: Avelumab verteilt sich überwiegend im extrazellulären Raum.
- Metabolisierung: Als monoklonaler Antikörper wird es durch proteolytische Prozesse in kleinere Peptide und Aminosäuren abgebaut.
- Halbwertszeit: 6 bis 10 Tage.
- Elimination: Primär über das retikuloendotheliale System; keine renale oder hepatische Ausscheidung.
Dosierung
Monotherapie
- Dosis: 800 mg alle 2 Wochen
- Verabreichung: Intravenös über einen Zeitraum von 60 Minuten
Kombinationstherapie mit Axitinib
- Avelumab: 800 mg alle 2 Wochen, intravenös über 60 Minuten
- Axitinib: 5 mg zweimal täglich, oral (alle 12 Stunden), unabhängig von den Mahlzeiten
Die Behandlung sollte fortgesetzt werden, bis entweder die Krankheitsprogression eintritt oder der Patient die Therapie nicht mehr verträgt.
Nebenwirkungen
Avelumab ist mit immunvermittelten Nebenwirkungen verbunden. Die meisten dieser Nebenwirkungen, auch schwerwiegende, konnten durch geeignete medizinische Maßnahmen oder das Absetzen des Medikaments behandelt werden.
Häufige Nebenwirkungen:
- Ermüdung (30,0%)
- Übelkeit (23,6%)
- Diarrhö (18,5%)
- Obstipation (18,1%)
- Verminderter Appetit (17,6%)
- Infusionsbedingte Reaktionen (15,9%)
- Erbrechen (15,6%)
- Gewichtsabnahme (14,5%)
Nebenwirkungen ≥ Grad 3:
- Anämie (5,6%)
- Hypertonie (3,9%)
- Hyponatriämie (3,6%)
- Dyspnoe (3,5%)
- Abdominalschmerzen (2,6%)
Schwerwiegende Nebenwirkungen:
- Immunvermittelte Nebenwirkungen
- Infusionsbedingte Reaktionen
Wechselwirkungen
Es wurden keine spezifischen Studien durchgeführt, um mögliche Wechselwirkungen von Avelumab mit anderen Arzneimitteln zu untersuchen. Da Avelumab hauptsächlich über katabole Stoffwechselprozesse abgebaut wird, ist es unwahrscheinlich, dass pharmakokinetische Wechselwirkungen mit anderen Medikamenten auftreten.
Kontraindikation
Avelumab darf nicht angewendet werden bei Überempfindlichkeit gegenüber dem Wirkstoff oder einem seiner Bestandteile.
Schwangerschaft
Es liegen nur begrenzte Erfahrungen zur Anwendung von Avelumab während der Schwangerschaft vor. Tierstudien zeigen, dass die Hemmung der PD-L1-Signalübertragung in trächtigen Mäusen zu erhöhter fötaler Verlustrate führt, was auf ein potenzielles Risiko für den Fötus hinweist. Da Avelumab ein humanes IgG1-Immunglobulin ist, könnte es die Plazenta passieren und den Fötus erreichen. Daher wird die Anwendung während der Schwangerschaft nicht empfohlen, es sei denn, sie ist aufgrund des klinischen Zustands der Mutter erforderlich.
Stillzeit
Es ist nicht bekannt, ob Avelumab in die Muttermilch übergeht. Da Antikörper in die Muttermilch gelangen können, besteht ein Risiko für das Neugeborene. Stillenden Frauen sollte geraten werden, während der Behandlung und mindestens einen Monat nach der letzten Dosis nicht zu stillen.
Verkehrstüchtigkeit
Avelumab hat keinen nennenswerten Einfluss auf die Verkehrstüchtigkeit oder die Fähigkeit, Maschinen zu bedienen. Es wurde jedoch von einigen Patienten über Ermüdung berichtet. Daher sollten Patienten vorsichtig sein, wenn sie ein Fahrzeug führen oder Maschinen bedienen, und dies nur tun, wenn sie sicher sind, dass Avelumab keine negativen Auswirkungen auf ihre Reaktionsfähigkeit hat.
Anwendungshinweise
Folgende Warnhinweise und Vorsichtsmaßnahmen sind bei der Anwendung von Avelumab zu beachten:
- Rückverfolgbarkeit:
Um die Rückverfolgbarkeit biologischer Arzneimittel zu verbessern, müssen die Bezeichnung des Arzneimittels und die Chargenbezeichnung des verwendeten Produkts eindeutig dokumentiert werden. - Infusionsbedingte Reaktionen:
Bei der Anwendung von Avelumab können infusionsbedingte Reaktionen auftreten, auch in schwerer Form. Zu den möglichen Symptomen gehören Fieber, Schüttelfrost, Hypotonie und Dyspnoe. Bei Reaktionen Grad 3 oder 4 muss die Infusion abgebrochen und Avelumab dauerhaft abgesetzt werden. Reaktionen Grad 1 oder 2 erfordern möglicherweise eine Anpassung der Infusionsgeschwindigkeit oder eine Unterbrechung der Infusion. - Immunvermittelte Nebenwirkungen:
Avelumab kann immunvermittelte Nebenwirkungen wie Pneumonitis, Hepatitis oder Kolitis verursachen, die in der Regel durch Absetzen von Avelumab und gegebenenfalls Kortikosteroiden behandelt werden können. Eine enge Überwachung und gegebenenfalls eine Therapieanpassung sind notwendig, insbesondere bei Patienten mit vorbestehenden Autoimmunerkrankungen. - Immunvermittelte Pneumonitis:
Bei Verdacht auf Pneumonitis sollte die Therapie unterbrochen und eine radiologische Bildgebung durchgeführt werden. Bei schwereren Fällen ist Avelumab dauerhaft abzusetzen und Kortikosteroide zu verabreichen. - Immunvermittelte Hepatitis:
Patienten müssen auf Veränderungen der Leberfunktion überwacht werden. Bei Grad 2 oder schwereren Leberfunktionsstörungen sollte die Therapie unterbrochen und gegebenenfalls mit Kortikosteroiden behandelt werden. - Immunvermittelte Kolitis:
Bei Auftreten von Kolitis-Symptomen sollte Avelumab unterbrochen werden, bis die Symptome abgeklungen sind. Bei schwereren Fällen kann Avelumab dauerhaft abgesetzt werden. - Immunvermittelte Pankreatitis:
Bei Anzeichen einer Pankreatitis muss Avelumab unterbrochen und gegebenenfalls mit Kortikosteroiden behandelt werden. Bei bestätigter Pankreatitis sollte Avelumab dauerhaft abgesetzt werden. - Immunvermittelte Myokarditis:
Verdacht auf Myokarditis erfordert eine sofortige Unterbrechung der Therapie. Bei Bestätigung der Diagnose muss Avelumab dauerhaft abgesetzt werden. - Immunvermittelte Endokrinopathien:
Schilddrüsen-, Nebennieren- oder Diabetes-Erkrankungen können auftreten. Patienten sollten auf entsprechende Symptome überwacht werden. Bei schwereren Fällen ist eine Therapieunterbrechung erforderlich. - Diabetes mellitus Typ 1:
Avelumab kann zu Diabetes mellitus Typ 1 führen. Patienten sollten auf Hyperglykämie und Symptome des Diabetes überwacht werden. Bei schwerer Hyperglykämie muss die Therapie mit Avelumab unterbrochen werden. - Immunvermittelte Nephritis und renale Dysfunktion:
Patienten müssen regelmäßig auf erhöhte Serumkreatinin-Werte überwacht werden. Bei einer Nephritis Grad 2 oder höher sollte Avelumab unterbrochen werden. - Andere immunvermittelte Nebenwirkungen:
Seltene, aber klinisch bedeutsame immunvermittelte Nebenwirkungen wie Myositis, Uveitis und Guillain-Barré-Syndrom können auftreten. Diese erfordern gegebenenfalls eine Therapieunterbrechung und Kortikosteroid-Gabe. - Hepatotoxizität (bei Kombination mit Axitinib):
Bei Kombination mit Axitinib können schwerere Leberfunktionsstörungen auftreten. Patienten sollten regelmäßig auf Leberwerte überwacht werden, insbesondere bei Erhöhungen von ALT und AST. - Von klinischen Studien ausgeschlossene Patienten:
Avelumab sollte mit Vorsicht bei Patienten mit aktiven metastatischen ZNS-Erkrankungen, aktiven Autoimmunerkrankungen, organtransplantierten Patienten oder solchen mit HIV, Hepatitis B oder C angewendet werden.
Alternativen
In Deutschland gibt es mehrere zugelassene Alternativen zu Avelumab:
Fortgeschrittenes Urothelkarzinom
- Pembrolizumab und Nivolumab (PD-1-Inhibitoren), die ebenfalls für die Behandlung von fortgeschrittenem oder metastasiertem Urothelkarzinom zugelassen sind. Merkelzellkarzinom
- Atezolizumab (PD-L1-Inhibitor): Ebenfalls zur Behandlung von fortgeschrittenem Urothelkarzinom nach Versagen der Chemotherapie zugelassen.
- Platinbasierte Chemotherapie (z.B. Cisplatin, Carboplatin): Standardtherapie in der Erstlinie bei fortgeschrittenem Urothelkarzinom, vor allem für Patienten, die für Immuntherapie nicht geeignet sind oder diese nicht ansprechen.
Kombination von Immuntherapie und Chemotherapie:
- Eine Kombination aus Immuncheckpoint-Inhibitoren (z.B. Pembrolizumab oder Atezolizumab) mit einer platinbasierten Chemotherapie (z.B. Cisplatin, Gemcitabin) stellt eine vielversprechende Behandlungsoption für Patienten mit fortgeschrittenem Urothelkarzinom dar.
Fortgeschrittenes Nierenzellkarzinom
- Eine Kombinationstherapie aus Nivolumab (PD-1-Inhibitor) und Ipilimumab (CTLA-4-Inhibitor) hat sich als besonders effektiv bei der Behandlung von fortgeschrittenem Nierenzellkarzinom erwiesen.
- Axitinib ist ein VEGF-Rezeptor-Inhibitor, der sowohl alleine als auch in Kombination mit Immuncheckpoint-Inhibitoren wie Pembrolizumab zur Behandlung von fortgeschrittenem Nierenzellkarzinom eingesetzt wird.
- Weitere zielgerichtete Therapien wie Sunitinib, Cabozantinib und Sorafenib, die auf spezifische Signalwege und die Angiogenese in Tumorzellen wirken, bieten ebenfalls eine sinnvolle Behandlungsoption für fortgeschrittenes Nierenzellkarzinom.
Merkelzellkarzinom
- Avelumab ist die einzige zugelassene Immuncheckpoint-Inhibitor-Therapie für das fortgeschrittene oder metastasierte Merkelzellkarzinom in Deutschland.
- Für Patienten, die nicht auf Immuntherapie ansprechen oder diese nicht erhalten können, kommen chemotherapeutische Behandlungen wie platinbasierte Chemotherapien (z.B. Cisplatin oder Carboplatin) in Frage.
Wirkstoff-Informationen
Fachinformation Bavencio
-
Bavencio 20 mg/ml CC Pharma Konzentrat zur Herstellung einer Infusionlösung, 10 ml
CC Pharma GmbH
-
Bavencio 20 mg/ml Eurim Konzentrat zur Herstellung einer Infusionlösung, 10 ml
Eurim-Pharm Arzneimittel GmbH
-
Bavencio 20 mg/ml Haemato-Pharm Konzentrat zur Herstellung einer Infusionlösung, 10 ml
HAEMATO PHARM GmbH
-
Bavencio 20 mg/ml kohlpharma Konzentrat zur Herstellung einer Infusionlösung, 10 ml
kohlpharma GmbH
-
Bavencio 20 mg/ml Konzentrat zur Herstellung einer Infusionlösung, 10 ml
Merck Serono GmbH
-
Bavencio 20 mg/ml Medicopharm Konzentrat zur Herstellung einer Infusionlösung, 10 ml
Medicopharm AG
-
Bavencio 20 mg/ml Orifarm Konzentrat zur Herstellung einer Infusionlösung, 10 ml
Orifarm GmbH
-
Bavencio 20 mg/ml Paranova Konzentrat zur Herstellung einer Infusionlösung, 10 ml
Paranova Pack A/S