Axitinib
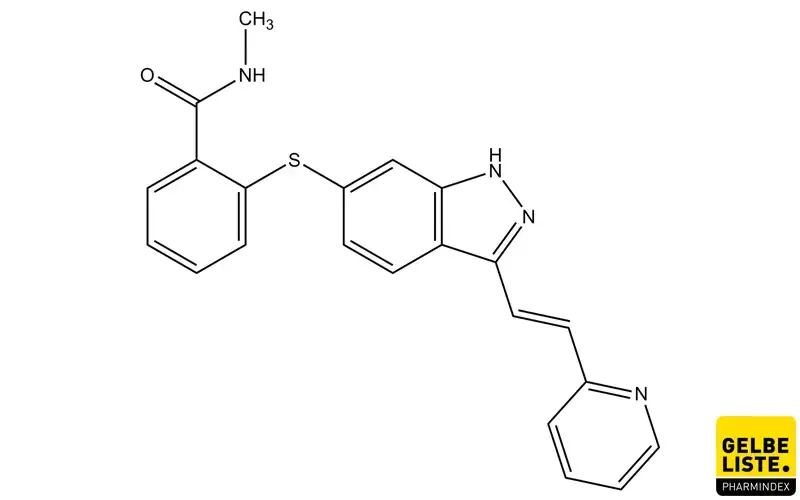
Axitinib ist ein Tyrosinkinase-Inhibitor, der VEGFR 1, 2, 3, PDGFR-alpha und -beta sowie c-kit hemmt. Der Wirkstoff wird angewendet zur Behandlung des fortgeschrittenen Nierenzellkarzinoms.
Axitinib: Übersicht
Anwendung
Axitinib (Inlyta) ist angezeigt zur Behandlung des fortgeschrittenen Nierenzellkarzinoms (renal cell cancer, RCC) bei erwachsenen Patienten nach Versagen von vorangegangener Therapie mit Sunitinib oder einem Zytokin.
Anwendungsart
Axitinib ist für die orale Anwendung bestimmt und sollte zweimal täglich im Abstand von etwa 12 Stunden zu oder unabhängig von den Mahlzeiten eingenommen werden.
Wirkmechanismus
Axitinib ist ein potenter und selektiver Inhibitor der zweiten Generation des Wachstumsfaktors Vascular Endothelial Growth Factor Receptor (VEGFR) 1, 2 und 3. Der Signalweg von VEGF/VEGF-Rezeptor-Tyrosinkinase (RTK) spielt eine entscheidende Rolle bei der Tumorangiogenese. Die Neovaskularisation fördert eine gesteigerte Proliferation, Überleben und Metastasierung von Tumorzellen.
Axitinib bindet in pikomolaren Konzentrationen an intrazelluläre Tyrosinkinase-Domänen von VEGFRs und blockiert nachgeschaltete Signalwege. Im Gegensatz zu Multitarget-Tyrosinkinase-Inhibitoren (z. B. Sorafenib, Sunitinib und Pazopanib) ist Axitinib selektiver gegen VEGFR-Tyrosinkinasen. Über diesen Mechanismus unterbindet der Wirkstoff das unkontrollierte Tumorwachstum und verhindert die Bildung von neuen Blutgefäßen im Tumor.
Pharmakokinetik
Resorption
- Nach einer 5-mg-Dosis Axitinib dauert es etwa 2,5 bis 4,1 Stunden, bis die maximale Plasmakonzentration erreicht ist.
Verteilung
- Das Verteilungsvolumen beträgt 160 l.
- Die Plasmaproteinbindung von Axitinib beträgt über 99%.
Metabolisierung
- Axitinib wird hauptsächlich hepatisch metabolisiert.
- CYP3A4 und CYP3A5 sind die wichtigsten hepatischen, CYP1A2, CYP2C19 und UGT1A1 sekundäre Enzyme bei der metabolisierung von Axitinib.
Elimination
- Axitinib wird hauptsächlich unverändert mit den Fäzes ausgeschieden (41%), wobei 12% der ursprünglichen Dosis als unverändertes Axitinib vorliegen.
- 23% werden renal eliminiert, hauptsächlich als Metaboliten.
- Die Halbwertszeit von Axitinib beträgt 2,5 bis 6,1 Stunden.
- Die durchschnittliche Clearance von Axitinib beträgt 38 l/h.
Nebenwirkungen
Nebenwirkungen, die bei über 20% der Patienten auftreten, sind unter anderem:
- Durchfall
- Fatigue
- Übelkeit, Erbrechen
- Hypertonie
- Erbrechen
- Appetitlosigkei, Gewichtsverlust
- Schilddrüsenunterfunktion
- Ausschlag
- Taubheitsgefühl an den Händen
- Husten
- Obstipation
Wechselwirkungen
Da Axitinib überwiegend durch CYP3A4/5 metabolisiert wird, sollte die gleichzeitige Anwendung starker CYP3A4/5-Hemmer (z. B. Ketoconazol, Itraconazol, Clarithromycin, Atazanavir, Indinavir, Nefazodon, Nelfinavir, Ritonavir, Saquinavir, Telithromycin und Voriconazol) vermieden werden. Wenn ein starker CYP3A4/5-Hemmer gleichzeitig verabreicht werden muss, wird empfohlen, ein alternatives Medikament ohne oder mit minimalem CYP3A4/5-Hemmungspotenzial auszuwählen oder die Anfangsdosis von Axitinib um etwa die Hälfte zu reduzieren.
Starke CYP3A4/5-Induktoren (z. B. Rifampicin, Dexamethason, Phenytoin, Carbamazepin, Rifabutin, Rifapentin, Phenobarbital und Johanniskraut) können die Plasmaexposition von Axitinib verringern und dadurch möglicherweise die Wirksamkeit beeinträchtigen, weshalb diese Medikamente nicht gleichzeitig mit Axitinib verabreicht weredn sollen.
Kontraindikationen
Die Anwendung von Axitinib ist kontraindiziert bei Patienten mit zuvor dokumentierter Überempfindlichkeit gegen den Wirkstoff.
Schwangerschaft
Es liegen keine Daten zur Anwendung von Axitinib an schwangeren Frauen vor. Basierend auf den pharmakologischen Eigenschaften von Axitinib kann dieses bei Anwendung an schwangere Frauen den Fötus schädigen. Tierexperimentelle Studien haben eine Reproduktionstoxizität gezeigt, einschließlich Missbildungen, weshalb Axitinib während der Schwangerschaft nicht angewendet werden soll, es sei denn, eine Behandlung ist aufgrund des klinischen Zustandes der Frau erforderlich.
Stillzeit
Es ist nicht bekannt, ob Axitinib in die Muttermilch übergeht. Da ein Risiko für das gestillte Kind nicht ausgeschlossen werden kann, soll Axitinib während der Stillzeit nicht angewendet werden.
Verkehrstüchtigkeit
Axitinib hat geringen Einfluss auf die Verkehrstüchtigkeit und die Fähigkeit zum Bedienen von Maschinen, weshalb Patienten darauf aufmerksam gemacht werden sollten, dass unter der Axitinib-Behandlung Beschwerden wie Schwindel und/ oder Müdigkeit auftreten können.
Anwendungshinweise
- Da in klinischen Studien mit Axitinib Herzinsuffizienz-Ereignisse (einschließlich Herzinsuffizienz, kongestive Herzinsuffizienz, kardiopulmonales Versagen, linksventrikuläre Dysfunktion, verringerte Auswurffraktion und Rechtsherzinsuffizienz) berichtet wurden, soll während der gesamten Behandlung mit Axitinib eine regelmäßige Überwachung im Hinblick auf Anzeichen oder Symptome einer Herzinsuffizienz stattfinden.
- Vor Einleitung einer Axitinib-Therapie sollte bei Patienten der Blutdruck gut eingestellt worden sein, da in klinischen Studien mit Axitinib Hypertonie sehr häufig berichtet wurde.
- Vor Beginn einer Axitinib-Behandlung und regelmäßig während der Therapie sollte die Schilddrüsenfunktion kontrolliert werden, da in klinischen Studien mit Axitinib Fälle von Hypothyreose und seltener auch von Hyperthyreose berichtet wurden.
- Bei Patienten mit einem Risiko für embolische und thrombotische Ereignisse oder mit derartigen Vorkommnissen in der Anamnese sollte Axitinib nur mit Vorsicht angewendet werden, da in klinischen Studien mit dem Wirkstoff arterielle embolische und thrombotische Ereignisse (einschließlich transitorische ischämische Attacke, Herzinfarkt, zerebrovaskuläres Ereignis und Verschluss der Retinaarterien) berichtet wurden.
- In klinischen Studien mit Axitinib wurde über venöse embolische und thrombotische Ereignisse (einschließlich Lungenembolie, tiefer Venenthrombose und Verschluss/ Thrombose der Retinavenen) berichtet. Bei Patienten mit einem Risiko für solche Ereignisse oder mit derartigen Vorkommnissen in der Vorgeschichte sollte Axitinib mit Vorsicht angewendet werden.
- Während der Behandlung mit Axitinib kann es zu einer Erhöhung des Hämoglobins oder Hämatokrits als Anzeichen einer Zunahme an Erythrozyten kommen, was das Risiko für embolische und thrombotische Ereignisse erhöhen kann. Aus diesem Grund soll vor Behandlungsbeginn und regelmäßig während der Therapie Hämoglobin und Hämatokrit kontrolliert werden.
- In klinischen Studien mit Axitinib wurde über hämorrhagische Ereignisse berichtet.
- Die Verwendung von VEGF-Signalweg-Hemmern kann die Entstehung von Aneurysmen und/oder Arteriendissektionen begünstigen. Vor Beginn der Behandlung mit sollte dieses Risiko bei Patienten mit Risikofaktoren wie Hypertonie oder Aneurysmen in der Vorgeschichte sorgfältig abgewogen werden.
- In klinischen Studien mit Axitinib wurde über gastrointestinale Perforation und Bildung von Fisteln berichtet.
- Die Behandlung mit Axitinib sollte mindestens 24 Stunden vor einer geplanten Operation gestoppt werden. Die Entscheidung zur Wiederaufnahme der Axitinib-Therapie sollte basierend auf der klinischen Beurteilung einer adäquaten Wundheilung getroffen werden.
- In klinischen Studien mit Axitinib wurde über posteriores reversibles Enzephalopathie-Syndrom (PRES) berichtet. PRES ist eine neurologische Erkrankung, bei der Kopfschmerzen, Krämpfe, Lethargie, Verwirrtheit, Blindheit und andere visuelle und neurologische Störungen auftreten können. Dabei kann leichte bis schwere Hypertonie auftreten.
- In klinischen Studien mit Axitinib wurde über Proteinurie, einschließlich der Schweregrade 3 und 4, berichtet. Vor Beginn einer Axitinib-Behandlung und regelmäßig während der Therapie werden Untersuchungen auf Proteinurie empfohlen.
- In einer kontrollierten klinischen Studie mit Axitinib wurde über leberassoziierte Nebenwirkungen berichtet. Zu den am häufigsten berichteten leberassoziierten Nebenwirkungen gehörten Anstiege der Alaninaminotransferase (ALT), der Aspartataminotransferase (AST) und des Bilirubins im Blut. Die Leberfunktion sollte deshalb vor Beginn einer Axitinib-Behandlung und regelmäßig während der Therapie kontrolliert werden.
- In einer klinischen Studie mit Axitinib war bei Probanden mit mäßiger Leberfunktionsstörung (Child-Pugh-Klasse B) die systemische Exposition etwa zweimal höher als bei Probanden mit normaler Leberfunktion. Bei Anwendung von Axitinib an Patienten mit mäßiger Leberfunktionsstörung (Child-Pugh-Klasse B) wird deshalb eine Dosisreduktion empfohlen.
Wirkstoff-Informationen
- EMA: Fachinformation Inlyta
- Yang, Lily PH, and Kate McKeage. "Axitinib." Drugs 72.18 (2012): 2375-2384.
- Chen, Ying, et al. "Clinical pharmacology of axitinib." Clinical pharmacokinetics 52.9 (2013): 713-725.
-
Axitinib Accord 1 mg Filmtabletten
Accord Healthcare GmbH
-
Axitinib Accord 3 mg Filmtabletten
Accord Healthcare GmbH
-
Axitinib Accord 5 mg Filmtabletten
Accord Healthcare GmbH
-
Axitinib AL 1 mg Filmtabletten
ALIUD PHARMA® GmbH
-
Axitinib AL 3 mg Filmtabletten
ALIUD PHARMA® GmbH
-
Axitinib AL 5 mg Filmtabletten
ALIUD PHARMA® GmbH
-
Axitinib AL 7 mg Filmtabletten
ALIUD PHARMA® GmbH
-
Axitinib HEXAL® 1 mg Filmtabletten
Hexal AG
-
Axitinib HEXAL® 3 mg Filmtabletten
Hexal AG
-
Axitinib HEXAL® 5 mg Filmtabletten
Hexal AG
-
Axitinib HEXAL® 7 mg Filmtabletten
Hexal AG
-
Axitinib-ratiopharm® 1 mg Filmtabletten
ratiopharm GmbH
-
Axitinib-ratiopharm® 3 mg Filmtabletten
ratiopharm GmbH
-
Axitinib-ratiopharm® 5 mg Filmtabletten
ratiopharm GmbH
-
Axitinib-ratiopharm® 7 mg Filmtabletten
ratiopharm GmbH
-
Axitinib STADA® 1 mg Filmtabletten
STADAPHARM GmbH
-
Axitinib STADA® 3 mg Filmtabletten
STADAPHARM GmbH
-
Axitinib STADA® 5 mg Filmtabletten
STADAPHARM GmbH
-
Axitinib STADA® 7 mg Filmtabletten
STADAPHARM GmbH
-
Inlyta® 1 mg Filmtabletten
Pfizer Pharma GmbH
-
Inlyta® 3 mg Filmtabletten
Pfizer Pharma GmbH
-
Inlyta® 5 mg Filmtabletten
Pfizer Pharma GmbH
-
Inlyta® 7 mg Filmtabletten
Pfizer Pharma GmbH












