Binimetinib
Binimetinib ist ein Benzimidazol, das als MEK1- und MEK2-Inhibitor wirkt und zur Behandlung von nicht-resezierbarem oder metastasiertem Melanom mit einer BRAF-V600-Mutation indiziert ist. Der Wirkstoff wird in Kombination mit dem BRAF-Kinase-Inhibitor Encorafenib verabreicht.
Binimetinib : Übersicht
Anwendung
Binimetinib (Mektovi) ist in Kombination mit Encorafenib angezeigt zur Behandlung von erwachsenen Patienten mit nicht-resezierbarem oder metastasiertem Melanom mit einer BRAF-V600-Mutation.
Anwendungsart
Binimetinib ist zum Einnehmen bestimmt. Die Tabletten können ann unabhängig von Mahlzeiten eingenommen werden und müssen als Ganzes zusammen mit Wasser geschluckt werden.
Wirkmechanismus
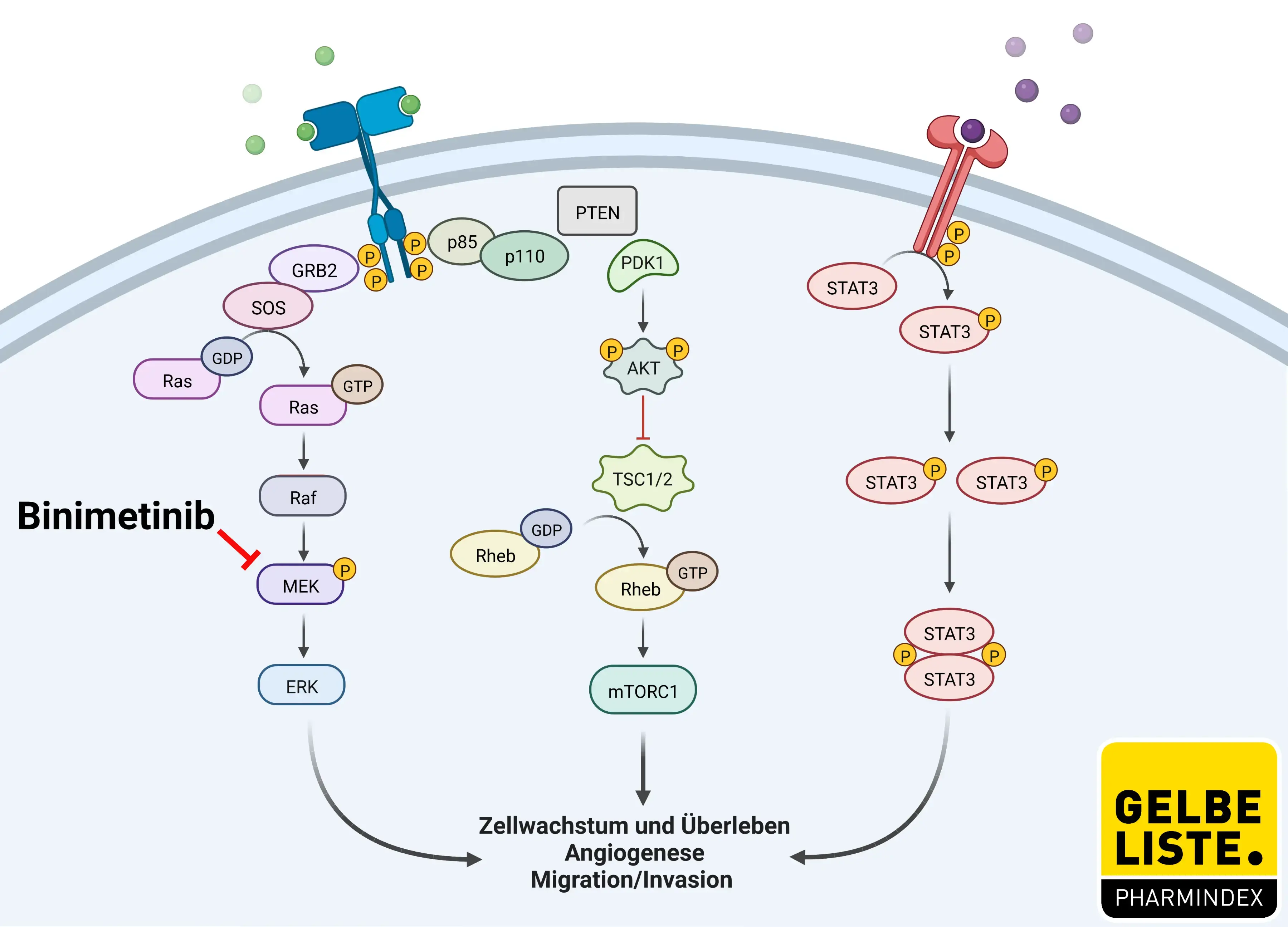
Binimetinib ist ein oral verfügbarer Inhibitor der mitogenaktivierten Proteinkinase-Kinase 1 und 2 (MEK1/2). Binimetinib, das nicht mit ATP konkurriert, bindet an MEK1/2 und hemmt dessen Aktivität. Die Hemmung von MEK1/2 verhindert die Aktivierung von MEK1/2-abhängigen Effektorproteinen und Transkriptionsfaktoren, was zu einer Hemmung der Wachstumsfaktor-vermittelten Zellsignalisierung führt. Dies kann schließlich zu einer Hemmung der Tumorzellproliferation und einer Hemmung der Produktion verschiedener entzündlicher Zytokine, einschließlich Interleukin-1, -6 und Tumornekrosefaktor, führen. MEK1/2 sind Threonin/Tyrosin-Kinasen mit doppelter Spezifität, die eine Schlüsselrolle bei der Aktivierung des RAS/RAF/MEK/ERK-Signalwegs spielen und häufig in einer Vielzahl von Tumorzelltypen hochreguliert werden.
Pharmakokinetik
Resorption
- Nach oraler Verabreichung wurden in einer pharmakokinetischen Studie mindestens 50% der Binimetinib-Dosis mit einer medianen Zeit bis zur maximalen Konzentration (Tmax) von 1,6 Stunden resorbiert.
- Die Verabreichung einer Einzeldosis von 45 mg zusammen mit einer fettreichen, kalorienreichen Mahlzeit hatte bei gesunden Probanden keine Auswirkung auf die Exposition gegenüber Binimetinib .
Verteilung
- Das scheinbare Verteilungsvolumen von Binimetinib beträgt 92 l (45%).
- Binimetinib wird zu 97% an menschliche Plasmaproteine gebunden und das Blut-zu-Plasma-Verhältnis beträgt 0,72.
Metabolisierung
- Der primäre Stoffwechselweg von Binimetinib ist die Glucuronidierung, wobei UGT1A1 mit bis zu 61% zum Metabolismus von Binimetinib beiträgt.
- Andere Stoffwechselwege von Binimetinib umfassen N-Dealkylierung, Amidhydrolyse und den Verlust von Ethandiol aus der Seitenkette.
- Der aktive Metabolit M3, der von CYP1A2 und CYP2C19 produziert wird, macht 8,6% der Binimetinib-Exposition aus.
- Nach einer oralen Einzeldosis von 45 mg radioaktiv markiertem Binimetinib waren etwa 60% der AUC der zirkulierenden Radioaktivität im Plasma auf Binimetinib zurückzuführen.
Elimination
- Nach einer oralen Einzeldosis von 45 mg radioaktiv markiertem Binimetinib bei gesunden Probanden wurden 62% (32% unverändert) der verabreichten Dosis im Stuhl und 31% (6,5% unverändert) im Urin wiedergefunden.
- Die mittlere (CV %) terminale Halbwertszeit (t1/2) von Binimetinib beträgt 3,5 Stunden (28,5%).
Dosierung
Die empfohlene Dosis von Binimetinib beträgt 45 mg zweimal täglich im Abstand von etwa 12 Stunden, entsprechend einer Gesamttagesdosis von 90 mg.
Nebenwirkungen
Die häufigsten Nebenwirkungen (≥25%) bei Patienten, die mit Encorafenib 300 mg in Kombination mit Binimetinib behandelt wurden, waren in klinischen Studien:
- Fatigue
- Übelkeit
- Diarrhoe
Wechselwirkungen
Folgende Wechselwirkungen müssen bei der Anwendung von Binimetinib beachtet werden:
- UGT1A1-Induktoren und -Inhibitoren: Binimetinib wird vorwiegend durch UGT1A1-vermittelte Glukuronidierung metabolisiert. Das Ausmaß von UGT1A1-vermittelten Wechselwirkungen mit Arzneimitteln ist wahrscheinlich klinisch nicht relevant; da dies jedoch nicht in einer formellen klinischen Studie untersucht wurde, sollten UGT1A1-Induktoren (z. B. Rifampicin und Phenobarbital) und -Inhibitoren (z. B. Indinavir, Atazanavir, Sorafenib) mit Vorsicht angewendet werden.
- Encorafenib: Obgleich Encorafenib ein relativ starker, reversibler Inhibitor von UGT1A1 ist, wurden bei Anwendung von Binimetinib und Encorafenib klinisch keine Unterschiede in der Binimetinib-Exposition festgestellt.
- Induktoren von CYP1A2-Enzymen (z. B. Carbamazepin und Rifampicin) und Induktoren des Pgp-Transportsystems (z. B. Johanniskraut oder Phenytoin) können die Binimetinib-Exposition verringern, was zu einer Abnahme der Wirksamkeit führen kann.
- Empfindliche Substrate von CYP1A2: Binimetinib ist ein potenzieller Induktor von CYP1A2; daher ist Vorsicht geboten, wenn es mit empfindlichen Substraten (z. B. Duloxetin oder Theophyllin) angewendet wird.
- EmpfindlicheSubstrate von OAT3: Binimetinib ist ein schwacher Inhibitor von OAT3; daher ist Vorsicht geboten, wenn es mit empfindlichen Substraten (z. B. Pravastatin oder Ciprofloxacin) verwendet wird.
Kontraindikationen
Binimetinib darf nicht bei Überempfindlichkeit gegen den Wirkstoff angewendet werden.
Schwangerschaft
Bisher liegen keine Erfahrungen mit der Anwendung von Binimetinib bei Schwangeren vor. Tierexperimentelle Studien haben eine Reproduktionstoxizität gezeigt. Binimetinib wird während der Schwangerschaft sowie bei gebärfähigen Frauen, die keine Kontrazeptiva anwenden, nicht empfohlen. Wenn Binimetinib während der Schwangerschaft angewendet wird oder die Patientin während der Behandlung mit Binimetinib schwanger wird, muss sie über die potentiellen Risiken für das ungeborene Kind aufgeklärt werden.
Stillzeit
Es ist nicht bekannt, ob Binimetinib oder seine Metabolite beim Menschen in die Muttermilch übergehen. Ein Risiko für Neugeborene/Säuglinge kann nicht ausgeschlossen werden. Es ist zu entscheiden, ob das Stillen beendet oder die Mektovi-Therapie abgesetzt wird. Dabei sind sowohl der Nutzen des Stillens für das Kind als auch der Nutzen der Therapie für die Mutter in Betracht zu
ziehen.
Verkehrstüchtigkeit
Binimetinib hat geringen Einfluss auf die Verkehrstüchtigkeit und die Fähigkeit zum Bedienen von Maschinen. In klinischen Studien sind bei Patienten unter Binimetinib Sehstörungen aufgetreten. Die
Patienten sollten darauf hingewiesen werden, keine Fahrzeuge zu lenken oder Maschinen zu bedienen, wenn bei ihnen Sehstörungen oder andere Nebenwirkungen auftreten, die ihre Verkehrstüchtigkeit und die Fähigkeit zum Bedienen von Maschinen beeinträchtigen können.
Anwendungshinweise
Patienten sollten darauf hingewiesen werden, bei folgenden Problemen unverzüglich einen Arzt zu kontaktieren:
- Symptome, die auf eine Störung der linksventrikulären Auswurffraktion hindeuten, zum Beispiel Schwindel, Dyspnoe, Palpitationen, Arrhythmie, Ödeme oder Fatigue
- Anzeichen einer Thromboembolie oder Lungenembolie: Brustschmerz, plötzliche Atembeschwerden/Kurzatmigkeit sowie blasse/kühle Haut an den Extremitäten
- Schwerwiegende Augenprobleme wie Augenschmerzen, eingeschränktes Gesichtsfeld, Verlust der Sehstärke, Halo-, Blitz- oder Fleckensehen
- Hinweise auf eine Rhabdomyolyse wie Myalgie, Muskelkrämpfe, Muskelsteifheit oder Muskelzucken, dunkler Urin
- Blutungsanzeichen wie Hämoptyse, Hämatemesis, Hämatochezie/Meläna, Hämaturie, Abdominalschmerzen oder vaginale Blutungen
- Neue dermatologische Befunde
- Symptome, die auf eine Pneumonitis/ILD hinweisen, beispielsweise Husten, Dyspnoe und andere Atembeschwerden.
Wirkstoff-Informationen
- Fachinformation Mektovi
- Shirley M. Encorafenib and Binimetinib: First Global Approvals. Drugs. 2018 Aug;78(12):1277-1284. doi: 10.1007/s40265-018-0963-x
Abbildung
Adapted from „ PI3K/Akt, RAS/MAPK, JAK/STAT Signaling”, by BioRender.com











