Capmatinib
Capmatinib ist ein MET-Inhibitor zur Behandlung von NSCLC-Patienten mit MET-Exon-14-skipping-Mutation. Eine MET-Dysregulation kann die Entwicklung und das Fortschreiten mehrerer Krebsarten fördern, darunter Lungen-, Leber-, Brust- und Eierstockkrebs.
Capmatinib: Übersicht
Anwendung
Capmatinib (Tabrecta) ist ein Inhibitor der MET-Rezeptor-Tyrosinkinase und wird als Monotherapie angewendet zur Behandlung von erwachsenen Patienten mit fortgeschrittenem nicht-kleinzelligen Bronchialkarzinom (non-small cell lung cancer, NSCLC) mit Veränderungen, die zu METex14-Skipping (Exon-14-Skipping im mesenchymal-epithelialen Transitionsfaktor-Gen) führen und die eine systemische Therapie nach einer Behandlung mit Immuntherapie und/oder Platin-basierter Chemotherapie benötigen.
Die MET-Exon-14-skipping-Mutation tritt bei ca. 3% der NSCLC Patienten auf und ist mit einer schlechteren Prognose assoziiert.
Anwendungsart
Tabrecta ist für die orale Einnahme in Form von Tabletten vorgesehen.
Wirkmechanismus
Niedermolekulare MET-Hemmer können in drei Typen eingeteilt werden; Typ I, II und III. Zu den Typ-I-Inhibitoren gehören Crizotinib (Typ Ia), Tepotinib und Capmatinib (Typ Ib). Sie blockieren die ATP-Bindung und verhindern so die Phosphorylierung und Aktivierung des Rezeptors. Ein Typ-II-Inhibitor ist Cabozantinib, der kompetitiv an eine hydrophobe Tasche neben der ATP-Bindungsstelle bindet. Typ-III-Hemmerwie Tivantinib binden eher an allosterische Stellen als an die ATP-Bindungsstelle.
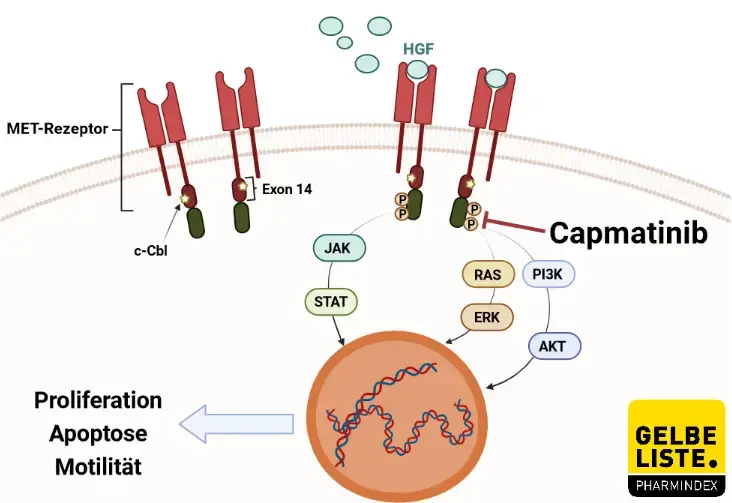
Nebenwirkungen
In der Phase-II-Studie GEOMETRY waren die häufigsten unerwünschten Ereignisse periphere Ödeme (52%), Übelkeit (44%), Müdigkeit (32%), Erbrechen (28%), Dyspnoe (24%) und verminderter Appetit (21%).
Dosisunterbrechungen aufgrund von Nebenwirkungen traten bei 54% der Patienten aufgrund peripherer Ödeme auf, erhöhtes Serumkreatinin, Übelkeit oder Erbrechen. Dosisreduktionen erfolgten bei 23% der Patienten aufgrund peripherer Ödeme, erhöhter Alaninaminotransferase (ALT), erhöhtem Serumkreatinin und Übelkeit
Wechselwirkungen
Capmatinib wird über CYP3A4-Enzyme und Aldehydoxidase metabolisiert, woraus sich Wechselwirkungen ergeben können. Vor der Anwendung sind deshalb folgende Interaktionen zu beachten:
- Starke CYP3A-Inhibitoren wie bspw. Clarithromycin, Indinavir, Itraconazol, Ketoconazol, Lopinavir, Ritonavir, Nefazodon, Nelfinavir, Posaconazol, Saquinavir, Telaprevir, Telithromycin, Verapamil und Voriconazol: engmaschige Überwachung auf Nebenwirkungen!
- Starke CYP3A-Induktoren wie Carbamazepin, Phenobarbital, Phenytoin, Rifampicin und Johanniskraut (Hypericum perforatum): Eine gemeinsame Anwendung sollte vermieden werden, da eine Verringerung der Capmatinib-Exposition die antitumorale Aktivität von Tabrecta herabsetzet.
- Bei einer gemeinsamen Anwendung mit moderaten CYP3A-Induktoren ist Vorsicht geboten.
- P-gp- oder BCRP-Substrate: Zunahme der Häufigkeit und Schwere von Nebenwirkungen dieser Substrate. Vorsicht ist geboten, wenn Tabrecta gemeinsam mit P-gp-Substraten (Digoxin, Dabigatranetexilat, Colchicin, Sitagliptin, Saxagliptin und Posaconazol) oder BCRP-Substraten (Methotrexat, Rosuvastatin, Pravastatin, Mitoxantron und Sulfasalazin) angewendet wird.
- P-gp- oder BCRP-Substrate mit geringer therapeutischer Breite: Verminderung der Dosis des gleichzeitig verabreichten Arzneimittels kann erforderlich sein.
Kontraindikationen
Capmatinib darf nicht angewendet werden bei Überempfindlichkeit gegen den Wirkstoff oder einen der sonstigen Bestandteile des Arzneimittels.
Schwangerschaft
Bisher liegen keine Erfahrungen mit der Anwendung von Capmatinib bei Schwangeren vor. Tierexperimentelle Studien haben eine Reproduktionstoxizität gezeigt. Basierend auf den Ergebnissen tierexperimenteller Studien und seinem Wirkmechanismus besteht der Verdacht, dass eine Anwendung von Capmatinib während der Schwangerschaft angeborene Fehlbildungen auslösen kann. Capmatinib darf während der Schwangerschaft nicht angewendet werden, es sei denn, eine Behandlung ist aufgrund des klinischen Zustandes der Frau erforderlich.
Stillzeit
Es ist nicht bekannt, ob Capmatinib oder seine Metaboliten in die Muttermilch übergehen. Ein Risiko für das gestillte Kind kann nicht ausgeschlossen werden. Aufgrund der Möglichkeit von schwerwiegenden Nebenwirkungen bei gestillten Kindern sollte das Stillen während der Behandlung mit Capmatinib und über mindestens 7 Tage nach der letzten Dosis unterbrochen werden.
Verkehrstüchtigkeit
Capmatinib hat keinen oder einen zu vernachlässigenden Einfluss auf die Verkehrstüchtigkeit und die Fähigkeit zum Bedienen von Maschinen.
Alternativen
Ein weiterer MET-Inhibitor zur Behandlung von NSCLC mit METex14-Skipping-Mutation ist Tepotinib (Tepmetko).
Wirkstoff-Informationen
- Wolf, Jürgen, et al. "Capmatinib in MET exon 14–mutated or MET-amplified non–small-cell lung cancer." New England Journal of Medicine 383.10 (2020): 944-957.
- Fachinformation Tabrecta
- Brazel D, Zhang S, Nagasaka M. Spotlight on Tepotinib and Capmatinib for Non-Small Cell Lung Cancer with MET Exon 14 Skipping Mutation. Lung Cancer (Auckl). 2022 May 13;13:33-45. doi: 10.2147/LCTT.S360574. PMID: 35592355; PMCID: PMC9113513
Abbildung
Created with Biorender.com











