Carmustin
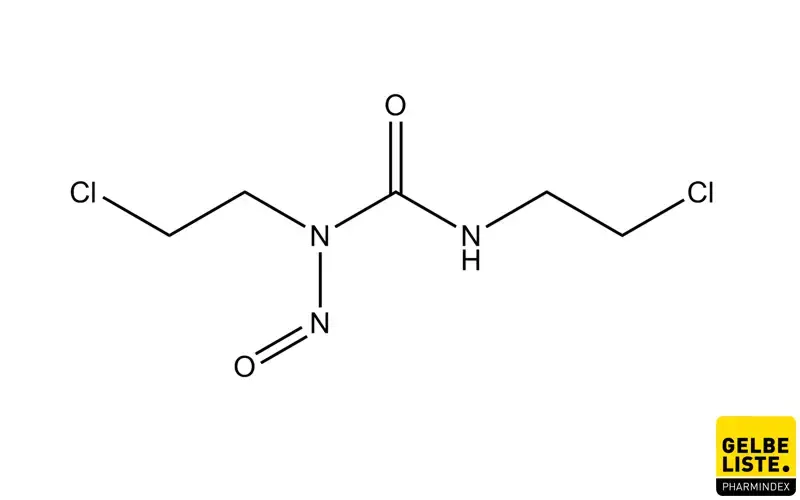
Carmustin ist ein Alkylierungsmittel und Nitrosoharnstoffderivat, das zur Behandlung von Hirntumoren, multiplem Myelom oder fortgeschrittenen Tumoren im Gastrointestinaltrakt angewendet wird.
Carmustin: Übersicht
Anwendung
Carmustin ist indiziert für die Behandlung von:
- Hirntumoren (Glioblastom, Hirnstammgliom, Medulloblastom, Astrozytom und Ependymom) und Hirnmetastasen
- Multiplem Myelom (in Kombination mit Glukokortikoiden wie z. B. Prednisolon)
- Morbus Hodgkin und Non-Hodgkin-Lymphom als Zweittherapie
- Fortgeschrittenen Tumoren im Gastrointestinaltrakt nach Versagen anderer Arzneimittel gegen Krebs
Wirkmechanismus
Als Alkylierungsmittel kann Carmustin Quervernetzungen zwischen den DNA-Strängen bilden, was die DNA-Replikation und DNA-Transkription verhindert.
Pharmakokinetik
Verteilung
- Intravenös verabreichtes Carmustin wird schnell abgebaut: nach 15 Minuten ist keine intakte Substanz mehr nachweisbar
- Aufgrund der guten Lipidlöslichkeit und der fehlenden Ionisation beim physiologischen pH-Wert passiert Carmustin sehr einfach die Blut-Hirn-Schranke
- Die Radioaktivität im Liquor ist um mindestens 50% höher als bei gleichzeitiger Messung im Plasma
- Die Kinetik von Carmustin beim Menschen wird durch ein Zwei-Kammer-Modell charakterisiert
- Nach einer einstündigen, intravenösen Infusion sinkt der Carmustin-Plasma-Spiegel biphasisch
- Die Halbwertszeit α beträgt 1–4 Minuten und die Halbwertszeit β 18–69 Minuten
Biotransformation
- Es wird angenommen, dass die antineoplastische und toxische Wirkung von Carmustin durch dessen Metabolite verursacht werden
Elimination
- Ungefähr 60–70 % der Gesamtdosis werden in Form von Metaboliten über einen Zeitraum von 96 Stunden in den Urin ausgeschieden und ca. 10% als CO2
- Über den Verbleib der Restmenge von 20–30% gibt es keine gesicherten Angaben
Dosierung
Die empfohlene Dosis beträgt 150 bis 200 mg/m2 Körperfläche intravenös alle 6 Wochen. Diese kann als Einzeldosis verabreicht oder aufgeteilt in tägliche Infusionen von z. B. 75 bis 100 mg/m2 an zwei aufeinander folgenden Tagen aufgeteilt werden.
Nebenwirkungen
Sehr häufige Nebenwirkungen (≥ 1/10) von Carmustin sind:
- Myelosuppression, Thrombozytopenie, Blutungen
- Ataxie, Schwindel, Kopfschmerzen
- Augentoxizität, vorübergehende Bindehautrötung und verschwommenes Sehen durch Netzhautblutungen
- Hypotonie, bedingt durch den Alkoholgehalt des Lösungsmittels (Hochdosis-Therapie)
- Venenentzündung
- Lungentoxizität, interstitielle Fibrose (bei verlängerter Therapie und kumulativer Dosis), Pneumonitis
- Übelkeit und Erbrechen (schwerwiegend)
- Dermatitis bei topischer Anwendung, die sich mit verminderter Konzentration des zusammengesetzten Produktes verbessert, Hyperpigmentierung (vorübergehend) bei versehentlichem Hautkontakt
Wechselwirkungen
Mit folgenden Verbindungen kann es bei der Anwendung von Carmustin zu Wechselwirkungen kommen:
- Phenytoin und Dexamethason: Verminderte Aktivität von Antiepileptika möglich
- Cimetidin: Verzögerte, erhöhte toxische Wirkung von Carmustin (aufgrund der Hemmung des Carmustin-Stoffwechsels) möglich
- Digoxin: Verzögerte, verminderte Wirkung von Digoxin (aufgrund der verminderten Digoxin-Resorption)
- Melphalan: Erhöhtes Risiko für eine Lungentoxizität
Kontraindikationen
Carmustin darf nicht angewendet werden bei:
- Überempfindlichkeit gegen den Wirkstoff oder andere Nitrosoharnstoffe
- Schwerer Knochenmarksdepression
- Schwerer Nierenfunktionsstörung
- Frauen, die stillen
- Kindern und Jugendlichen
Schwangerschaft
Carmustin darf in der Schwangerschaft nicht angewendet werden. Carmustin ist im humantherapeutischen Dosisbereich bei Ratten und Kaninchen embryotoxisch und bei Ratten teratogen. Wenn Carmustin während der Schwangerschaft angewendet wird, oder wenn die Patientin während der Behandlung mit Carmustin schwanger wird, sollte sie über das potenzielle Risiko für den Fetus aufgeklärt werden.
Stillzeit
Es ist nicht bekannt, ob Carmustin/Metabolite in die Muttermilch übergehen. Da ein Risiko für das Neugeborene bzw. den Säugling nicht ausgeschlossen werden kann, ist Carmustin während der Stillzeit und bis zu sieben Tagen nach der Behandlung kontraindiziert.
Verkehrstüchtigkeit
Carmustin hat keinen oder einen zu vernachlässigenden Einfluss auf die Verkehrstüchtigkeit und die Fähigkeit zum Bedienen von Maschinen.
Wirkstoff-Informationen
- Fachinformation Carmustin-ratiopharm
- Steinhilber, Schubert, Zsilavecz, Roth; Medizinische Chemie 2. Auflage 2010
- Mutschler Mutschler Arzneimittelwirkungen, Pharmakologie – Klinische Pharmakologie – Toxikologie, Begründet von Ernst Mutschler, 11. Auflage 2020, Wissenschaftliche Verlagsgesellschaft Stuttgart
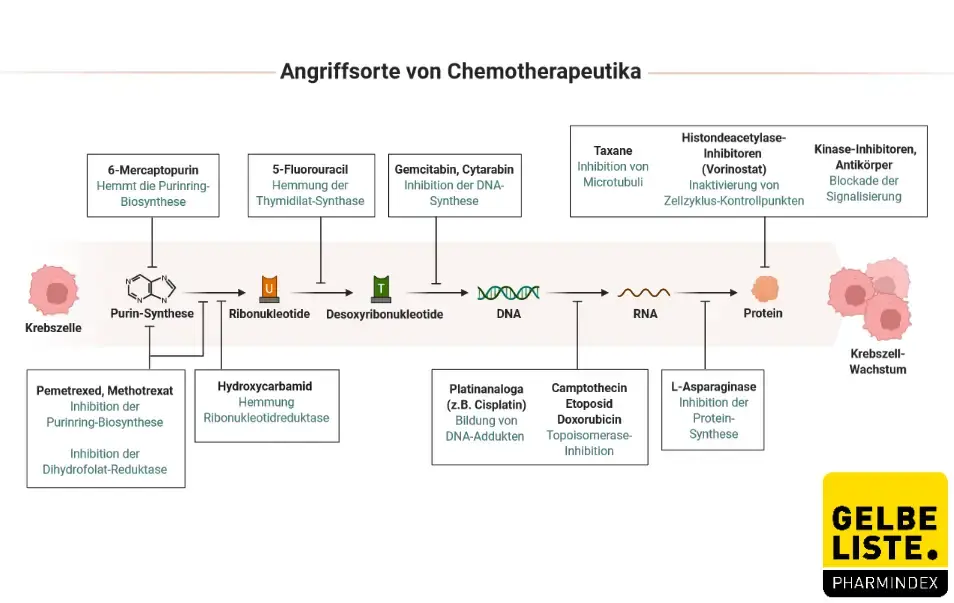
Abbildung
Adapted from „Basic Methods of Chemotherapy”, by BioRender.com
-
Carmubris® Pulver und Lösungsmittel zur Herstellung einer Infusionslösung
Zentiva Pharma GmbH
-
Carmustin Accord 100 mg Pulver und Lösungsmittel für ein Konzentrat zur Herstellung einer Infusionslösung
Accord Healthcare GmbH
-
Carmustin Accordpharma 300 mg Pulver und Lösungsmittel für ein Konzentrat zur Herstellung einer Infusionslösung
Accord Healthcare GmbH
-
Carmustin Glenmark 100 mg Pulver und Lösungsmittel für ein Konzentrat zur Herstellung einer Infusionslösung
Glenmark Arzneimittel GmbH
-
Carmustin medac 100 mg Pulver und Lösungsmittel zur Herstellung eines Konzentrates für eine Infusionslösung
medac Gesellschaft für klinische Spezialpräparate mbH
-
Carmustin-ratiopharm 100 mg Pulver und Lösungsmittel für ein Konzentrat zur Herstellung einer Infusionslösung
ratiopharm GmbH
-
Carmustin STADA® 100 mg Pulver und Lösungsmittel für ein Konzentrat zur Herstellung eine Infusionslösung
STADAPHARM GmbH
-
Carmustin Waymade 100 mg Pulver und Lösungsmittel für ein Konzentrat zur Herstellung einer Infusionslösung
Waymade B.V.
-
GLIADEL 7,7 mg Implantate
Clinigen Healthcare B.V.











