Cladribin
Cladribin ist ein Nukleosid-Analogon des Desoxyadenosins und wirkt immunsuppressiv. Der Wirkstoff wird bei Erwachsenen mit hochaktiver schubförmiger Multipler Sklerose (MS) angewendet.
Cladribin: Übersicht

Anwendung
Cladribin wird angewendet zur Behandlung von erwachsenen Patienten mit hochaktiver schubförmiger Multipler Sklerose (MS).
Wirkmechanismus
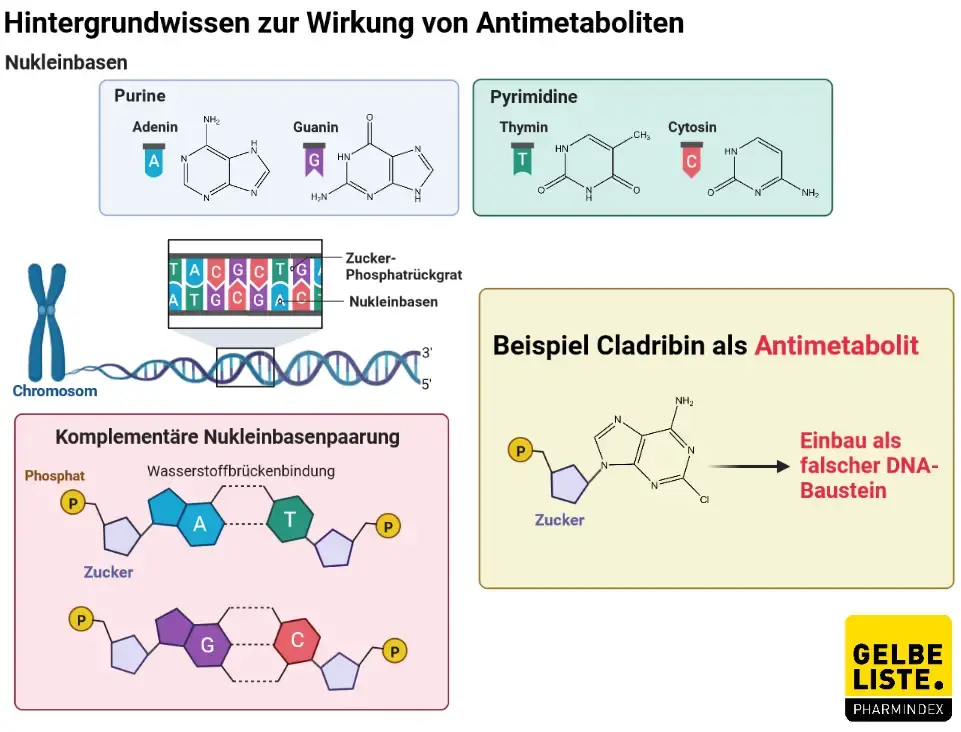
Cladribin (2-Chlordesoxyadenosin) ist ein synthetisches chloriertes Desoxyadenosin-Analogon, das in ausgewählten Zelltypen biologisch aktiv ist und eine gezielte und anhaltende Reduktion von zirkulierenden T- und B-Lymphozyten bewirkt, die an der Pathogenese von MS beteiligt sind. Die biologische Aktivität von Cladribin hängt von der bevorzugten Akkumulation von Cladribinphosphaten in Zelltypen mit einem hohen intrazellulären Verhältnis von Desoxycytidinkinase zu 5'-Nukleotidasen ab. Cladribin-Phosphate stören die DNA-Synthese und -Reparatur durch Einbau in die DNA und durch Hemmung von Enzymen, die am DNA-Metabolismus beteiligt sind, einschließlich DNA-Polymerase und Ribonukleotid-Reduktase. Dies wiederum führt zu DNA-Strangbrüchen und schließlich zum Zelltod.
Dosierung
- Die empfohlene kumulative Dosis beträgt 3,5 mg/kg Körpergewicht über zwei Jahre, angewendet als eine Behandlungsphase von 1,75 mg/kg pro Jahr.
- Jede Behandlungsphase besteht aus zwei Behandlungswochen, eine zu Beginn des ersten Monats und eine zu Beginn des zweiten Monats des jeweiligen Behandlungsjahres.
- Die Behandlungsphase in Jahr zwei kann bei medizinischer Notwendigkeit (z. B. damit sich die Lymphozytenzahl erholen kann) um bis zu sechs Monate verschoben werden.
- Jede Behandlungswoche besteht aus vier oder fünf Tagen, an denen ein Patient abhängig vom Körpergewicht 10 mg oder 20 mg als tägliche Einmaldosis erhält.
- Nach Abschluss der zwei Behandlungsphasen ist keine weitere Behandlung mit Cladribin in den Jahren drei und vier erforderlich.
Nebenwirkungen
Die klinisch relevantesten Nebenwirkungen von Cladribin sind Lymphopenie (25,6%) und Herpes Zoster (3,0%). Sehr häufig (≥1/10) führt die Anwendung zu einer Lymphopenie.
Wechselwirkungen
Folgende Wechselwirkungen sind bei der Anwendung von Cladribin zu beachten:
- Immunsuppressive Arzneimittel: Aufgrund des Risikos additiver Wirkungen auf das Immunsystem ist der Beginn einer Behandlung mit Cladribin bei immungeschwächten Patienten kontraindiziert, einschließlich Patienten, die derzeit eine immunsuppressive oder myelosuppressive Therapie mit Wirkstoffen wie Methotrexat, Cyclophosphamid, Ciclosporin oder Azathioprin erhalten, sowie bei Patienten unter chronischer Behandlung mit Kortikosteroiden ➝ Eine akute Kurzzeitbehandlung mit systemischen Kortikosteroiden ist während der Behandlung möglich.
- Andere krankheitsmodifizierende Arzneimittel: Die Anwendung von Cladribin zusammen mit Interferon beta führt zu einem erhöhten Risiko einer Lymphopenie. Die Sicherheit und Wirksamkeit von Cladribin in Kombination mit anderen krankheitsmodifizierenden MS-Therapien ist nicht erwiesen. Eine gleichzeitige Behandlung wird deshalb nicht empfohlen.
- Hämatotoxische Arzneimittel: Wegen der Cladribin-induzierten Verminderung der Lymphozytenzahl ist mit additiven hämatologischen Nebenwirkungen zu rechnen, wenn Cladribin vor oder gleichzeitig mit anderen Wirkstoffen angewendet wird, die das hämatologische Profil beeinflussen (z. B. Carbamazepin). In solchen Fällen wird eine sorgfältige Kontrolle der hämatologischen Parameter empfohlen.
- Lebendimpfstoffe und abgeschwächte Lebendimpfstoffe: Eine Behandlung sollte wegen des Risikos einer aktiven Impfinfektion frühestens vier bis sechs Wochen nach einer Impfung mit Lebendimpfstoffen oder abgeschwächten Lebendimpfstoffen begonnen werden.
- Starke Inhibitoren von BCRP-Transportern: Hinsichtlich der Resorption von Cladribin scheint die einzig denkbare, klinisch relevante Wechselwirkungsmöglichkeit über das Brustkrebs-Resistenz-Protein (BCRP oder ABCG2) zu bestehen. Die Hemmung von BCRP im Gastrointestinaltrakt erhöht möglicherweise die orale Bioverfügbarkeit von Cladribin und die systemische Exposition. Zu den bekannten BCRP-Inhibitoren, die die Pharmakokinetik von BCRP-Substraten in vivo um 20% verändern, gehört unter anderem Eltrombopag.
- Inhibitoren von ENT1- und CNT3-Transportern wie Dilazep, Nifedipin, Nimodipin, Cilostazol, Sulindac oder Reserpin: In-vitro-Studien deuten darauf hin, dass Cladribin ein Substrat der equilibrativen Nukleosid(ENT1)-und konzentrativen Nukleosid(CNT3)-Transporterproteine ist. Daher können die Bioverfügbarkeit, intrazelluläre Verteilung und renale Elimination von Cladribin theoretisch durch starke Inhibitoren dieser Transporter verändert werden.
- Starke Induktoren von BCRP- und P-gp-Transportern: Bei gleichzeitiger Anwendung starker Induktoren der BCRP-Transporter (z. B. Kortikosteroide) oder P-gp-Transporter (z. B. Rifampicin, Johanniskraut) ist eine mögliche Verringerung der Cladribin-Exposition in Betracht zu ziehen.
- Hormonelle Kontrazeptiva: Bisher ist nicht bekannt, ob Cladribin möglicherweise die Wirksamkeit systemisch wirkender hormoneller Kontrazeptiva vermindert. Daher sollten Frauen, die systemisch wirkende hormonelle Kontrazeptiva anwenden, während der Behandlung mit Cladribin sowie für mindestens vier Wochen nach der letzten Dosis eines jeden Behandlungsjahres zusätzlich eine Barrieremethode anwenden.
Kontraindikationen
Bei der Anwendung von Cladribin sind folgende Gegenanzeigen zu beachten:
- Überempfindlichkeit gegen den Wirkstoff
- Infektion mit dem Humanen Immundefizienz-Virus (HIV)
- Aktive chronische Infektion (Tuberkulose oder Hepatitis)
- Immungeschwächten Patienten, einschließlich Patienten, die derzeit eine immunsuppressive oder myelosuppressive Therapie erhalten
- Aktive maligne Erkrankungen
- Mittelschwere oder schwere Einschränkung der Nierenfunktion (Kreatinin-Clearance <60 ml/min)
- Schwangerschaft und Stillzeit
Schwangerschaft
Es ist davon auszugehen, dass Cladribin angeborene Fehlbildungen verursachen kann, wenn es während derSchwangerschaft angewendet wird. Tierexperimentelle Studien haben eine Reproduktionstoxizität gezeigt. Cladribin ist deshalb bei Schwangeren kontraindiziert.
Stillzeit
Es ist nicht bekannt, ob Cladribin in die Muttermilch übergeht. Im Hinblick auf das Potenzial schwerwiegender unerwünschter Wirkungen bei gestillten Kindern ist während der Behandlung mit
und für eine Woche nach der letzten Dosis das Stillen kontraindiziert.
Verkehrstüchtigkeit
Cladribin hat keinen oder einen zu vernachlässigenden Einfluss auf die Verkehrstüchtigkeit und die Fähigkeit zum Bedienen von Maschinen.
Wirkstoff-Informationen
- EMA: Fachinformation Mavenclad
- Leist TP, Weissert R. Cladribine: mode of action and implications for treatment of multiple sclerosis. Clin Neuropharmacol. 2011 Jan-Feb;34(1):28-35. doi: 10.1097/WNF.0b013e318204cd90
- Mutschler Mutschler Arzneimittelwirkungen, Pharmakologie – Klinische Pharmakologie – Toxikologie, Begründet von Ernst Mutschler, 11. Auflage 2020, Wissenschaftliche Verlagsgesellschaft Stuttgart
Abbildung
Created with Biorender
-
Leustatin 10 mg/10 ml Konzentrat zur Herstellung einer Infusionslösung
Pharmanovia A/S (Athnahs Pharma Nordics A/S)
-
Litak 2 mg/ml Injektionslösung
Lipomed GmbH
-
Litak 2 mg/ml Orifarm Injektionslösung
Orifarm GmbH
-
Mavenclad 10 mg kohlpharma Tabletten
kohlpharma GmbH
-
MAVENCLAD 10 mg Tabletten
Merck Serono GmbH