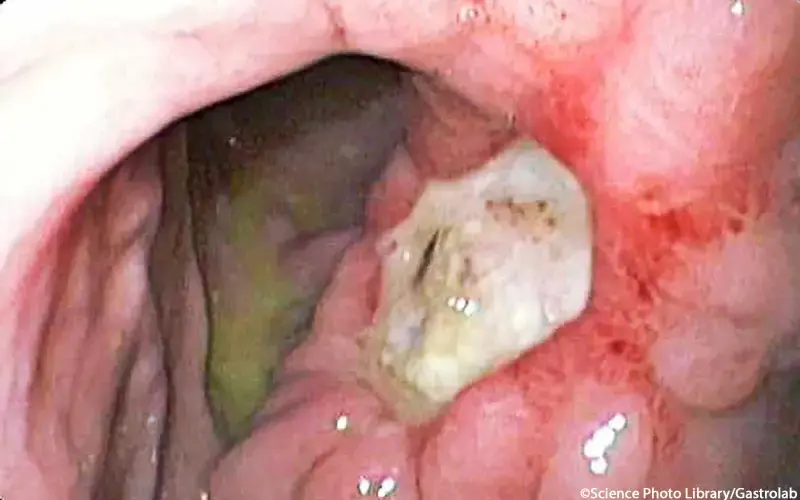
Durvalumab
Durvalumab, ein monoklonaler Antikörper, wird in der Krebstherapie eingesetzt und bindet an PD-L1 exprimierende Zellen, wodurch diese eliminiert werden. Er wird in Kombination mit anderen Therapien oder als Monotherapie gegen verschiedene Krebsarten eingesetzt.
Durvalumab: Übersicht
Anwendung
Der Wirkstoff Durvalumab ist ein monoklonaler Antikörper, der zur Therapie verschiedener Krebsarten zugelassen ist. Das Immuntherapeutikum bindet an Krebszellen, die das PD-L1 Oberflächenprotein exprimieren und ermöglicht so die Elimination durch körpereigene Immunzellen.
Das Anwendungsgebiet von Durvalumab umfasst folgende Indikationen:
- Nicht-kleinzelliges Lungenkarzinom (NSCLC): Als Monotherapie für lokal fortgeschrittene, inoperable Fälle mit PD-L1-Expression ≥1% nach platinbasierter Radiochemotherapie ohne Krankheitsprogression. Zudem in Kombination mit Tremelimumab und platinbasierter Chemotherapie für die Erstbehandlung von metastasiertem NSCLC ohne EGFR- oder ALK-Mutationen.
- Kleinzelliges Lungenkarzinom (SCLC): In Kombination mit Etoposid und Carboplatin oder Cisplatin zur Erstlinientherapie im fortgeschrittenen Stadium.
- Biliäre Tumore (BTC): In Kombination mit Gemcitabin und Cisplatin für die Erstbehandlung von nicht resezierbaren oder metastasierten biliären Tumoren.
- Hepatozelluläres Karzinom (HCC): Als Monotherapie oder in Kombination mit Tremelimumab für die Erstlinienbehandlung von fortgeschrittenem oder nicht resezierbarem HCC.
- Endometriumkarzinom: In Kombination mit Carboplatin und Paclitaxel zur Erstbehandlung von fortgeschrittenem oder rezidivierendem Karzinom, gefolgt von einer Erhaltungstherapie mit Durvalumab allein oder in Kombination mit Olaparib je nach Mismatch-Reparaturstatus.
Anwendungsart
Durvalumab wird ausschließlich intravenös als Infusion über eine Stunde verabreicht. Folgende Hinweise sind bei der Art der Anwendung zu beachten:
- Verdünnung und Vorbereitung: Für spezifische Anweisungen zur Verdünnung von Durvalumab vor der Anwendung wird auf die jeweilige Fachinformation des Wirkstoffs verwiesen.
- Infusionsreihenfolge bei Kombinationstherapie: Bei der Kombination mit Tremelimumab und Chemotherapie wird zuerst Tremelimumab, dann Durvalumab und anschließend die Chemotherapie infundiert. Separate Infusionsbeutel und -filter werden für jede Infusion verwendet.
- Zeitmanagement: Im ersten Zyklus folgt eine Stunde nach Ende der Tremelimumab-Infusion die Durvalumab-Infusion; die Chemotherapie beginnt eine Stunde nach Durvalumab. In späteren Zyklen kann der zeitliche Abstand auf 30 Minuten reduziert werden, falls klinisch vertretbar.
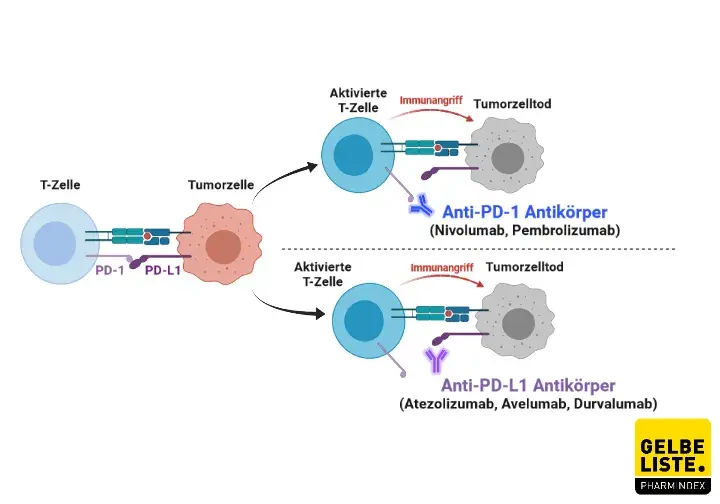
Wirkmechanismus
Der Checkpoint-Inhibitor Durvalumab bindet als PD-L1-Inhibitor an PD-L1, den Liganden des Oberflächenproteins PD-1. Durvalumab verhindert somit die Interaktion von PD-L1 mit PD-1 und dem CD80- Antigen der T-Zellen. Hierdurch werden Tumorzellen, die sich mithilfe von PD-1 dem Angriff des Immunsystems entziehen, einer Elimination durch körpereigene Immunzellen zugänglich gemacht.
Pharmakokinetik
- Bei Dosen < 3 mg/kg erhöhte sich in Studien die Exposition überdosisproportional und folgte somit einer nichtlinearen Pharmakokinetik. Bei Dosen ≥ 3 mg/kg lag eine dosisproportionale lineare Pharmakokinetik vor.
- Nach ca. 16 Wochen wurde der Steady-State erreicht.
- Bei einem Dosisbereich ≥ 10 mg/kg alle 2 Wochen betrug der geometrische Mittelwert des Verteilungsvolumens im Steady-State 5,64 l. Die Clearance verringerte sich mit der Zeit, was jedoch als nicht klinisch relevant angesehen wurde und erreichte an Tag 365 einen geometrischen Mittelwert im Steady-State von 8,16 ml/h.
- Die terminale Halbwertzeit betrug etwa 18 Tage. Durvalumab wird über Proteinkatabolismus über das retikuloendotheliale System oder über Elimination des Antikörper-Zielprotein-Komplexes ausgeschieden.
Dosierung
Dosierung von Durvalumab
- Empfohlene Dosis: Durvalumab wird als Monotherapie und in Kombinationstherapie gemäß der festgelegten Dosierung in der Fachinformation angewendet. Die Infusion dauert 1 Stunde.
- Dosisanpassungen: Änderungen der Dosis sind nicht vorgesehen. Abhängig von Verträglichkeit und Sicherheit kann eine Behandlungspause oder das Beenden der Therapie nötig sein.
Besondere Patientengruppen
- Ältere Patienten (≥ 65 Jahre): Keine Dosisanpassung erforderlich.
- Nierenfunktion: Keine Anpassung bei leichter bis mäßiger Einschränkung. Begrenzte Daten für schwere Niereninsuffizienz.
- Leberfunktion: Keine Anpassung bei leichter bis mäßiger Einschränkung. Datenlage für schwere Beeinträchtigung unzureichend.
- Kinder und Jugendliche: Nicht für Patienten unter 18 Jahren außerhalb klinischer Studien empfohlen.
Nebenwirkungen
Die häufigsten in klinischen Studien beschriebenen Nebenwirkungen waren (bei ≥ 20% Patienten):
- Husten
- Fatigue
- Dyspnoe
- radiogene Pneumonitis
15,4% der Patienten brachen die Therapie aufgrund von unerwünschten Ereignissen ab. Bei den mit Placebo behandelten Patienten waren es 9,8%.
Wechselwirkungen
Bei gleichzeitiger Anwendung von systemisch wirkenden Kortikosteroiden (Ausnahme systemische Kortikosteroide in physiologischer Dosis ≤10 mg/Tag Prednison oder ein entsprechendes Äquivalent) oder von Immunsuppressiva kann es zu einer Beeinflussung der pharmakodynamischen Aktivität und der Wirksamkeit von Durvalumab kommen.
Da Durvalumab durch Proteinkatabolismus über das retikuloendotheliale System oder die Zielstruktur-vermittelte Disposition eliminiert wird, werden keine metabolischen Arzneimittelwechselwirkungen erwartet.
Kontraindikation
Durvalumab darf nicht bei Überempfindlichkeit oder Allergie gegen den Wirkstoff angewendet werden.
Schwangerschaft
Durvalumab ist während der Schwangerschaft aufgrund potenzieller Risiken für den Fötus mit Vorsicht zu verwenden. Studien zeigen, dass Durvalumab die Plazenta passieren kann und in tierexperimentellen Modellen zu erhöhten Abortraten führte. Bei Frauen im gebärfähigen Alter ist während und bis mindestens drei Monate nach der Behandlung eine effektive Verhütungsmethode notwendig.
Stillzeit
Es ist unbekannt, ob Durvalumab in die Muttermilch übertritt. Das Risiko für das gestillte Kind kann nicht ausgeschlossen werden, was eine sorgfältige Abwägung zwischen Stillen und Behandlung erfordert.
Verkehrstüchtigkeit
Durvalumab hat keinen oder einen zu vernachlässigenden Einfluss auf die Verkehrstüchtigkeit und die Fähigkeit zum Bedienen von Maschinen.
Anwendungshinweise
Folgende Warnhinweise und Vorsichtsmaßnahmen sind bei der Anwendung von Durvalumab zu beachten:
- Immunvermittelte Nebenwirkungen: Bei Verdacht auf immunvermittelte Nebenwirkungen, wie Pneumonitis, Hepatitis oder Kolitis, ist eine genaue Überwachung erforderlich. Eine Therapie mit Kortikosteroiden kann notwendig sein.
- Pneumonitis/Strahlenpneumonitis: Patienten, die eine Radiochemotherapie erhalten haben, sollten auf Pneumonitis überwacht werden.
- Endokrinopathien: Regelmäßige Kontrolle der Schilddrüsen- und Nebennierenfunktion.
- Diabetes mellitus Typ 1: Überwachung auf Symptome von Diabetes.
- Nephritis: Überwachung der Nierenfunktion ist essenziell.
- Reaktionen auf Infusionen: Überwachung auf infusionsbedingte Reaktionen.
Alternativen
Je nach Indikationsgebiet und patientenindividuellen Gegebenheiten kommen weitere Checkpoint-Inhibitoren als Alternative in Frage:
Anti-CTLA-4-Antikörper
- Ipilimumab
- Tremelimumab
Anti-PD-1-Antikörper
Anti-PD-L1-Antikörper
Wirkstoff-Informationen
- EMA: Fachinformation Imfinzi
- Syed, Yahiya Y. "Durvalumab: first global approval." Drugs 77.12 (2017): 1369-1376.
- EMA: Summary of opinion (post authorisation) Imfinzi, 10 November 2022
- Fachinformationen des Durvalumab-Herstellers AstraZeneca (IMFINZI 50 mg /ml Konzentrat zur Herstellung einer Infusionslösung)