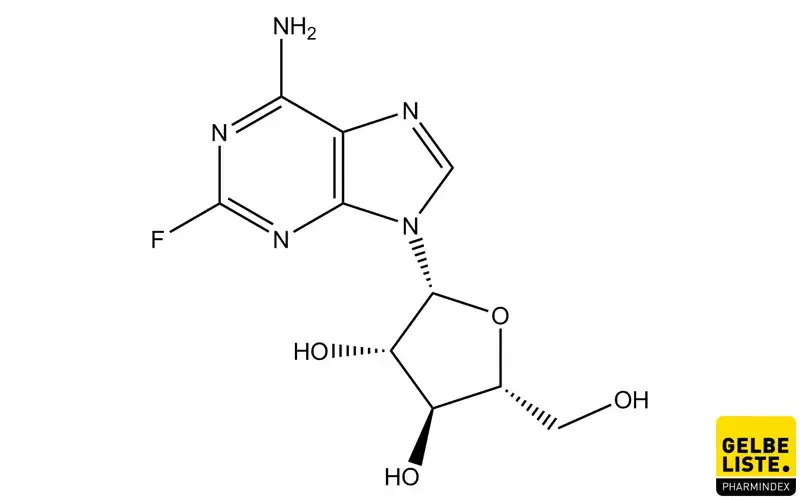
Fludarabin
Fludarabin ist ein fluoriertes Nukleotid-Analogon aus der Gruppe der Zytostatika, das zur Behandlung von chronisch lymphatischer Leukämie (CLL) angewendet wird. Fludarabin hat eine starke immunsuppressive Aktivität und wurde in einigen Fällen mit einer Reaktivierung von Hepatitis B in Verbindung gebracht.
Fludarabin: Übersicht
Anwendung
Fludarabin ist indiziert zur Therapie der chronischen lymphatischen Leukämie (CLL) vom B-Zell-Typ bei erwachsenen Patienten mit ausreichender Knochenmarkreserve. Die First-Line-Therapie mit sollte nur bei erwachsenen Patienten mit fortgeschrittener Erkrankung begonnen werden, d. h. im Rai-Stadium III/IV (Binet-Stadium C) oder im Rai-Stadium I/II (Binet-Stadium A/B), einhergehend mit krankheitsbedingten Symptomen oder dem Nachweis der fortschreitenden Erkrankung.
Off-label wird Fludarabin auch bei Haarzell-Leukämie, Mycosis fungoides, Hodgkin- und Non-Hodgkin-Lymphomen sowie in immunsuppressiven Therapien für nichtmyeloablative hämatopoetische Zelltransplantationen (HCT) eingesetzt.
Wirkmechanismus
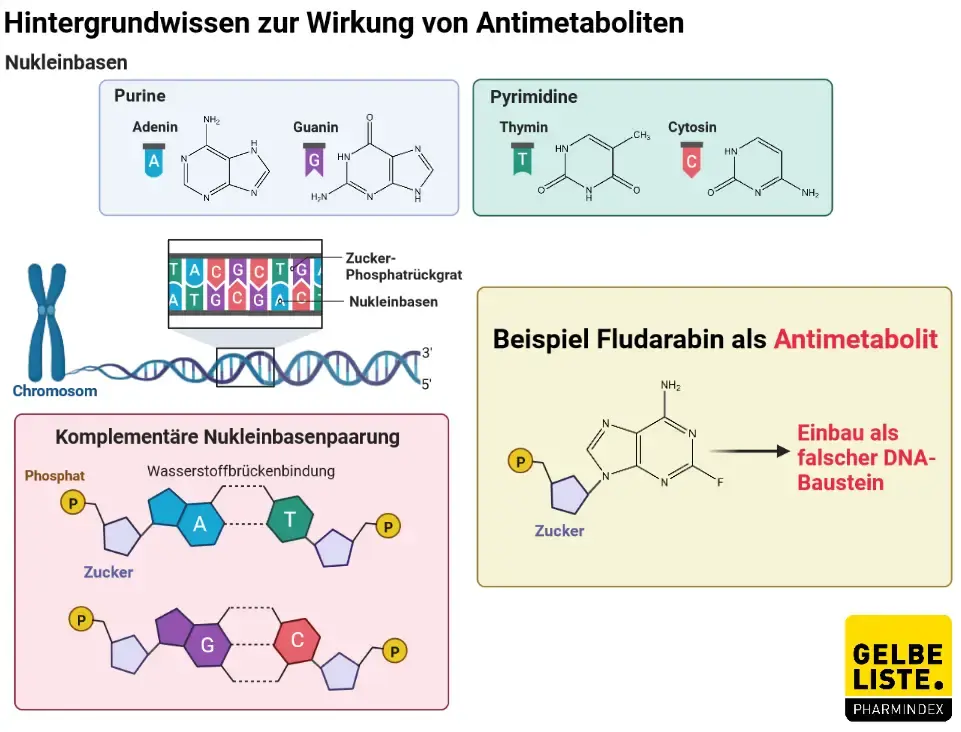
Fludarabin wird intrazellulär in das aktive Triphosphat umgewandelt, das mit Adenintriphosphat um die Bindung durch die DNA-Polymerase konkurriert, was zu einer Hemmung der DNA-Synthese führt.
Dosierung
Die typische Erwachsenendosis bei der Behandlung von CLL beträgt 25 mg/m2 Fludarabin intravenös oder 40 mg/m2 oral an 5 aufeinander folgenden Tagen in Abständen von 28 Tagen.
Nebenwirkungen
Häufige Nebenwirkungen von Fludarabin sind:
- Knochenmarksuppression
- Leukopenie
- Infektionen
- Fieber
- Übelkeit
- Erbrechen
- Anorexie
- Durchfall
- Kopfschmerzen
- Müdigkeit
- Hautausschlag
Wechselwirkungen
Folgende Wechselwirkungen sind bei der Anwendung von Fludarabin zu beachten:
- Pentostatin: Toxische Wirkungen auf die Lunge mit letalem Ausgang möglich
- Dipyridamol und andere Inhibitoren der Adenosinaufnahme: Therapeutische Wirksamkeit von Fludarabin kann reduziert werden
- Cytarabin: Anstieg der intrazellulären Spitzenkonzentrationen sowie der intrazellulären Exposition gegenüber Ara-CTP (aktiver Metabolit von Cytarabin) in leukämischen Zellen möglich
Kontraindikationen
Fludarabin besitzt folgende Gegenanzeigen:
- Überempfindlichkeit gegen den Wirkstoff
- Nierenfunktionsbeeinträchtigung mit einer Kreatinin-Clearance unter 30 ml/min
- Dekompensierte hämolytische Anämie
- Stillzeit
Schwangerschaft
Fludarabin darf während der Schwangerschaft nicht angewendet werden, es sei denn, dies ist eindeutig erforderlich (z. B. lebensbedrohliche Situationen, keine sicherere Behandlungsalternative), da Fludarabin schädigende Effekte auf den Fötus haben kann.
Stillzeit
Präklinische Daten deuten darauf hin, dass Fludarabinphosphat und/oder dessen Metaboliten in die Muttermilch übertreten. Aufgrund der Möglichkeit schwerwiegender Nebenwirkungen bei gestillten Säuglingen ist Fludarabin bei stillenden Müttern kontraindiziert.
Verkehrstüchtigkeit
Fludarabin kann die Verkehrstüchtigkeit oder die Fähigkeit zum Bedienen von Maschinen vermindern, da unter der Behandlung Ermüdung, Schwäche, Verwirrtheit, Krampfanfälle, Agitiertheit und Sehstörungen auftreten können.
- Steinhilber, Schubert, Zsilavecz, Roth; Medizinische Chemie 2. Auflage 2010
- Mutschler Mutschler Arzneimittelwirkungen, Pharmakologie – Klinische Pharmakologie – Toxikologie, Begründet von Ernst Mutschler, 11. Auflage 2020, Wissenschaftliche Verlagsgesellschaft Stuttgart
- Fachinformation Fludara
- Mutschler Mutschler Arzneimittelwirkungen, Pharmakologie – Klinische Pharmakologie – Toxikologie, Begründet von Ernst Mutschler, 11. Auflage 2020, Wissenschaftliche Verlagsgesellschaft Stuttgart
Abbildung
Created with Biorender
-
Bendarabin 50 mg Pulver zur Herstellung einer Injektions- oder Infusionslösung
Bendalis GmbH
-
Fludarabin Accord 25 mg/ml Konzentrat zur Herstellung einer Injektions- /Infusionslösung
Accord Healthcare GmbH
-
Fludarabin HEXAL® 25 mg/ml Konzentrat zur Herstellung einer Injektions- oder Infusionslösung
Hexal AG
-
Fludarabinphosphat-GRY® 25 mg/ml Konzentrat zur Herstellung einer Injektions- oder Infusionslösung
Teva GmbH