Galcanezumab
Galcanezumab ist ein humanisierter monoklonaler Antikörper, der zur Migräneprophylaxe angewendet wird. Der Wirkstoff gehört zu den ersten Antikörpern, die bei Migräne eingesetzt werden können und greift in das Calcitonin-Gene-Related-Peptide-System (CGRP) ein.
Galcanezumab: Übersicht
Anwendung
Galcanezumab (Emgality) ist als subkutane Injektion zur Migräneprophylaxe bei Erwachsenen mit mindestens vier Migränetagen pro Monat zugelassen.
Wirkmechanismus
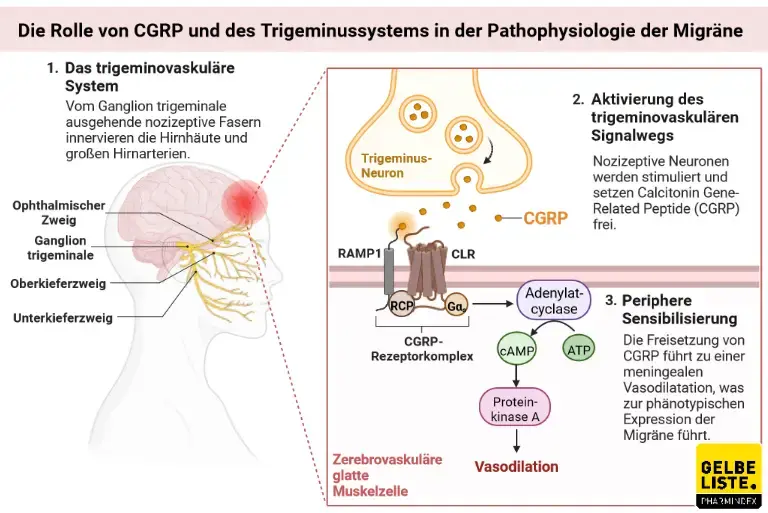
Galcanezumab ist ein humanisierter monoklonaler Antikörper, der an CGRP (Calcitonin Gene-Related Peptide) bindet und dessen biologische Aktivität inhibiert.
CGRP spielt eine wichtige Rolle im Entzündungsgeschehen und somit der Pathogenese von Migräne. Migräne-Patienten weisen während einer Migräne-Attacke erhöhte Blutkonzentrationen von CGRP auf.
Pharmakokinetik
Nach einer Anfangsdosis von 240 mg Galcanezumab betrug die maximale Serumkonzentration (Cmax) circa 30 μg/ml und die Zeit nach der Verabreichung bis dorthin 5 Tage. Unterschiedliche Injektionsstellen hatten keinen signifikanten Einfluss auf die Resorption von Galcanezumab. Das berechnete Verteilungsvolumen von Galcanezumab betrug 7,3 l. Es ist davon auszugehen, dass Galcanezumab wie endogenes IgG über katabole Stoffwechselwege zu kleinen Peptiden und Aminosäuren abgebaut wird. Die berechnete Clearance von Galcanezumab betrug etwa 0,008 l/Stunde und die Halbwertszeit lag bei 27 Tagen. Die Exposition von Galcanezumab erhöht sich proportional zur Dosis.
Dosierung
Die Behandlung wird mit 240 mg mittels subkutaner Injektion eingeleitet. Danach beträgt die empfohlene Dosierung 120 mg Galcanezumab einmal monatlich. 3 Monate nach Behandlungsbeginn sollte der Behandlungserfolg beurteilt werden.
Nebenwirkungen
Unter der Anwendung von Galcanezumab ist es sehr häufig (≥ 1/10) zu Schmerzen an der Injektionsstelle und Reaktionen an der Injektionsstelle gekommen. Häufig (≥ 1/100 bis < 1/10) kam es auch zu:
- Obstipation
- Vertigo
- Pruritus
Wechselwirkungen
Es wurden keine Wechselwirkungsstudien durchgeführt. Basierend auf den Eigenschaften von Galcanezumab sind keine pharmakokinetischen Wechselwirkungen zu erwarten.
Kontraindikationen
Galcanezumab darf bei einer Überempfindlichkeit gegenüber dem Wirkstoff nicht angewendet werden.
Schwangerschaft
Da humanes Immunglobulin (IgG) bekanntermaßen die Plazentaschranke passiert, sollte Galcanezumab als Vorsichtsmaßnahme während der Schwangerschaft nicht angewendet werden.
Stillzeit
Humanes IgG geht bekanntlich in den ersten Tagen nach der Geburt in die Muttermilch über. Kurz danach sinkt diese Konzentration auf einen niedrigen Spiegel ab. Während dieser Zeitspanne kann ein Risiko für das gestillte Kind nicht ausgeschlossen werden, danach kann die Anwendung von Galcanezumab in Betracht gezogen werden.
Verkehrstüchtigkeit
Da Galcanezumab zu Schwindel führen kann, ist ein geringer Einfluss auf die Verkehrstüchtigkeit und die Fähigkeit zum Bedienen von Maschinen möglich.
Alternativen
Galcanezumab ist nach Erenumab (Aimovig) der zweite Antikörper zur Migräneprophylaxe. Danach wurden die CGRP-Antikörper Fremanezumab (Ajovy) und Eptinezumab (VYEPTI) zugelassen.
- European comission, Fachinformation Emgality
- Lamb, Yvette N. "Galcanezumab: first global approval." Drugs 78.16 (2018): 1769-1775.
Abbildung
Adapted from „The Role of CGRP and the Trigeminal System in Migraine Pathophysiology”, by BioRender.com














