Gemcitabin
Der Wirkstoff Gemcitabin gehört zur Wirkstoffgruppe der Antimetabolite und wirkt als Zytostatikum gegen eine Reihe von Krebserkrankungen. Das Chemotherapeutikum wird u.a. eingesetzt zur Behandlung von Bronchial-, Harnblasen-, Pankreas-, Ovarial- und Mammakarzinom.
Gemcitabin: Übersicht
Anwendung
Gemcitabin wird zur Behandlung folgender Erkrankungen angewendet:
- lokal fortgeschrittenes oder metastasiertes Harnblasenkarzinom in Kombination mit Cisplatin
- lokal fortgeschrittenes oder metastasiertes Adenokarzinom des Pankreas
- Erstlinientherapie von lokal fortgeschrittenem oder metastasiertem nichtkleinzelligen Bronchialkarzinom (NSCLC) in Kombination mit Cisplatin. Eine Gemcitabin-Monotherapie kann bei älteren Patienten oder solchen mit einem Performance Status 2 in Betracht gezogen werden.
- lokal fortgeschrittenes oder metastasiertes epitheliales Ovarialkarzinom in Kombination mit Carboplatin und bei Patientinnen mit einem Rezidiv nach einer rezidivfreien Zeit von mindestens 6 Monaten nach einer platinbasierten Erstlinientherapie
- nicht operables, lokal rezidivierter oder metastasierter Brustkrebs, wenn es nach einer adjuvanten/neoadjuvanten Chemotherapie zu einem Rezidiv kam in Kombination mit Paclitaxel. Die vorausgegangene Chemotherapie sollte ein Anthracyclin enthalten haben, sofern dieses nicht klinisch kontraindiziert war
Anwendungsart
Gemcitabin ist in Form von eines Pulvers sowie eines Konzentrates zur Herstellung einer Infusionslösung auf dem deutschen Markt zugelassen.
Wirkmechanismus
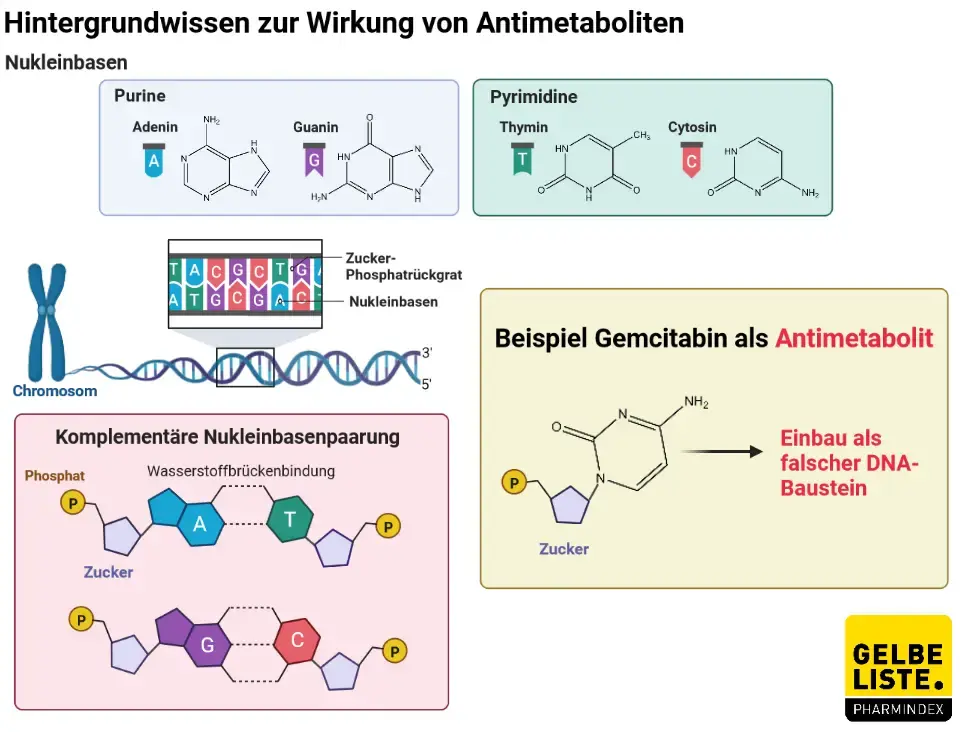
Gemcitabin ist ein Pyrimidin-Antimetabolit, der als Prodrug intrazellulär durch Nukleosidkinasen zu dem pharmakologisch aktiven Diphosphat-Nukleosid und Triphosphat-Nukleosid metabolisiert wird. Das Diphosphat-Nukleosid hemmt die Ribonukleotidreduktase, so dass keine Deoxynukleosidtriphosphate (dCTP) für die DNS-Synthese mehr geliefert werden können. Das Triphosphat-Nukleosid konkurriert mit Deoxynukleosidtriphosphaten um den Einbau in die DNS. In geringem Ausmaß kann auch Gemcitabin in die RNS eingebaut werden. Die DNS-Polymerase Epsilon ist nicht in der Lage, Gemcitabin zu entfernen und die gebildeten DNS-Stränge zu reparieren. Hierdurch resultiert eine vollständige Hemmung der weiteren DNS-Synthese und die Apoptose wird induziert.
Pharmakokinetik
Resorption
5 Minuten nach Ende der Infusion werden Plasma-Spitzen-Konzentration mit 3,2-45,5 μg/ml ermittelt. Nach einer Infusion von 1.000 mg/m2/30 min werden Konzentrationen der Muttersubstanz von über 5 μg/ml für etwa 30 min nach Infusion erreicht; in der daran anschließenden Stunde liegen sie über 0,4 μg/ml.
Verteilung
Das Verteilungsvolumen des zentralen Kompartimentes betrug 12,4 l/m2 bei Frauen und 17,5 l/m2 bei Männern mit einer interindividuelle Variabilität von 91,9%. Das Verteilungsvolumen des peripheren Kompartimentes betrug 47,4 l/m2. Die Plasmaproteinbindung ist vernachlässigbar gering.
Die Halbwertszeit von Gemcitabin liegt zwischen 42 und 94 Minuten in Abhängigkeit von Alter und Geschlecht. Bei dem empfohlenen Dosierungsschema ist die Ausscheidung von Gemcitabin innerhalb von 5 bis 11 Stunden nach Infusionsbeginn nahezu vollständig abgeschlossen. Bei einmaliger Gabe pro Woche erfolgt keine Kumulation.
Biotransformation
Gemcitabin wird durch die Cytidindeaminase rasch in der Leber, den Nieren, im Blut und weiteren Organen metabolisiert. Durch intrazellulären Metabolismus entstehen Gemcitabinmono-, -di- und -tri-phosphat (dFdCMP, dFdCDP und dFdCTP), von denen dFdCDP und dFdCTP als aktive Metaboliten angesehen werden. Diese intrazellulären Metaboliten wurden nicht im Plasma und im Urin gefunden. Der primäre Metabolit 2‘-Deoxy-2‘,2‘-difluoruridin (dFdU) ist inaktiv und kommt im Plasma und im Urin vor.
Elimination
Die systemische Clearance beträgt 29,2-92,2 l/Stunde/m2 und ist abhängig vom Geschlecht und vom Alter (die interindividuelle Variabilität betrug 52,2%). Die Clearancewerte für Frauen liegen etwa 25% unter denen für Männer. Die Clearance verringert sich mit dem Alter. Im Harn werden weniger als 10% unverändertes Gemcitabin ausgeschieden.
Die renale Clearance beträgt 2-7 l/Stunde/m2. 92-98% der Gemcitabin-Dosis werden innerhalb einer Woche ausgeschieden, 99% davon im Urin und 1% der Dosis über die Faeces.
Dosierung
Je nach Krebserkrankung liegen unterschiedliche Dosierungsempfehlungen vor, die der jeweiligen Fachinformation entnommen werden können.
Nebenwirkungen
Zu den am häufigsten berichteten Nebenwirkungen im Zusammenhang mit einer Gemcitabin-Behandlung gehören:
- Übelkeit mit oder ohne Erbrechen
- erhöhte Transaminasen (AST, ALT) und alkalische Phosphatase
- Proteinurie und Hämaturie
- Atemnot
- allergische Hautausschläge
Die Häufigkeit und Schwere der Nebenwirkungen hängen von der Dosis, der Infusionsgeschwindigkeit und dem Abstand zwischen den einzelnen Dosen.
Wechselwirkungen
Es wurden keine speziellen Wechselwirkungsstudien durchgeführt. Folgende mögliche Wechselwirkungen sind jedoch zu beachten:
- Strahlentherapie ► Präklinische und klinische Studien haben gezeigt, dass Gemcitabin eine strahlensensibilisierende Wirkung hat. Es wurden schwerwiegende und möglicherweise lebensbedrohliche Mukositiden, insbesondere Ösophagitis und Pneumonitis, beobachtet, speziell bei Patienten, bei denen ein großes Volumen bestrahlt wurde (mittlere Behandlungsvolumina 4.795 cm3). Später durchgeführte Studien haben gezeigt, dass es möglich ist, Gemcitabin in niedrigerer Dosierung gleichzeitig mit einer Strahlentherapie zu geben bei berechenbarer Toxizität, wie eine Phase-II-Studie bei NSCLC-Patienten, in der eine Bestrahlung des Thorax mit Dosen von 66 Gy gleichzeitig mit einer Verabreichung von Gemcitabin (600 mg/m2 4-mal) und Cisplatin (80 mg/m2 2-mal) innerhalb von 6 Wochen gegeben wurde. Das optimale Dosierungsschema für die sichere Anwendung von Gemcitabin zusammen mit therapeutischen Strahlendosen ist jedoch nicht für alle Tumorarten bekannt.
- Gelbfieberimpfung und andere attenuierte Lebendimpfstoffe ►die gleichzeitige Anwendung wird nicht empfohlen aufgrund des Risikos einer systemischen, möglicherweise tödlichen Erkrankung, insbesondere bei immunsupprimierten Patienten.
Kontraindikationen
Gemcitabin darf nicht angewendet werden, wenn eine Überempfindlichkeit gegen den Wirkstoff vorliegt. Stillen gehört außerdem zu den Gegenanzeigen.
Schwangerschaft
Es liegen keine adäquaten Daten zur Anwendung von Gemcitabin bei Schwangeren vor. Tierexperimentelle Studien haben eine Reproduktionstoxizität gezeigt. Aufgrund der Ergebnisse aus tierexperimentellen Studien und des Wirkungsmechanismus von Gemcitabin, darf die Substanz nicht in der Schwangerschaft angewendet werden, außer wenn unbedingt erforderlich. Frauen sollten angewiesen werden, während einer Behandlung mit Gemcitabin nicht schwanger zu werden und den behandelnden Arzt unverzüglich zu informieren, wenn dieses trotzdem eintreten sollte.
Stillzeit
Es ist nicht bekannt, ob Gemcitabin in der Muttermilch ausgeschieden wird und Nebenwirkungen beim gestillten Kind können nicht ausgeschlossen werden. Während einer Gemcitabin-Behandlung muss abgestillt werden.
Verkehrstüchtigkeit
Es wurden keine Studien zu den Auswirkungen auf die Verkehrstüchtigkeit und die Fähigkeit zum Bedienen von Maschinen durchgeführt. Jedoch kann Gemcitabin leichte bis mäßige Schläfrigkeit verursachen, insbesondere im Zusammenwirken mit Alkohol. Die Patienten müssen vor der aktiven Teilnahme am Verkehr oder dem Bedienen von Maschinen gewarnt werden, solange nicht gesichert ist, dass sie nicht schläfrig werden.
Weitere Informationen sind der jeweiligen Fachinformation zu entnehmen.
Wirkstoff-Informationen
- Fachinformation Gemcitabin HEXAL
- Parker, W. B. (2009). Enzymology of purine and pyrimidine antimetabolites used in the treatment of cancer. Chemical reviews, 109(7), 2880-2893
- Mutschler Mutschler Arzneimittelwirkungen, Pharmakologie – Klinische Pharmakologie – Toxikologie, Begründet von Ernst Mutschler, 11. Auflage 2020, Wissenschaftliche Verlagsgesellschaft Stuttgart
Abbildung
Created with Biorender
-
axigem® 38 mg/ml, Pulver zur Herstellung einer Infusionslösung, 200 mg
Axionovo GmbH
-
axigem® 38 mg/ml, Pulver zur Herstellung einer Infusionslösung, 1000 mg
Axionovo GmbH
-
axigem® 38 mg/ml, Pulver zur Herstellung einer Infusionslösung, 1500 mg
Axionovo GmbH
-
Bendacitabin 38 mg/ml Pulver zur Herstellung einer Infusionslösung, 1 g
Bendalis GmbH
-
Bendacitabin 38 mg/ml Pulver zur Herstellung einer Infusionslösung, 2 g
Bendalis GmbH
-
Bendacitabin 38 mg/ml Pulver zur Herstellung einer Infusionslösung, 200 mg
Bendalis GmbH
-
GEMCI-Cell® 38 mg/ml Konzentrat zur Herstellung einer Infusionslösung, 1000 mg
STADAPHARM GmbH
-
GEMCI-Cell® 38 mg/ml Konzentrat zur Herstellung einer Infusionslösung, 2000 mg
STADAPHARM GmbH
-
Gemcitabin Accord 100 mg/ml Konzentrat zur Herstellung einer Infusionslösung, 200 mg
Accord Healthcare GmbH
-
Gemcitabin Accord 100 mg/ml Konzentrat zur Herstellung einer Infusionslösung, 1000 mg
Accord Healthcare GmbH
-
Gemcitabin Accord 100 mg/ml Konzentrat zur Herstellung einer Infusionslösung, 2000 mg
Accord Healthcare GmbH
-
Gemcitabin AqVida 38 mg/ml Pulver zur Herstellung einer Infusionslösung, 200 mg
AqVida GmbH
-
Gemcitabin AqVida 38 mg/ml Pulver zur Herstellung einer Infusionslösung, 1000 mg
AqVida GmbH
-
Gemcitabin Aurobindo 40 mg/ml Konzentrat zur Herstellung einer Infusionslösung, 1000 mg
PUREN Pharma GmbH & Co. KG
-
Gemcitabin Aurobindo 40 mg/ml Konzentrat zur Herstellung einer Infusionslösung, 2000 mg
PUREN Pharma GmbH & Co. KG
-
Gemcitabin-GRY® 1000 mg Pulver zur Herstellung einer Infusionslösung
Teva GmbH
-
Gemcitabin HEXAL® 40 mg/ml Konzentrat zur Herstellung einer Infusionslösung, 200 mg/5 ml
Hexal AG
-
Gemcitabin HEXAL® 40 mg/ml Konzentrat zur Herstellung einer Infusionslösung, 1000 mg/25 ml
Hexal AG
-
Gemcitabin HEXAL® 40 mg/ml Konzentrat zur Herstellung einer Infusionslösung, 2000 mg/50 ml
Hexal AG
-
Gemcitabin Hikma 38 mg/ml Konzentrat zur Herstellung einer Infusionslösung, 200 mg
Hikma Pharma GmbH
-
Gemcitabin Hikma 38 mg/ml Konzentrat zur Herstellung einer Infusionslösung, 1000 mg
Hikma Pharma GmbH
-
Gemcitabin Hikma 38 mg/ml Konzentrat zur Herstellung einer Infusionslösung, 2000 mg
Hikma Pharma GmbH
-
Gemcitabin SUN 10 mg/ml Infusionslösung, 120 ml
Sun Pharmaceuticals Germany GmbH
-
Gemcitabin SUN 10 mg/ml Infusionslösung, 140 ml
Sun Pharmaceuticals Germany GmbH
-
Gemcitabin SUN 10 mg/ml Infusionslösung, 160 ml
Sun Pharmaceuticals Germany GmbH
-
Gemcitabin SUN 10 mg/ml Infusionslösung, 180 ml
Sun Pharmaceuticals Germany GmbH
-
Gemcitabin SUN 10 mg/ml Infusionslösung, 200 ml
Sun Pharmaceuticals Germany GmbH
-
Gemcitabin SUN 10 mg/ml Infusionslösung, 220 ml
Sun Pharmaceuticals Germany GmbH
-
Gemcitabin VENUS 1.000 mg Pulver zur Herstellung einer Infusionslösung
Venus Pharma GmbH
-
Gemcitabin VENUS 200 mg Pulver zur Herstellung einer Infusionslösung
Venus Pharma GmbH
-
Gemcitabin Vipharm 200 mg Pulver zur Herstellung einer Infusionslösung
Vipharm GmbH
-
Gemcitabin Vipharm 1000 mg Pulver zur Herstellung einer Infusionslösung
Vipharm GmbH
-
Gemcitabin Vitane 38 mg/ml Pulver zur Herstellung einer Infusionslösung, 200 mg
Vitane Pharma GmbH
-
Gemcitabin Vitane 38 mg/ml Pulver zur Herstellung einer Infusionslösung, 1000 mg
Vitane Pharma GmbH
-
Gemcitabine SUN 1 g Pulver zur Herstellung einer Infusionslösung
Sun Pharmaceuticals Germany GmbH
-
Ribozar® 1 g Pulver zur Herstellung einer Infusionslösung
Hikma Pharma GmbH
-
Ribozar® 200 mg Pulver zur Herstellung einer Infusionslösung
Hikma Pharma GmbH