Letermovir
Letermovir ist ein antivirales Arzneimittel, das zur Prophylaxe einer Cytomegalovirus-(CMV-)Reaktivierung bei CMV-seropositiven Erwachsenen nach allogener hämatopoetischer Stammzelltransplantation (HSCT) eingesetzt wird. Es hemmt die CMV-Replikation durch Blockade des viralen Terminase-Komplexes.
Wirkstoff Letermovir: Übersicht
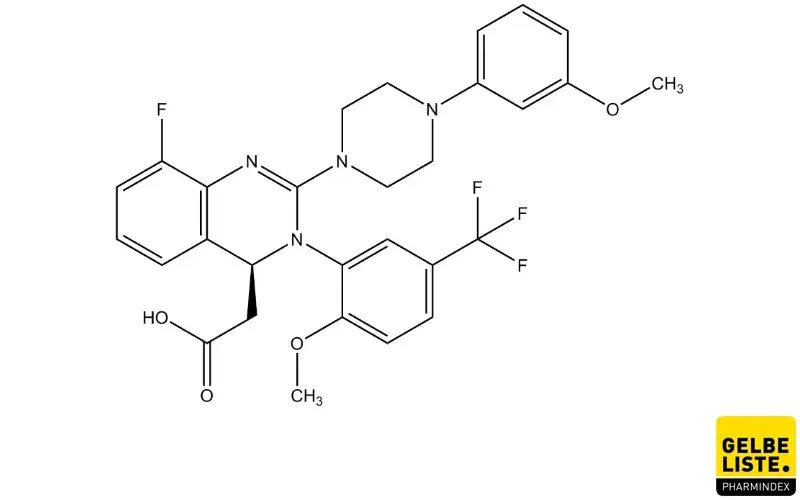
Anwendung
Letermovir wird zur Prophylaxe einer CMV-Infektion und CMV-Erkrankung bei CMV-seropositiven Erwachsenen nach allogener hämatopoetischer Stammzelltransplantation angewendet.
Anwendungsart
Letermovir wird oral als Filmtablette oder intravenös als Infusionslösung verabreicht. Die Therapie sollte so bald wie möglich innerhalb der ersten 28 Tage nach Transplantation begonnen werden.
Wirkmechanismus
Letermovir hemmt spezifisch den Terminase-Komplex (pUL56-pUL89-pUL51) des humanen Cytomegalovirus. Dieser Komplex ist für die Verarbeitung und Verpackung der viralen DNA erforderlich. Durch die Hemmung dieses Komplexes wird die Prozessierung viraler DNA-Konkatemere zu genomlangen Einheiten und deren Verpackung in Kapside verhindert. Dies führt zur Bildung unreifer, nicht-infektiöser Viruspartikel und unterbricht den viralen Replikationszyklus. Letermovir ist CMV-spezifisch und zeigt keine Aktivität gegen andere Herpesviren.
Pharmakokinetik
Die pharmakokinetischen Eigenschaften von Letermovir umfassen:
- Resorption: Nach oraler Gabe wird Letermovir resorbiert, die absolute Bioverfügbarkeit beträgt ca. 35% (bei Gabe mit Ciclosporin ca. 85%). Die Einnahme mit Nahrung kann die Resorption erhöhen. Die Zeit bis zum Erreichen der maximalen Plasmakonzentration (tmax) beträgt ca. 1,5 - 2,25 Stunden.
- Verteilung: Hohe Plasmaproteinbindung (>98%), hauptsächlich an Albumin. Das Verteilungsvolumen im Steady State ist moderat (ca. 45 l).
- Metabolismus: Letermovir wird hauptsächlich durch Glucuronidierung über die UGT1A1 und UGT1A3 Enzyme metabolisiert. CYP-Enzyme spielen für den Metabolismus von Letermovir selbst eine untergeordnete Rolle, Letermovir ist jedoch ein moderater Inhibitor von CYP3A und ein Induktor von CYP2C9/2C19 sowie ein Substrat und Inhibitor der Transporter OATP1B1/3.
- Elimination: Die Elimination erfolgt überwiegend über die Galle und Fäzes (>93% der Dosis), während die renale Elimination vernachlässigbar ist (<2%). Die terminale Halbwertszeit beträgt ca. 12 Stunden bei alleiniger Gabe.
Dosierung
Die empfohlene Dosierung von Letermovir beträgt:
- Orale oder intravenöse Anwendung: 480 mg einmal täglich.
- Bei gleichzeitiger Anwendung mit Ciclosporin: Reduktion auf 240 mg einmal täglich.
- Die Therapie sollte bis Tag 100 nach Transplantation fortgeführt werden.
Nebenwirkungen
Mögliche Nebenwirkungen bei der Anwendung von Letermovir sind:
- Sehr häufig (≥1/10): Übelkeit.
- Häufig (≥1/100 bis <1/10): Erbrechen, Bauchschmerzen, Durchfall, Kopfschmerzen, Fatigue.
- Gelegentlich (≥1/1.000 bis <1/100): Vorhofflimmern, Leberfunktionsstörungen, Hautausschlag.
- Selten (<1/1.000): Überempfindlichkeitsreaktionen.
- Sehr selten (<1/10.000): Keine bekannt.
Wechselwirkungen
Bei gleichzeitiger Anwendung können zahlreiche klinisch signifikante Wechselwirkungen auftreten, hauptsächlich durch die Wirkung von Letermovir auf CYP3A, CYP2C9/19 und OATP1B1/3:
- Ciclosporin: Erhöht die Letermovir-Exposition (Dosisreduktion von Letermovir erforderlich!). Letermovir erhöht auch leicht die Ciclosporin-Konzentration.
- CYP3A-Substrate: Letermovir (insbesondere ohne Ciclosporin) hemmt CYP3A moderat. Vorsicht/Dosisanpassung bei gleichzeitig angewendeten CYP3A-Substraten (z.B. bestimmte Immunsuppressiva wie Tacrolimus, Sirolimus; Amiodaron, Chinidin, viele Statine, Kalziumkanalblocker).
Kontraindiziert: Pimozid, Ergotalkaloide.
Nicht empfohlen/Vorsicht: Bestimmte Statine (Simvastatin, Pitavastatin - v.a. mit Ciclosporin), Alfentanil, Fentanyl, Midazolam. - OATP1B1/3-Substrate: Letermovir hemmt OATP1B1/3. Vorsicht/Dosisanpassung bei Substraten wie Statinen (z.B. Atorvastatin, Pravastatin, Rosuvastatin), Repaglinid, Glyburid.
- CYP2C9/19-Substrate: Letermovir induziert diese Enzyme. Die Wirksamkeit von Substraten (z.B. Warfarin, Phenytoin, Omeprazol, Voriconazol) kann reduziert sein.
- CYP3A-Induktoren: Starke Induktoren (z.B. Rifampicin, Carbamazepin, Phenytoin, Johanniskraut) können die Letermovir-Konzentration stark senken und sind kontraindiziert oder nicht empfohlen.
- Orale Kontrazeptiva: Die Wirksamkeit kann reduziert sein.
Eine sorgfältige Prüfung aller Begleitmedikamente ist vor und während der Therapie essenziell.
Einfluss der Applikationsart und von Ciclosporin:
Die Wechselwirkungen können sich abhängig von der Applikationsart (oral oder i.v.) und der gleichzeitigen Einnahme von Ciclosporin verändern. Bei Änderungen sollten die jeweiligen Empfehlungen überprüft werden.
Kontraindikationen
Letermovir darf nicht angewendet werden bei
- Überempfindlichkeit gegen Letermovir oder einen der sonstigen Bestandteile.
- Gleichzeitiger Anwendung mit Pimozid
- Gleichzeitiger Anwendung mit Mutterkornalkaloiden
Bei Kombination von Letermovir mit Ciclosporin darf zusätzlich keine Anwendung erfolgen von:
Schwangerschaft
Für Letermovir liegen keine ausreichenden Daten zur Anwendung in der Schwangerschaft vor. In tierexperimentellen Studien wurden keine teratogenen Effekte beobachtet. Aus Vorsichtsgründen sollte die Anwendung während der Schwangerschaft vermieden werden.
Stillzeit
Es ist nicht bekannt, ob Letermovir in die Muttermilch übergeht. Eine Anwendung während der Stillzeit wird nicht empfohlen.
Verkehrstüchtigkeit
Letermovir hat keinen oder nur einen vernachlässigbaren Einfluss auf die Verkehrstüchtigkeit und das Bedienen von Maschinen.
Anwendungshinweise
Folgende Warnhinweise und Vorsichtsmaßnahmen sind bei der Anwendung von Letermovir zu beachten:
- Überwachung der CMV-DNA:
Die CMV-DNA sollte regelmäßig kontrolliert werden, insbesondere während der ersten 14 Wochen nach Transplantation wöchentlich und anschließend alle zwei Wochen. Bei klinisch relevanter CMV-DNA-ämie oder Erkrankung ist die Prophylaxe zu beenden. - Wechselwirkungen:
Letermovir kann die Wirkung anderer Arzneimittel beeinflussen oder selbst in seiner Wirkung beeinträchtigt werden. Eine sorgfältige Prüfung möglicher Wechselwirkungen ist erforderlich. - CYP3A-Substrate:
Bei gleichzeitiger Anwendung mit Arzneimitteln, die CYP3A-Substrate mit geringer therapeutischer Breite sind (z. B. Alfentanil, Fentanyl, Chinidin), ist Vorsicht geboten. Eine engmaschige Überwachung und Dosisanpassung dieser Medikamente wird empfohlen. - Immunsuppressiva:
Die Konzentration von Ciclosporin, Tacrolimus und Sirolimus kann durch Letermovir beeinflusst werden. Eine engmaschige Kontrolle der Blutspiegel ist zu Beginn und nach Beendigung der Letermovir-Therapie sowie bei Wechsel der Anwendungsart erforderlich. - Induktion von Enzymen und Transportern:
Letermovir kann den Abbau bestimmter Arzneimittel beschleunigen und deren Wirkung verringern. Dies betrifft unter anderem Voriconazol, Phenytoin und Dabigatran. Bei Voriconazol und Phenytoin wird ein Therapeutisches Drug Monitoring empfohlen. Dabigatran sollte möglichst nicht gleichzeitig angewendet werden. - OATP1B1/3-Substrate:
Letermovir kann die Plasmakonzentrationen von Arzneimitteln erhöhen, die über OATP1B1/3 transportiert werden, z. B. bestimmte Statine. Eine Dosisanpassung kann erforderlich sein.
Alternativen
Folgende Alternativen stehen (je nach Situation und Patient) für die CMV-Prophylaxe oder Präemptivtherapie nach allo-HSZT zur Verfügung:
- Valganciclovir / Ganciclovir: Breiter wirksam gegen Herpesviren, aber mit signifikanter hämatologischer Toxizität (Neutropenie). Oft für Präemptivtherapie verwendet.
- Foscarnet: Nephrotoxisch, Elektrolytstörungen. Meist bei Resistenzen oder Unverträglichkeiten gegen Ganciclovir eingesetzt.
- Cidofovir: Stark nephrotoxisch. Selten zur Prophylaxe eingesetzt.
Wirkstoff-Informationen
Fachinformation Prevymis® (Letermovir)
-
PREVYMIS 20 mg Granulat im Beutel
MSD Sharp & Dohme GmbH
-
PREVYMIS 120 mg Granulat im Beutel
MSD Sharp & Dohme GmbH
-
PREVYMIS® 240 mg Filmtabletten
MSD Sharp & Dohme GmbH
-
PREVYMIS® 240 mg Konzentrat zur Herstellung einer Infusionslösung
MSD Sharp & Dohme GmbH
-
PREVYMIS® 480 mg Filmtabletten
MSD Sharp & Dohme GmbH
-
PREVYMIS® 480 mg Konzentrat zur Herstellung einer Infusionslösung
MSD Sharp & Dohme GmbH











