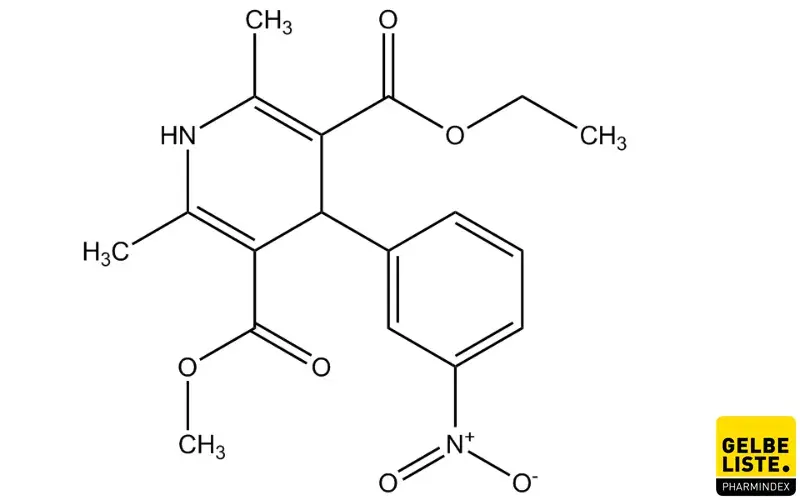
Nitrendipin
Das Antihypertensivum Nitrendipin ist ein selektiver Calciumkanalantagonist vom Dihydropyridin-Typ, der den Calciumioneneinstrom in die glatte Gefäßmuskulatur inhibiert und dadurch die calciumabhängige Kontraktion der Gefäße verhindert.
Nitrendipin: Übersicht
Anwendung
Der Wirkstoff Nitrendipin gehört zur Wirkstoffgruppe der Calciumkanalblocker vom Dihydropyridin-Typ. Aufgrund seiner vorwiegenden Gefäßwirkung ist Nitrendipin indiziert zur Behandlung der essenziellen Hypertonie.
Anwendungsart
Nitrendipin ist in Tablettenform (10 mg, 20 mg) und war als Lösung zum Einnehmen (5 mg/ml, Bayotensin® akut, mittlerweile eingestellt) auf dem deutschen Markt verfügbar.
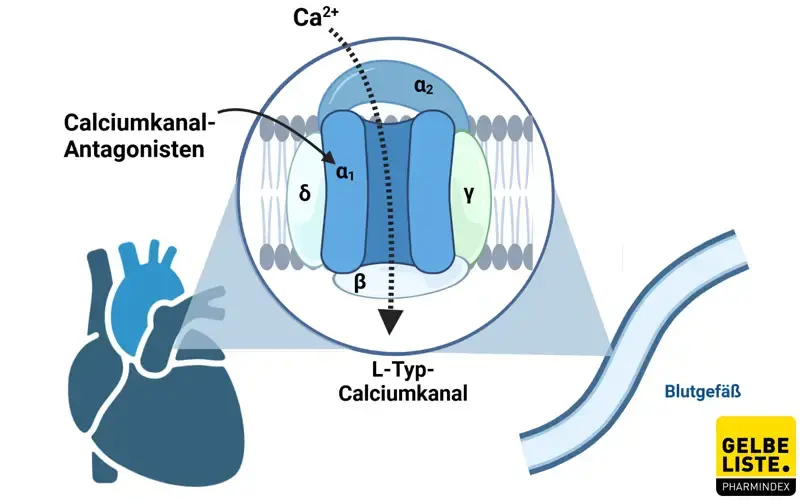
Wirkmechanismus
Nitrendipin zählt zur Klasse der 1,4-Dihydropyridine, welche L-Typ-Calciumkanäle hemmen, indem sie deren inaktiven Zustand stabilisieren. Dieser inaktive Zustand liegt vor allem in der glatten Gefäßmuskulatur vor, wodurch sich eine Selektivität für glatte Gefäßmuskelzellen ergibt. Durch die Aufrechterhaltung des inaktivierten Zustandes kommt es zu einem verminderten Einstrom von Calciumionen in die Gefäßmuskulatur, was zu einer Relaxation der Gefäße und einer Senkung des peripheren Gefäßwiderstandes führt [4]. Daraus resultiert eine Blutdrucksenkung. Zu Beginn der Therapie ergibt sich ein leicht natriuretischer Effekt.
Pharmakokinetik
Resorption
Nach oraler Einnahme erfolgt eine schnelle und nahezu vollständige Resorption (88%). Maximale Plasmakonzentrationen (cmax) nach Tabletteneinnahme werden 1-3 Stunden nach der Einnahme erreicht. Bei Anwendungder Lösung zum Einnehmen tritt die cmax bereits nach ca. 30 min auf.
Bioverfügbarkeit
Die absolute Bioverfügbarkeit wird durch einen ausgeprägten First-Pass-Effekt auf 20-30% reduziert. Die relative Bioverfügbarkeit der Tabletten im Vergleich zur oralen Lösung beträgt ca. 82%.
Verteilung
Nitrendipin liegt vorwiegend an Albumin gebunden vor (96-98%), weshalb es nicht dialysierbar ist. Das Verteilungsvolumen liegt im Steady State bei 5-9 l/kg Körpergewicht, wodurch beispielsweise eine Plasmapherese wenig Erfolg einbringen wird.
Metabolismus (Biotransformation)
Nitrendipin wird vor allem über oxidative Reaktionen nahezu vollständig hepatisch metabolisiert. Entsprechend muss bei Patienten mit chronischen Lebererkrankungen die Dosierung angepasst werden, da sonst mit erhöhten Plasmaspiegeln zu rechnen ist.
Elimination
Nur geringe Mengen (< 0,1%) einer oralen Dosis Nitrendipin werden unverändert mit dem Urin ausgeschieden.
Nitrendipin wird in Form seiner Metabolite vorwiegend renal ausgeschieden (etwa 77%, Rest über Fäzes). Da diese Metabolite pharmakologisch jedoch nicht aktiv sind, muss keine Dosisanpassung bei Patienten mit eingeschränkter Nierenfunktion erfolgen. Die Eliminationshalbwertszeit beträgt 8-12 Stunden für Tablettenformulierungen.
Dosierung
Die Dosierungsempfehlung von Nitrendipin basiert auf dem Schweregrad der Hypertonie.
Standarddosierungen für Erwachsene:
- 2 x täglich (morgens und abends) 10 mg
- 1 x täglich (morgens) 20 mg
Tagesdosen bis zu 40 mg Nitrendipin sind möglich.
Patientenindividuelle Dosisanpassungen (aufgrund von Lebererkrankungen oder CYP3A4 beeinflussenden Co-Medikationen) können notwendig sein. Hierbei wird eine Startdosis von 10 mg unter häufiger Blutdruckkontrolle empfohlen. Grapefruitsaft sollte nicht zusammen mit Nitrendipin eingenommen werden, da sich die Wirkung des Wirkstoffs dadurch verstärken kann.
Nitrendipin ist lichtempfindlich und sollte erst unmittelbar vor der Einnahme aus dem schützenden Blister entnommen werden.
Nebenwirkungen
Häufige Nebenwirkungen bei der Anwendung von Nitrendipin sind:
- Kopfschmerzen
- Palpitationen
- Ödeme
- Flatulenz
- Schwächegefühl
- Angstzustände
Zu den schwerwiegenden Nebenwirkungen, die eine sofortige Intervention erfordern können, zählen:
- arterielle Hypotonien und Angina-pectoris-Anfälle
Auch allergische Reaktionen einschließlich Angioödem sind möglich.
Wechselwirkungen
Bei der Anwendung von Nitrendipin sind folgende Wechselwirkungen zu beachten:
- CYP3A4-Inhibitoren (Makrolide, HIV-Proteaseinhibitoren, Azol-Antimykotika, Nefazodon, Quinupristin/Dalfopristin, Valproinsäure, Cimetidin/Ranitidin, Fluoxetin): Die gleichzeitige Anwendung erhöht die Nitrendipin Plasmakonzentration. Eventuell ist eine Dosisanpassung unter Berücksichtigung des Blutdrucks notwendig.
- Grapefruitsaft: Grapefruitsaft hemmt ebenfalls das CYP3A4-System. Aus diesem Grund kann die Plasmakonzentration von Nitrendipin noch bis zu 3 Tage nach Einnahme von Grapefruitsaft erhöht sein. Die gleichzeitige Einnahme von Nitrendipin und Grapefruitsaft sollte vermieden werden.
- CYP3A4-Induktoren (Rifampicin, Phenytoin, Carbamazepin): Die gleichzeitige Anwendung verringert die Nitrendipin Plasmakonzentration und kann zu einer reduzierten Wirksamkeit der antihypertensiven Therapie führen.
- Digoxin: Die gleichzeitige Einnahme von Nitrendipin kann zu einer Erhöhung der Plasmakonzentration von Digoxin führen. Eine engmaschige Kontrolle sowie ggf. eine Dosisminderung werden empfohlen.
- Muskelrelaxanzien (wie z.B. Pankuronium): Unter gleichzeitiger Therapie mit Nitrendipin kann die Wirkung von Muskelrelaxanzien verlängert und verstärkt werden.
- Blutdrucksenkende Arzneimittel (Diuretika, Beta-Blocker, ACE-Inhibitoren, AT1-Rezeptorantagonisten, andere Calciumantagonisten, Alpha-Rezeptorblocker, PDE5-Inhibitoren, Alpha-Methyldopa) können bei gleichzeitiger Anwendung die Wirkung von Nitrendipin potenzieren.
Kontraindikation
Nitrendipin darf nicht angewendet werden bei:
- Überempfindlichkeit gegen Nitrendipin oder einen der sonstigen Bestandteile der Formulierung
- akutem Myokardinfarkt (innerhalb der ersten 4 Wochen)
- instabiler Angina pectoris
- während der Schwangerschaft und Stillzeit
- Anwendung von Rifampicin (CYP3A4-Induktor, keine wirksamen Nitrendipin Plasmaspiegel)
Schwangerschaft
Die Einnahme von Nitrendipin ist während der Schwangerschaft und Stillzeit kontraindiziert. Es liegen keine hinreichenden Daten für die Verwendung von Nitrendipin bei Schwangeren und Stillenden vor. Im Tierexperiment haben sich teilweise Hinweise für eine Reproduktionstoxizität ergeben. Beim Menschen liegen keine Erfahrungen vor.
Stillzeit
Die Einnahme von Nitrendipin ist während der Schwangerschaft und Stillzeit kontraindiziert. Es liegen keine hinreichenden Daten für die Verwendung von Nitrendipin bei Schwangeren und Stillenden vor. Da Nitrendipin in geringen Mengen in die Muttermilch übergeht, sollte bei notwendiger Therapiefortsetzung mit Nitrendipin abgestillt werden, da auch hier keine Erfahrungen vorliegen.
Verkehrstüchtigkeit
Vor allem zu Behandlungsbeginn, bei Dosiserhöhung sowie im Zusammenspiel mit Alkohol können sich Einschränkungen unter der Anwendung von Nitrendipin ergeben.
Anwendungshinweise
Dekompensierte Herinsuffizienz
Patienten mit dekompensierter Herzinsuffizienz sollten besonders sorgfältig unter ärztlicher Überwachung stehen.
Leberfunktionsstörungen
Patienten mit Leberfunktionsstörungen können verstärkte oder verlängerte Wirkungen von Nitrendipin aufweisen. Somit sollte die Behandlung mit 10 mg (niedrigste Dosis) begonnen werden und der Behandlungsverlauf sollte regelmäßig überprüft werden. Gegebenenfalls muss bei zu starkem Blutdruckabfall auf andere Präparate umgestiegen werden.
Angina pectoris
Patienten mit bestehender Angina pectoris können vor allem zu Beginn der Behandlung vermehrt und intensiver unter Angina pectoris-Anfällen leiden. Teilweise liegen auch Berichte über aufgetretenen Herzinfarkten vor.
CYP3A4-System
Zu beachten sind Interaktionen mit dem CYP3A4-Enzymsystem (siehe Wechselwirkungen).
Kinder und Jugendliche
Es liegen keine ausreichenden Erfahrungen zur Anwendung bei Kindern und Jugendlichen vor.
Alternativen
Die medikamentöse Behandlung der essenziellen Hypertonie bietet eine breite Palette an blutdrucksenkenden Wirkstoffen. Alternativen sind:
- andere Dihydropyridine wie z.B. Amlodipin, Felodipin, Nifedipin (retard)
- Diuretika
- Beta-Rezeptorblocker
- ACE-Inhibitoren
- AT1-Rezeptorantagonisten
- PDE5-Inhibitoren (pulmonale Hypertonie)
- Alpha-Rezeptorblocker wie z.B. Urapidil
- für Schwangere Alpha-Methyldopa und Dihydralazin
Wirkstoff-Informationen
- Aristo Pharma: Fachinformation Nitrendipin Aristo
- AbZ Pharma: Fachinformation Nitrendipin ABZ
- Bayer: Fachinformation (Bayotensin® akut)
- Freissmuth et al., 2020: Pharmakologie und Toxikologie (3. Auflage)
Abbildung
Dr. Isabelle Viktoria Maucher, Created with Biorender
-
ENEAS® 10 mg/20 mg Tabletten
Trommsdorff GmbH & Co. KG
-
Nitrendipin AbZ 10 mg Tabletten
AbZ Pharma GmbH
-
Nitrendipin AbZ 20 mg Tabletten
AbZ Pharma GmbH
-
Nitrendipin AL 10
ALIUD PHARMA® GmbH
-
Nitrendipin AL 20
ALIUD PHARMA® GmbH
-
Nitrendipin Aristo® 10 mg Filmtabletten
Aristo Pharma GmbH
-
Nitrendipin Aristo® 20 mg Filmtabletten
Aristo Pharma GmbH
-
Nitrendipin-ratiopharm® 10 mg Tabletten
ratiopharm GmbH
-
Nitrendipin-ratiopharm® 20 mg Tabletten
ratiopharm GmbH












