Olaparib
Olaparib ist ein antitumoraler und zytotoxischer Wirkstoff, der zur Behandlung von Ovarialkarzinomen angewendet wird. Olaparib gehört als Hemmstoff des Enzyms Poly-ADP-Ribose-Polymerase zur pharmakotherapeutischen Gruppe der PARP-Inhibitoren.
Olaparib: Übersicht
Anwendung
Der PARP-Hemmer Olaparib (Lynparza) besitzt folgende Anwendungsgebiete:
Ovarialkarzinom
Olaparib wird angewendet als Monotherapie für die:
- Erhaltungstherapie von erwachsenen Patientinnen mit einem fortgeschrittenen (FIGO-Stadien III und IV) BRCA1/2-mutierten (in der Keimbahn und/oder somatisch), high-grade epithelialen Ovarialkarzinom, Eileiterkarzinom oder primären Peritonealkarzinom, die nach einer abgeschlossenen Platin-basierten Erstlinien-Chemotherapie ein Ansprechen (vollständig oder partiell) haben.
- Erhaltungstherapie von erwachsenen Patientinnen mit einem Platin-sensitiven Rezidiv eines high-grade epithelialen Ovarialkarzinoms, Eileiterkarzinoms oder primären Peritonealkarzinoms, die auf eine Platin-basierte Chemotherapie ansprechen (vollständig oder partiell).
Olaparib wird in Kombination mit Bevacizumab angewendet für die:
- Erhaltungstherapie von erwachsenen Patientinnen mit einem fortgeschrittenen (FIGO-Stadien III und IV) high-grade epithelialen Ovarialkarzinom, Eileiterkarzinom oder primären Peritonealkarzinom, die nach einer abgeschlossenen Platin-basierten Erstlinien-Chemotherapie in Kombination mit Bevacizumab ein Ansprechen (vollständig oder partiell) haben und deren Tumor mit einem positiven Status der homologen Rekombinations-Defizienz (HRD) assoziiert ist. Der Status HRD-positiv ist definiert entweder durch eine BRCA1/2- Mutation und/oder genomische Instabilität.
Mammakarzinom
Olaparib wird angewendet:
- als Monotherapie oder in Kombination mit einer endokrinen Therapie für die adjuvante Behandlung von erwachsenen Patienten mit Keimbahn-BRCA1/2-Mutationen, die ein HER2-negatives Mammakarzinom im Frühstadium mit hohem Rezidivrisiko haben und zuvor mit neoadjuvanter oder adjuvanter Chemotherapie behandelt wurden.
- als Monotherapie für die Behandlung von erwachsenen Patienten mit BRCA1/2-Mutationen in der Keimbahn, die ein HER2-negatives, lokal fortgeschrittenes oder metastasiertes Mammakarzinom haben. Die Patienten sollten zuvor mit einem Anthrazyklin und einem Taxan im (neo)adjuvanten oder metastasierten Setting behandelt worden sein, es sei denn, die Patienten waren für diese Behandlungen nicht geeignet. Patienten mit Hormonrezeptor (HR)-positivem Mammakarzinom sollten außerdem eine Krankheitsprogression während oder nach einer vorherigen endokrinen Therapie aufweisen oder für eine endokrine Therapie nicht geeignet sein.
Adenokarzinom des Pankreas
Olaparib wird angewendet:
- als Monotherapie für die Erhaltungstherapie von erwachsenen Patienten mit Keimbahn-BRCA1/2-Mutationen, die ein metastasiertes Adenokarzinom des Pankreas haben und deren Erkrankung nach einer mindestens 16-wöchigen Platin-haltigen Behandlung im Rahmen einer Erstlinien-Chemotherapie nicht progredient war.
Prostatakarzinom
Olaparib wird angewendet:
- als Monotherapie für die Behandlung von erwachsenen Patienten mit metastasiertem kastrationsresistentem Prostatakarzinom (mCRPC) und BRCA1/2-Mutationen (in der Keimbahn und/oder somatisch), deren Erkrankung nach vorheriger Behandlung, die eine neue hormonelle Substanz (new hormonal agent) umfasste, progredient ist.
- in Kombination mit Abirateron und Prednison oder Prednisolon für die Behandlung von erwachsenen Patienten mit mCRPC, bei denen eine Chemotherapie nicht klinisch indiziert ist.
Wirkmechanismus
Olaparib ist ein potenter Inhibitor der humanen Poly(ADP-ribose)-Polymerase-Enzyme (PARP-1, PARP-2 und PARP-3). Der Wirkstoff hemmt als Monotherapeutikum oder in Kombination mit etablierten Chemotherapien in-vitro das Wachstum selektierter Tumorzelllinien und in-vivo das Tumorwachstum.
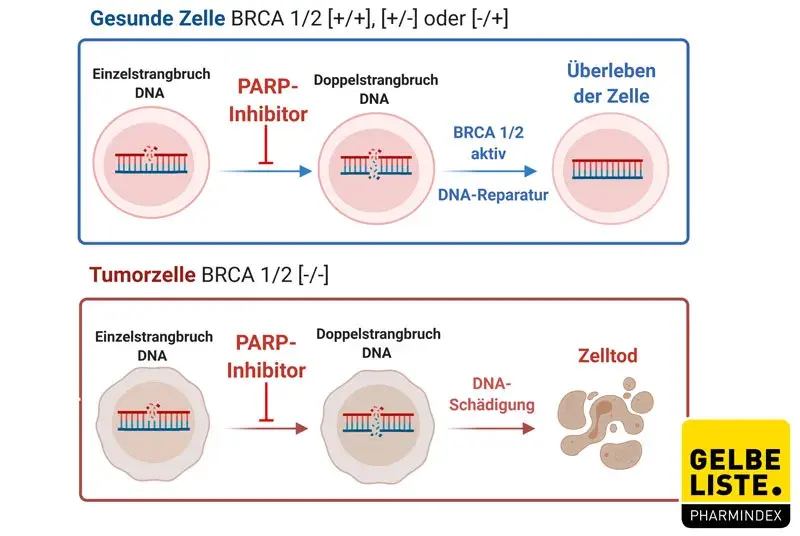
PARP sind an der Reparatur von DNA-Einzelstrangbrüchen beteiligt. Für eine effiziente PARP-induzierte Reparatur ist es erforderlich, dass sich PARP nach der Chromatin-Modifikation automodifizieren und von der DNA dissoziieren. So wird der Zugang für die Basenexzisionsreparatur-(BER)-Enzyme erleichtert. Bindet Olaparib an das aktive Zentrum der DNA-assoziierten PARP, wird die Dissoziation von PARP verhindert. Damit verbleiben die Enzyme fest an der DNA und die Reparatur wird blockiert. Treffen die Replikationsgabeln auf das PARP-DNA-Addukt, kommt es bei replizierenden Zellen zu DNA-Doppelstrangbrüchen (DSBs).
Bei normalen Zellen werden diese DNA-Doppelstrangbrüche durch eine homologe Rekombinationsreparatur (HRR) repariert. Dafür sind funktionelle BRCA1- und 2-Gene erforderlich. Fehlen funktionelle BRCA1- oder 2-Gene jedoch, ist eine DNA-DSBs n-Reparatur durch HRR nicht möglich. Stattdessen werden alternative, fehleranfällige Wege aktiviert. Dazu gehört beispielsweise der non-homologous end joining (NHEJ) pathway. Infolge kommt es zu einer erhöhten genomischen Instabilität. Nach mehreren Replikationsrunden kann die genomische Instabilität so groß werden, dass die Krebszelle abstirbt. Das ist möglich, da Krebszellen im Verhältnis zu normalen Zellen ein höheres Vorkommen von DNA-Schäden aufweisen.
Im Rahmen von BRCA-defizienten in-vivo-Modellen verzögerte Olaparib nach einer Platin-Behandlung, verglichen mit einer Platin-Behandlung allein, die Tumorprogression. Gleichzeitig wurde sie Gesamtüberlebenszeit verlängert.
Pharmakokinetik
Olaparib weist bei 400 mg Wirkstoff zweimal täglich eine apparente Plasma-Clearance von rund 8,6 l/h, ein apparentes Verteilungsvolumen von etwa 167 l und eine terminale Halbwertzeit von 11,9 Stunden auf.
Nach der oralen Aufnahme von Olaparib als Kapsel-Formulierung wird der Wirkstoff rasch resorbiert. Die maximalen Plasmakonzentrationen werden typischerweise 1 bis 3 Stunden nach Einnahme erreicht. Bei Mehrfachdosierung tritt keine nennenswerte Akkumulation auf. Die Steady-state-Konzentrationen werden innerhalb von durchschnittlich 3 bis 4 Tagen erreicht.
Die gleichzeitige Zufuhr von Nahrung verlangsamte die Resorptionsgeschwindigkeit. Dabei wurde die tmax um 2 Stunden verzögert. Das Ausmaß der Resorption von Olaparib stieg marginal an; die AUC war um ca. 20 Prozent erhöht. Der Hersteller empfiehlt, Olaparib mindestens 1 Stunde nach einer Mahlzeit einzunehmen. Danach sollten die Patientinnen möglichst weitere 2 Stunden lang nichts essen.
Dosierung
- Die empfohlene Dosierung beträgt 300 mg (zwei 150-mg-Tabletten) Olaparib zweimal täglich, insgesamt 600 mg pro Tag. Die 100-mg-Tablette kann für Dosisanpassungen verwendet werden.
- Bei PatientInnen mit wiederkehrendem, platin-sensitivem Ovarial-, Eileiter- oder primärem Peritonealkarzinom sollte die Behandlung spätestens acht Wochen nach der letzten platinbasierten Therapie begonnen werden.
- In Kombination mit Bevacizumab wird Olaparib als Erstlinien-Erhaltungstherapie für bestimmte Krebsarten angewendet. Die Bevacizumab-Dosis beträgt 15 mg/kg alle drei Wochen. Für weitere Informationen zu Bevacizumab wird auf die entsprechende Fachinformation verwiesen.
- Bei der Kombination mit endokriner Therapie sollte die empfohlene Dosierung des endokrinen Kombinationspartners gemäß dessen Fachinformation beachtet werden.
- Olaparib kann auch in Kombination mit Abirateron und Prednison oder Prednisolon zur Behandlung von metastasiertem kastrationsresistentem Prostatakarzinom (mCRPC) angewendet werden. Die Dosis von Abirateron beträgt 1000 mg oral einmal täglich, zusammen mit zweimal täglich 5 mg Prednison oder Prednisolon oral. Für weitere Informationen zu Abirateron wird auf die entsprechende Fachinformation verwiesen.
Nebenwirkungen
Sehr häufige Nebenwirkungen:
- verminderter Appetit
- Kopfschmerzen
- Schwindel
- Dysgeusie
- Nausea, Emesis, Diarrhoe, Dyspepsie
- Erschöpfung (einschließlich Asthenie)
- Anämie, Neutropenie, Lymphopenie
- Anstieg der Kreatinin-Konzentration
- Erhöhung des mittleren korpuskulären Volumens.
Häufige Nebenwirkungen:
- Schmerzen im Oberbauch
- Stomatitis
- Thrombozytopenie.
Wechselwirkungen
Klinische Studien zeigten bei der gemeinsamen Gabe von Olaparib und anderen onkologischen Arzneimitteln (einschließlich DNA-schädigender Wirkstoffe) eine Potenzierung und Verlängerung der myelosuppressiven Toxizität. Olaparib wird deshalb ausschließlich zur Monotherapie empfohlen und ist nicht für eine Kombinationstherapie mit anderen onkologischen Arzneimitteln geeignet.
Die gemeinsame Gabe von Olaparib mit Impfstoffen oder Immunsuppressiva wurde nicht untersucht. Sollen diese Arzneimittel gleichzeitig mit Olaparib angewendet werden, ist besondere Vorsicht geboten. Die Patientinnen sollten darüber hinaus engmaschig überwacht werden.
Die gleichzeitige Anwendung von Olaparib und starken oder moderaten CYP3A-Inhibitoren wird nicht empfohlen. Wenn ein starker oder moderater CYP3A-Inhibitor gleichzeitig angewendet werden muss, sollte die Dosis von Olaparib verringert werden.
Ebenso gibt es keine Empfehlungen für die gleichzeitige Anwendung von Olaparib und starken oder moderaten CYP3A-Induktoren. Ist eine Behandlung mit einem starken oder moderaten CYP3A-Induktor unbedingt erforderlich, muss mit einer erheblich reduzierten Wirksamkeit von Olaparib gerechnet werden.
Wird während einer Olaparib-Therapie ein P-gp-Inhibitor benötigt, muss die Patientin sorgfältig hinsichtlich der mit Olaparib assoziierten Nebenwirkungen überwacht werden.
So wirken andere Arzneimittel auf Olaparib
Für die metabolische Clearance von Olaparib sind hauptsächlich die Isoenzyme CYP3A4/5 verantwortlich. Eine klinische Studie zeigte, dass Rifampicin als bekannter CYP3A-Induktor zusammen mit Olaparib die Cmax von Olaparib um durchschnittlich 71 Prozent und die durchschnittliche AUC um 87 Prozent verringerte. Die Wirksamkeit von Olaparib kann also deutlich reduziert sein. Deshalb wird auch keine gemeinsame Anwendung von Olaparib mit starken CYP3A-Induktoren empfohlen. Zu diesen Arzneimitteln gehören unter anderem:
- Phenytoin
- Rifampicin
- Rifapentin
- Carbamazepin
- Nevirapin
- Phenobarbital
- Johanniskraut.
Das Ausmaß des Effekts von moderaten bis starken CYP3A-Induktoren wie Efavirenz und Rifabutin wurde bislang nicht untersucht. Daher wird auch keine gleichzeitige Gabe von Olaparib mit diesen Arzneimitteln empfohlen.
Die gemeinsame Anwendung des CYP3A-Inhibitors Itraconazol mit Olaparib erhöhte die durchschnittliche Cmax von Olaparib 1,42-fach und die durchschnittliche AUC 2,70-fach. Daher wird die kombinierte Anwendung mit starken oder moderaten CYP3A-Inhibitoren nicht empfohlen. Starke CYP3A-Hemmer sind beispielsweise:
Moderate CYP3A-Hemmer sind unter anderem:
Sollten starke oder moderate CYP3A-Inhibitoren gleichzeitig angewendet werden, wird empfohlen, die Dosis von Olaparib zu reduzieren.
In vitro ist Olaparib ein Substrat für den Efflux-Transporter P-gp. Daher können P-gp-Inhibitoren die Olaparib-Exposition erhöhen.
So wirkt Olaparib auf andere Arzneimittel
Olaparib inhibiert in-vitro das Enzym CYP3A4. Es wird angenommen, dass Olaparib auch in vivo ein schwacher CYP3A-Inhibitor ist. Daher ist Vorsicht angezeigt, wenn sensitive CYP3A-Substrate oder Substrate mit einer geringen therapeutischen Breite zusammen Olaparib gegeben werden sollen. Vertreter dieser Gruppe sind beispielsweise:
- Simvastatin
- Cisaprid
- Ciclosporin
- Mutterkornalkaloide
- Fentanyl
- Pimozid
- Sirolimus
- Tacrolimus
- Quetiapin.
Werden solche CYP3A-Substrate mit einer geringen therapeutischen Breite zusammen mit Olaparib gegeben, sollten die Patientinnen entsprechend klinisch überwacht werden.
In-vitro-Untersuchungen mit Olaparib zeigten eine Induktion von CYP1A2, 2B6 und 3A4. Die Induktion von CYP2B6 ist dabei vermutlich von klinisch relevantestem Ausmaß. Eine Induktion von CYP2C9, CYP2C19 und P-gp kann ebenfalls nicht ausgeschlossen werden. Olaparib könnte demnach die Exposition von Substraten dieser Stoffwechselenzyme und Transportproteine reduzieren. Olaparib verringert so möglicherweise auch die Wirksamkeit hormoneller Kontrazeptiva.
Olaparib inhibiert in-vitro den Efflux-Transporter P-gp (IC50 = 76 μM). Demzufolge sind klinisch relevante Wechselwirkungen mit P-gp-Substraten denkbar. Patientinnen, die diese Arzneimittel zusammen mit Olaparib erhalten, sollten entsprechend klinisch überwacht werden. Das gilt unter anderem für:
Olaparib ist in-vitro ein Inhibitor von OATP1B1, OCT1, OCT2, OAT3, MATE1 und MATE2K. Es ist nicht auszuschließen, dass Olaparib in-vivo die Exposition von Substraten der OATP1B1 (zum Beispiel Bosentan, Glibenclamid, Repaglinid, Statine und Valsartan), OCT1 (zum Beispiel Metformin), OCT2 (zum Beispiel Serumkreatinin), OAT3 (zum Beispiel Furosemid und Methotrexat), MATE1 (zum Beispiel Metformin) und MATE2K (zum Beispiel Metformin) erhöhen kann. Besondere Vorsicht wird bei der gleichzeitigen Gabe von Olaparib und Statinen empfohlen.
Kontraindikationen
Bei Überempfindlichkeit gegen den Wirkstoff darf Olaparib nicht eingenommen werden.
Schwangerschaft
Olaparib sollte nicht während der Schwangerschaft und nicht bei Frauen im gebärfähigen Alter, die während der Therapie nicht zuverlässig verhüten, angewendet werden. Frauen im gebärfähigen Alter sollten während der Behandlung mit Olaparib nicht schwanger werden und bei Behandlungsbeginn nicht schwanger sein. Zuverlässige Verhütungsmittel sind noch 1 Monat nach Einnahme der letzten Dosis von Olaparib anzuwenden.
Aufgrund seines Wirkmechanismus als PARP-Inhibitor könnte Olaparib den Fetus schädigen. Präklinische Studien an Ratten zeigten, dass Olaparib negative Auswirkungen auf das embryo-fetale Überleben hat und schwere Missbildungen beim Fetus verursacht.
Bei allen prämenopausalen Patientinnen wird vor Behandlungsbeginn ein Schwangerschaftstest empfohlen. Möglicherweise verringert Olaparib durch eine Enzym-Induktion die Exposition von CYP3A-Substraten und kann so die Wirksamkeit hormoneller Kontrazeptiva beeinträchtigen. Daher werden zusätzliche nicht-hormonelle Kontrazeptionsmethoden empfohlen. Gleichzeitig sind regelmäßige Schwangerschaftstests während der Behandlung mit Olaparib in Betracht zu ziehen.
Stillzeit
Es ist nicht bekannt, ob Olaparib oder seine Metaboliten in die Muttermilch übergehen. Aufgrund der pharmakologischen Eigenschaften von Olaparib darf während Therapie und noch 1 Monat nach Einnahme der letzten Dosis nicht gestillt werden.
Verkehrstüchtigkeit
Olaparib besitzt einen mäßigen Einfluss auf die Verkehrstüchtigkeit und die Fähigkeit zum Bedienen von Maschinen, da Fatigue, Asthenie oder Schwindel mögliche Nebenwirkungen sein können. Patienten, bei denen diese Symptome auftreten, sollten beim Führen von Fahrzeugen oder beim Bedienen von Maschinen vorsichtig sein.
Wichtige Hinweise
- Während der Behandlung mit Olaparib wurden Fälle von leichter oder mäßiger Anämie (CTCAE-Grad 1 oder 2), Neutropenie, Thrombozytopenie und Lymphopenie bekannt. Vor Beginn der Olaparib-Therapie sollten die Konzentrationen von Hämoglobin, Thrombozyten und der Neutrophilen im Normalbereich liegen (bzw. CTCAE-Grad 1 sein).
- Eine Untersuchung des großen Blutbilds wird bei Behandlungsbeginn, nachfolgend in monatlichen Abständen für die ersten 12 Behandlungsmonate und anschließend routinemäßig empfohlen.
- Während der Olaparib-Therapie sollte kein Grapefruitsaft konsumiert werden.
Abbruch der Behandlung
Kommt es zu einer schwerwiegenden hämatologischen Toxizität oder wird eine Patientin Bluttransfusion-pflichtig, sollte die Behandlung mit Olaparib unterbrochen werden. Gleichzeitig ist eine entsprechende hämatologische Untersuchung einzuleiten. Wenn sich die Blutparameter auch nach einer 4-wöchigen Unterbrechung der Behandlung nicht normalisieren, wird eine Analyse des Knochenmarks und/oder eine zytogenetische Blutanalyse empfohlen.
Bei einer kleinen Anzahl von Patientinnen, die Olaparib allein oder in Kombination mit anderen Arzneimitteln gegen Krebserkrankungen erhielten, kam es zu myelodysplastischem Syndrom und/oder akuter myeloischer Leukämie (MDS, AML). Die Mehrzahl der Fälle verlief letal. Alle Patientinnen wiesen Faktoren auf, die potenziell zur Entwicklung von MDS/AML beigetragen haben könnten. Die meisten Betroffenen waren Trägerinnen der gBRCA-Mutation, einige hatten eine vorangegangene Krebserkrankung oder eine Knochenmarksdysplasie in der Anamnese. Alle Patientinnen hatten zuvor Platin-basierte Chemotherapien, eine Strahlentherapie oder andere DNA-schädigende Substanzen erhalten. Ein MDS und/oder eine AML muss entsprechend behandelt werden. Wird eine zusätzliche onkologische Behandlung nötig, sollte Olaparib abgesetzt werden. Die Anwendung in Kombination mit einer anderen onkologischen Therapie wird nicht empfohlen.
Treten neue oder sich verschlechternde Atemwegssymptome wie Dyspnoe, Husten und Fieber auf, sollte die Behandlung mit Olaparib unterbrochen und unverzüglich eine Untersuchung eingeleitet werden. Das gilt ebenso bei radiologischen Anomalien. Bei einer bestätigten Pneumonitis sollte Olaparib abgesetzt und die Patientin entsprechend behandelt werden. Bei einer kleinen Anzahl von Patientinnen verlief die Pneumonitis tödlich. Bislang konnte kein konsistentes klinisches Muster dafür festgestellt werden.
Alternativen
Seit 2020 ist neben Olaparib auch der PARP-Inhibitor Talzenna (Talazoparib) zur Behandlung des Mammakarzinoms verfügbar.
Wirkstoff-Informationen
Fachinformation Lynparza, European Medicines Agency












