Tepotinib
Tepotinib ist ein oraler MET-Inhibitor zur Behandlung von metastasiertem nicht kleinzelligem Lungenkarzinom mit METex14-Skipping Mutation.
Tepotinib: Übersicht
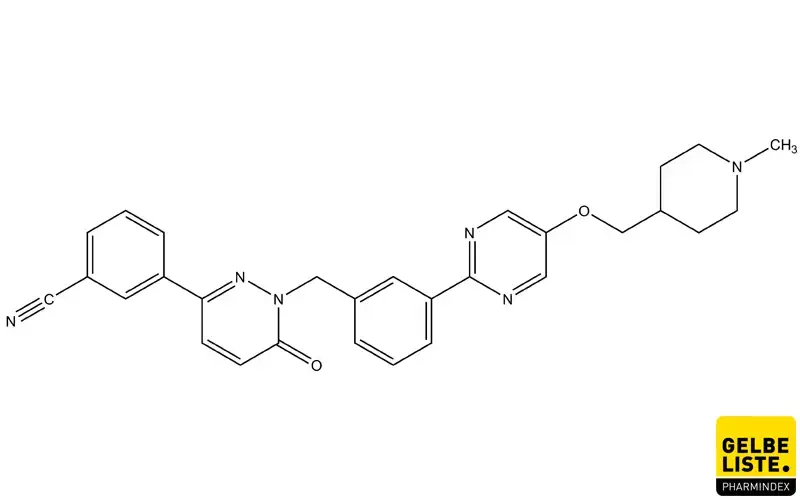
Anwendung
Tepotinib (Tepmetko) ist ein einmal täglich einzunehmender, hochselektiver oraler MET (Mesenchymal-eptihelial Transition Factor)-Inhibitor, der eine vielversprechende klinische Aktivität bei Patienten mit MET-bedingten Tumoren gezeigt hat. Das Medikament ist als Monotherapie indiziert bei erwachsenen Patienten mit einem fortgeschrittenen nicht-kleinzelligem Lungenkrebs (NSCLC) mit Veränderungen, die zu METex14-Skipping (Exon-14-Skipping im mesenchymal-epithelialen Transitionsfaktor-Gen) führen, die eine systemische Therapie nach Platin-basierter Chemotherapie und/oder einer Behandlung mit Immuntherapie benötigen.
Anwendungsart
Tepotinib ist in Form von Filmtabletten für die orale Anwendung auf dem Markt und soll zusammen mit einer Mahlzeit eingenommen werden.
Wirkmechanismus
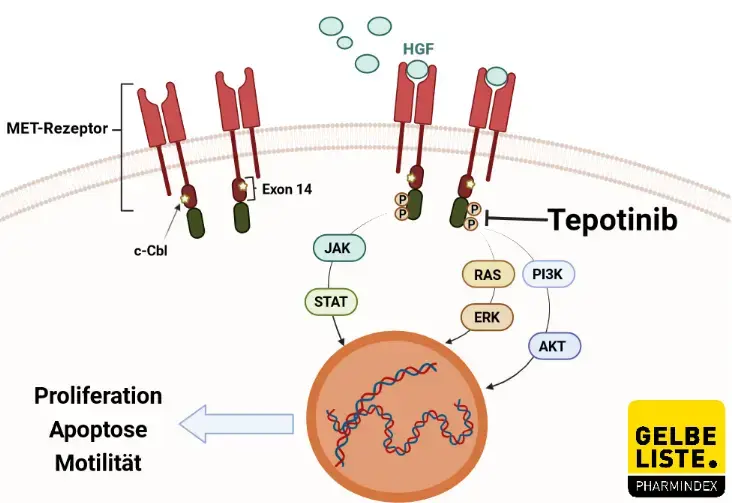
Tepotinib ist ein reversibler kleinmolekularer Adenosintriphosphat-(ATP-)kompetitiver MET-Inhibitor des Typs I. Der Wirkstoff hemmt dosisabhängig die MET-Phosphorylierung und die MET-abhängige nachgelagerte Signaltransduktion über Signalwege der Phosphatidylinositol-3-Kinase/Proteinkinase B (PI3K/Akt) und der mitogenaktivierten Proteinkinase/extrazellulären signalregulierten Kinase (MAPK/ERK).
Dosierung
Die empfohlene Dosis von Tepmetko beträgt 450 mg Tepotinib (2 Tabletten) einmal täglich. Die Behandlung soll so lange fortgesetzt werden, wie ein klinischer Nutzen zu verzeichnen ist.
Wird eine Tagesdosis versäumt, kann deren Einnahme am selben Tag nachgeholt werden, es sei denn, der nächste Einnahmezeitpunkt liegt innerhalb der nächsten 8 Stunden.
Nebenwirkungen
Die häufigsten Nebenwirkungen, die bei ≥20% der Patienten in klinischen Studien mit Tepotinib auftraten, sind:
- Ödeme (77,3%)
- überwiegend peripheres Ödem (65,6%)
- Übelkeit (30,2%)
- Hypoalbuminämie (28,5%)
- Diarrhoe (27,8%)
- Anstieg des Kreatinins (27,1%)
Die häufigsten schwerwiegenden Nebenwirkungen, die bei ≥1% der Patienten beobachtet wurden, sind peripheres Ödem (3,1%), generalisiertes Ödem (2,1%) und interstitielle Lungenerkrankung (ILD) (1,4%). Darüber hinaus wurde über eine begrenzte Anzahl von Patienten mit QTc-Verlängerungen berichtet.
Wechselwirkungen
Bei der Anwendung von Tepotinib soll die gelichzeitige Einnahme von starken CYP- und P-gp-Induktoren oder dualen starken CYP3A- und P-gp-Inhibitoren vermieden werden.
Kontraindikationen
Tepotinib darf nicht angewendet werden bei Überempfindlichkeit gegen den Wirkstoff oder einen der sonstigen Bestandteile des Arzneimittels.
Schwangerschaft
Tepotinib kann den Fötus schädigen, wenn es während der Schwangerschaft angewendet wird. Frauen im gebärfähigen Alter und Männer mit Partnerinnen im gebärfähigen Alter müssen deshalb während der Behandlung mit Tepotinib und bis mindestens eine Woche nach der letzten Dosis eine zuverlässige Verhütungsmethode anwenden.
Stillzeit
Es liegen keine Daten zum Übergang von Tepotinib oder seiner Metaboliten in die Muttermilch oder zu den Auswirkungen auf den gestillten Säugling oder die Milchbildung beim Menschen vor. Das
Stillen soll während der Behandlung mit Tepotinib und bis mindestens eine Woche nach der letzten Dosis unterbrochen werden.
Verkehrstüchtigkeit
Tepotinib hat keinen Einfluss auf die Verkehrstüchtigkeit und die Fähigkeit zum Bedienen von Maschinen.
Anwendungshinweise
Untersuchung des Status von METex14-Skipping-Veränderungen
Wenn das Vorliegen von Veränderungen, die zu METex14-Skipping führen, mittels gewebebasierter oder Blutplasma-basierter Proben festgestellt werden soll, ist es wichtig, einen gut validierten und robusten Test zu verwenden, um falsch negative oder falsch positive Ergebnisse zu vermeiden.
Interstitielle Lungenerkrankung und Pneumonitis
Bei Patienten, die eine Tepotinib-Monotherapie nach dem empfohlenen Dosierungsschema erhalten hatten, wurde über interstitielle Lungenerkrankung (ILD) oder ILD-artige Reaktionen einschließlich Pneumonitis berichtet, die tödlich verlaufen können.
Überwachung der Leberenzyme
Bei Patienten, die eine Tepotinib-Monotherapie nach dem empfohlenen Dosierungsschema erhalten hatten, wurde über einen ALT- und/oder AST-Anstieg berichtet. Die Leberenzyme (ALT und AST) und Bilirubin sind vor Beginn der Behandlung und nachfolgend wie klinisch angezeigt zu überwachen. Falls es zu einem Anstieg auf Grad 3 oder höher (ALT und/oder AST > 5 x ULN) kommt, wird eine Dosisanpassung bzw. ein Behandlungsabbruch empfohlen.
QTc-Verlängerung
Für eine begrenzte Anzahl von Patienten wurden QTc-Verlängerungen berichtet. Bei Patienten mit einem Risiko für eine QTc-Verlängerung, darunter Patienten mit bekannten Elektrolytstörungen oder Patienten unter Behandlung mit Arzneimitteln, die bekanntermaßen QTc-Verlängerungen bewirken können, wird je nach klinischer Indikation eine Überwachung (z. B. mittels EKG, Elektrolytbestimmung) empfohlen.
Embryofetale Toxizität
Tepotinib kann den Fötus schädigen, wenn es während der Schwangerschaft angewendet wird. Bei Frauen im gebärfähigen Alter wird vor Beginn der Behandlung ein Schwangerschaftstest empfohlen. Frauen im gebärfähigen Alter und Männer mit Partnerinnen im gebärfähigen Alter müssen während der Behandlung und bis mindestens eine Woche nach der letzten Dosis eine zuverlässige Verhütungsmethode anwenden.
Interpretation von Laborwerten
In-vitro-Studien deuten darauf hin, dass Tepotinib oder sein Hauptmetabolit die renalen tubulären Transportproteine organischer Kationentransporter (OCT) 2 und Multidrug-and-Toxin-Extrusion-Transporter (MATE) 1 und 2 hemmt. Kreatinin ist ein Substrat dieser Transporter, und ein beobachteter Kreatinin-Anstieg ist möglicherweise eher das Ergebnis einer Hemmung der aktiven tubulären Sekretion als einer Nierenschädigung. Nierenfunktionswerte, die auf Serumkreatinin beruhen (Kreatinin-Clearance oder geschätzte glomeruläre Filtrationsrate), sind unter Berücksichtigung dieses Effekts mit Vorsicht zu interpretieren. Falls es während der Behandlung zu einem Anstieg des Kreatinins im Blut kommt, wird eine weitergehende Beurteilung der Nierenfunktion empfohlen, um eine Nierenfunktionsstörung auszuschließen.
- EMA: Fachinformation Tepmetko
- NEJM: Paul K. Paik, M.D et al.,Tepotinib in Non–Small-Cell Lung Cancer with MET Exon 14 Skipping Mutations, 3. September 2021
- Merck: Tepmetko; METex14 Skipping-Mutation, abgerufen: 14.03.2022
Abbildung
Created with Biorender.com











