Topotecan
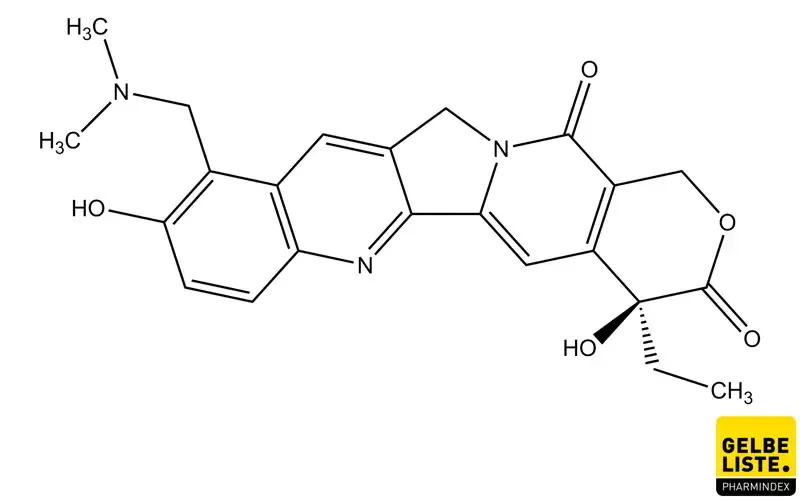
Topotecan ist ein Hemmstoff der DNA-Topoisomerase Typ I, der als Chemotherapeutikum zur Behandlung von Ovarial-, Zervix- und Lungenkarzinom angewendet wird. Topotecan ist ein synthetisches, wasserlösliches Analogon des Alkaloids Camptothecin.
Topotecan: Übersicht
Anwendung
Topotecan ist als Monotherapie indiziert zur Behandlung von:
- metastasierendem Ovarialkarzinom nach Versagen einer Primär- oder Folgetherapie
- rezidiviertem kleinzelligen Lungenkarzinom (SCLC), wenn eine Wiederbehandlung mit dem in der Primärtherapie verwendeten Behandlungsschema nicht geeignet sind.
In Kombination mit Cisplatin wird Topotecan zur Behandlung von Zervixkarzinom im Rezidiv nach Strahlentherapie und bei Stadium IVB der Erkrankung angewendet.
Bevor mit der Behandlung begonnen werden kann, müssen Patienten eine Neutrophilenzahl von ≥ 1,5 x 109/l, eine Thrombozytenzahl von ≥ 100 x 109/l und einen Hämoglobinwert ≥ 9 g/dl
(gegebenenfalls nach Transfusion) aufweisen.
Anwendungsart
Topotecan ist in Form von Hartkapseln sowie als Konzentrat und Pulver zur Herstellung einer Infusionslösung verfügbar.
Wirkmechanismus
In physiologischer Umgebung steht Topotecan im Gleichgewicht mit seiner inaktiven Carboxylatform. Die aktive Lactonform von Topotecan interkaliert zwischen DNA-Basen im Topoisomerase-I-Spaltungskomplex. Die Bindung von Topotecan im Spaltkomplex hindert die Topoisomerase-I daran, den geknickten DNA-Strang wieder zu ligieren. Die Interkalation fängt die Topoisomerase-I in dem an die DNA gebundenen Spaltkomplex ein. Wenn die Replikationsgabel mit der eingeschlossenen Topoisomerase-I kollidiert, kommt es zu DNA-Schäden, die DNA-Replikation wird verhindert und es kommt schließlich zum Zelltod.

Pharmakokinetik
Metabolisierung
Topotecan unterliegt einer reversiblen pH-abhängigen Hydrolyse seiner Lactoneinheit; pharmakologisch aktiv ist die Lactonform.
Elimination
- Die renale Clearance ist ein wichtiger Faktor für die Elimination von Topotecan.
- In einer Massenbilanz-/Ausscheidungsstudie an 4 Patienten mit soliden Tumoren betrug die Gesamtwiederfindung des gesamten Topotecans und seines N-Desmethyl-Metaboliten im Urin und im Stuhl über 9 Tage durchschnittlich 73,4 ± 2,3% der verabreichten i.v.-Dosis.
- Die fäkale Elimination von Gesamt-Topotecan machte 9 ± 3,6% aus, während die fäkale Elimination von N-Desmethyl-Topotecan 1,7 ± 0,6% betrug.
- Die Halbwertzeit beträgt 2-3 Stunden.
Dosierung
Bei der Behandlung von Ovarial- und kleinzelligem Lungenkarzinom beträgt die empfohlene Anfangsdosis Topotecan 1,5 mg/m2 Körperoberfläche pro Tag, verabreicht als 30minütige intravenöse Infusion an fünf aufeinander folgenden Tagen. Zwischen dem Beginn eines Behandlungszyklus und dem Beginn des nächsten sollten drei Wochen liegen. Eine weitere Gabe von Topotecan sollte erst dann erfolgen, wenn die Neutrophilenzahl ≥ 1 x 109/l, die Thrombozytenzahl ≥ 100 x 109/l und der Hämoglobinwert ≥ 9 g/dl (gegebenenfalls nach Transfusion) betragen.
Zur Behandlung des Zervixkarzinoms wird eine Anfangsdosierung von 0,75 mg/m2/Tag Topotecan, verabreicht als 30minütige intravenöse Infusion an den Tagen 1, 2 und 3 empfohlen. Cisplatin wird als intravenöse Infusion in einer Dosis von 50 mg/m2/Tag am Tag 1 nach der Topotecan-Dosis verabreicht. Dieses Behandlungsschema wird alle 21 Tage über sechs Behandlungszyklen oder bis zum Fortschreiten der Erkrankung wiederholt. Eine weitere Gabe von Topotecan sollte erst dann erfolgen, wenn die Neutrophilenzahl ≥ 1,5 x 109/l, die Thrombozytenzahl ≥ 100 x 109/l und der Hämoglobinwert ≥ 9 g/dl (gegebenenfalls nach Transfusion) betragen.
Nebenwirkungen
Unter der Anwendung von Topotecan kann es sehr häufig (≥ 1/10) zu folgenden Nebenwirkungen kommen:
- Infektion
- Febrile Neutropenie, Neutropenie, Thrombozytopenie, Anämie, Leukopenie
- Anorexie (die schwer sein kann)
- Übelkeit, Erbrechen und Durchfall (die alle schwer sein können), der zu einer
- Dehydratation führen kann
- Haarausfall
- Fatigue
Wechselwirkungen
Topotecan hat keinen Einfluss auf CYP450-Enzyme, so dass auch das Interaktionspotenzial des Wirkstoffs recht gering ist. Wenn Topotecan mit anderen Chemotherapeutika kombiniert wird, kann eine Dosisreduktion jedes einzelnen Arzneimittels erforderlich sein, um die Verträglichkeit zu verbessern. In Kombination mit platinhaltigen Arzneimitteln besteht jedoch eine sequenzabhängige Wechselwirkung, abhängig davon, ob das platinhaltige Mittel am Tag 1 oder am Tag 5 der Topotecan-Verabreichung gegeben wird.
Wenn Cisplatin oder Carboplatin am Tag 1 der Topotecan-Verabreichung gegeben wird, müssen niedrigere Dosierungen eines jeden Arzneimittels angewendet werden, um die Verträglichkeit zu verbessern, als wenn das platinhaltige Arzneimittel am Tag 5 der Topotecan-Verabreichung gegeben wird.
Kontraindikationen
Für die Anwendung von Topotecan gelten folgende Gegenanzeigen:
- schwerer Überempfindlichkeit gegen den Wirkstoff oder einen der sonstigen Bestandteile
- bereits vor Beginn des ersten Zyklus bestehende schwere Knochenmarkdepression, bei einer Neutrophilenzahl von < 1,5 x 109/l und/oder Thrombozytenzahl von ≤ 100 x 109/l
- Stillzeit
Schwangerschaft
Wenn Topotecan in der Schwangerschaft angewendet werden muss, oder falls die Patientin unter der Therapie schwanger werden sollte, muss die Patientin vor den möglichen Risiken für den Fetus gewarnt werden.
Verkehrstüchtigkeit
Da unter der Anwendung von Topotecan Fatigue und Asthenie auftreten können, ist beim Führen von Fahrzeugen und Bedienen von Maschinen Vorsicht angezeigt.
Anwendungshinweise
- Wie andere zytotoxische Arzneimittel kann Topotecan zu einer schweren Myelosuppression führen, die zu Sepsis und Todesfällen führen kann. Das Blutbild (einschließlich der Thrombozytenzahl) sollte deshalb bei den Patienten regelmäßig bestimmt werden.
- Topotecan wurde mit Berichten über interstitielle Lungenerkrankungen, von denen einige tödlich verliefen, in Verbindung gebracht. Patienten sollten deshalb auf pulmonale Symptome, die auf eine interstitielle Lungenerkrankung hinweisen können (z. B. Husten, Fieber, Dyspnoe und/oder Hypoxie), überwacht werden.
- Topotecan wird zum Teil renal eliminiert, weshalb eine Nierenfunktionsstörung zu einer erhöhten Exposition von Topotecan führen kann.
- Topotecan kann schwere Diarrhoe auslösen, die eine Hospitalisierung erforderlich machen kann. Der durch eine Antitumortherapie induzierte Durchfall (ATID) ist mit einer signifikanten Morbidität assoziiert und kann lebensbedrohlich sein.
Wirkstoff-Informationen
- Steinhilber, Schubert, Zsilavecz, Roth; Medizinische Chemie 2. Auflage 2010
- Mutschler Mutschler Arzneimittelwirkungen, Pharmakologie – Klinische Pharmakologie – Toxikologie, Begründet von Ernst Mutschler, 11., Auflage 2020, Wissenschaftliche Verlagsgesellschaft Stuttgart
- Fachinformation Hycamtin
Abbildung
Adapted from „DNA Replisome (Eukaryotic Replication)”, by BioRender.com
-
HYCAMTIN® 0,25 mg Hartkapseln
Novartis Pharma GmbH
-
Hycamtin 1 mg Abacus Hartkapseln
Abacus Medicine A/S
-
Hycamtin 1 mg Eurim Hartkapseln
Eurim-Pharm Arzneimittel GmbH
-
HYCAMTIN® 1 mg Hartkapseln
Novartis Pharma GmbH
-
Hycamtin 1 mg Orifarm Hartkapseln
Orifarm GmbH
-
Hycamtin 1 mg SynCo pharma Hartkapseln
SynCo pharma B.V.
-
Topotecan Accord 1 mg/ml Konzentrat zur Herstellung einer Infusionslösung, 1 ml
Accord Healthcare GmbH
-
Topotecan Accord 1 mg/ml Konzentrat zur Herstellung einer Infusionslösung, 4 ml
Accord Healthcare GmbH
-
Topotecan HEXAL® 1 mg/ml Konzentrat zur Herstellung einer Infusionslösung, 1 ml
Hexal AG
-
Topotecan HEXAL® 1 mg/ml Konzentrat zur Herstellung einer Infusionslösung, 3 ml
Hexal AG
-
Topotecan HEXAL® 1 mg/ml Konzentrat zur Herstellung einer Infusionslösung, 4 ml
Hexal AG
-
Topotecan Hikma 4 mg Pulver für ein Konzentrat zur Herstellung einer Infusionslösung
Hikma Pharma GmbH
-
Topotecan medac 1 mg/ml Konzentrat zur Herstellung einer Infusionslösung, 1 ml
medac Gesellschaft für klinische Spezialpräparate mbH
-
Topotecan medac 1 mg/ml Konzentrat zur Herstellung einer Infusionslösung, 2 ml
medac Gesellschaft für klinische Spezialpräparate mbH
-
Topotecan medac 1 mg/ml Konzentrat zur Herstellung einer Infusionslösung, 4 ml
medac Gesellschaft für klinische Spezialpräparate mbH











