Trifaroten
Trifaroten gehört zur Wirkstoffgruppe der Retinoide und ist zugelassen für die topische Behandlung von Acne vulgaris. Der Wirkstoff ist ein selektiver Agonist des Retinsäure-Rezeptors RAR-gamma.
Trifaroten: Übersicht
Anwendung
Trifaroten wird angewendet zur lokalen Therapie der Acne vulgaris im Gesicht und/oder am Rumpf bei Patienten ab 12 Jahren, wenn viele Komedone, Papeln und Pusteln vorhanden sind. Der Wirkstoff wird in Form einer Creme in einer dünnen Schicht einmal täglich abends auf die betroffenen sauberen und trockenen Gesichts- und/oder Körperregionen aufgetragen. Nach einer dreimonatigen Anwendung ist der Behandlungserfolg durch einen Arzt zu überprüfen.
Trifaroten soll nicht auf Schnittwunden, Abschürfungen sowie ekzematöse oder sonnenverbrannte Haut aufgetragen werden.
Anwendungsart
Trifaroten ist in Form einer Creme zur dermalen Anwendung unter dem Handelsnamen Selgamis in Deutschland zugelassen.
Wirkmechanismus
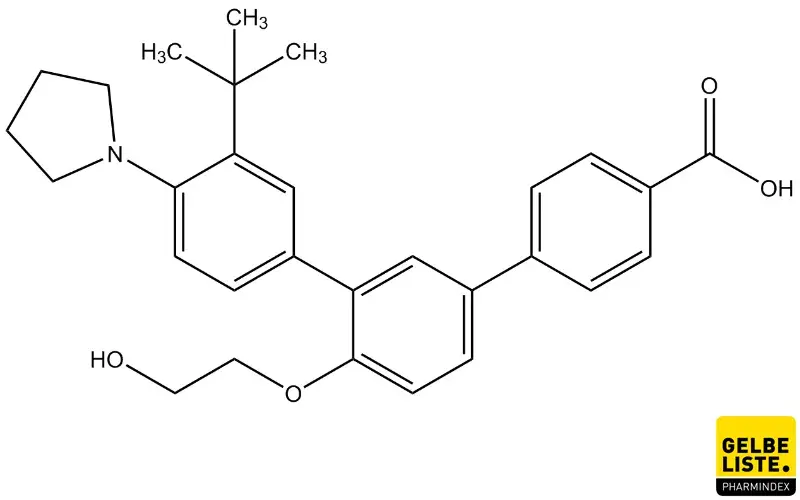
Trifaroten ist ein chemisch stabiles Terphenylsäure-Derivat mit retinoidähnlicher Wirkung. Es ist ein stark wirksamer Agonist am Retinsäure-Rezeptor RARγ, der vor allem in der Haut vorkommt. Trifaroten moduliert außerdem Retinoid-Zielgene in immortalisierten Keratinozyten und rekonstruierter Epidermis.
Pharmakokinetik
Resorption
Nachdem Probanden 30 Tage lang einmal täglich mit 2 g/Tag Selgamis behandelt wurden war der Grad der systemischen Exposition gering und zwischen den erwachsenen und pädiatrischen Populationen vergleichbar. Nach 4-wöchiger Behandlung hatten sieben von neunzehn (37%) erwachsenen Probanden quantifizierbare Trifaroten-Plasmaspiegel. Die Cmax reichte von unterhalb der Bestimmungsgrenze (LOQ < 5 pg/ml) bis 10 pg/ml und die AUC0–24 h von 75 bis 104 pg·h/ml. Drei der siebzehn (18%) pädiatrischen Probanden hatten eine quantifizierbare systemische Exposition. Die Cmax reichte von unterhalb der Bestimmungsgrenze (LOQ < 5 pg/ml) bis 9 pg/ml und die AUC0–24 h von 89 bis 106 pg·h/ml. Steady-State-Bedingungen wurden sowohl bei den erwachsenen als auch bei den pädiatrischen Probanden nach 2-wöchiger topischer Applikation erreicht. Bei Langzeitanwendung ist keine Arzneimittelkumulation zu erwarten.
Verteilung
Trifaroten penetriert in die Haut mit einer Exponentialverteilung vom Stratum corneum zur Epidermis und Dermis. In einer in-vitro-Studie wurde nachgewiesen, dass Trifaroten zu mehr als 99,9% an Plasmaproteine gebunden ist. Es wurde keine signifikante Bindung von Trifaroten an Erythrozyten beobachtet.
Biotransformation
In-vitro-Studien mit humanen hepatischen Mikrosomen und rekombinanten CYP450-Enzymen haben gezeigt, dass Trifaroten hauptsächlich durch CYP2C9, CYP3A4, CYP2C8 und in geringerem Ausmaß durch CYP2B6 metabolisiert wird
Dosierung
Trifaroten wird in einer dünnen Schicht einmal täglich abends auf die betroffenen sauberen und trockenen Gesichts- und/oder Körperregionen aufgetragen. Nach drei Monaten sollte der Arzt den Behandlungserfolg beurteilen.
Nebenwirkungen
Zu den häufigsten möglichen unerwünschten Wirkungen unter der Anwendung von Trifaroten gehören Reizungen und Juckreiz an der Verabreichungsstelle und ein Sonnenbrand.
Wechselwirkungen
Die topische Anwendung von Trifaroten beeiflusste die Konzentration oral verabreichter hormoneller Kontrazeptiva (Ethinylestradiol und Levonorgestrel) im Blut nicht. Andere Wechselwirkungsstudien wurden nicht durchgeführt.
In-vitro-Studien zeigten, dass Trifaroten in Konzentrationen, die systemisch nach topischer Applikation erreicht werden, nicht die CYP450-Isoenzyme CYP1A2, 2B6, 2C8, 2C9, 2C19, 2D6 und 3A4 hemmt und CYP1A2, 2B6 oder 3A4 nicht induziert. Weiterhin hemmte es nicht die Aufnahmetransporter MATE, OATP, OAT oder OCT noch die Effluxtransporter BCRP, PgP, BSEP oder MPR.
Kontraindikation
Trifaroten darf nicht bei bekannter Überempfindlichkeit gegen den Wirkstoff, während der Schwangerschaft oder bei geplanter Schwangerschaft angewendet werden.
Schwangerschaft/Stillzeit
Schwangerschaft
Die orale Anwendung von Retinoiden verursacht kongenitale Fehlbildungen. Bei bestimmungsgemäßer Anwendung wird bei topisch applizierten Retinoiden generell angenommen, dass es aufgrund minimaler dermaler Absorption zu einer niedrigen systemischen Exposition kommt. Es kann jedoch individuelle Faktoren geben (z. B. verletzte Hautbarriere, übermäßiger Gebrauch), die zu einer erhöhten systemischen Exposition beitragen können.
Der Wirkstoff ist deshalb in der Schwangerschaft und bei Frauen, die eine Schwangerschaft planen, kontraindiziert.
Stillzeit
Da ein Risiko für das gestillte Neugeborene/Kind nicht ausgeschlossen werden kann, muss eine Entscheidung darüber getroffen werden, ob das Stillen zu unterbrechen ist oder ob auf die Behandlung verzichtet werden soll. Dabei ist sowohl der Nutzen des Stillens für das Kind als auch der Nutzen der Therapie für die Frau zu berücksichtigen.
Um das Risiko einer Aufnahme durch den Säugling und/oder einer Exposition des Säuglings durch direkten Kontakt zu vermeiden, sollte die stillende Mutter die Trifaroten Creme nicht auf die Brust und den Brustbereich auftragen.
Verkehrstüchtigkeit
Trifaroten hat keinen oder einen zu vernachlässigenden Einfluss auf die Verkehrstüchtigkeit und die Fähigkeit zum Bedienen von Maschinen.
Wirkstoff-Informationen
[1] Fachinformation Selgamis
[2] Clinical Pharmacology Clinical Pharmacology and Safety of Trifarotene, a First‐in‐Class RARγ‐Selective Topical Retinoid











