Vericiguat
Der Wirkstoff Vericiguat stimuliert die lösliche Guanylatzyklase, die ein elementares Enzym des kardiopulmonalen Systems darstellt, und ist indiziert zur Behandlung von chronischer Herzinsuffizienz, da diese mit einer reduzierten Guanylatzyklase-Aktivität assoziiert ist.
Vericiguat: Übersicht

Anwendung
Vericiguat ist indiziert zur Behandlung von symptomatischer, chronischer Herzinsuffizienz bei erwachsenen Patienten mit reduzierter Ejektionsfraktion, die nach einem kürzlich aufgetretenen Dekompensationsereignis, das eine i.v.-Therapie erforderte, stabilisiert wurden.
Anwendungsart
Vericiguat ist in Form von Filmtabletten in folgenden Dosierungen erhältlich:
- 2,5 mg
- 5 mg
- 10 mg
Vericiguat wird üblicherweise mit anderen Herzinsuffizienz-Medikationen kombiniert und zu einer Mahlzeit eingenommen.
Die Filmtabletten können für Patienten, die nicht in der Lage sind, ganze Tabletten zu schlucken, unmittelbar vor der Anwendung zerstoßen und mit Wasser gemischt und anschließend oral verabreicht werden.
Vor Behandlungsbeginn sollte Volumenstatus und Diuretikatherapie optimiert werden, um die Patienten nach dem Dekompensationsereignis zu stabilisieren (insbesondere bei Patienten mit sehr hohen NT-proBNP-Spiegeln).
Falls bei Patienten Verträglichkeitsprobleme auftreten (symptomatische Hypotonie oder systolischer Blutdruck [SBD] unter 90 mmHg), wird eine vorübergehende Dosisreduktion oder das Absetzen von Vericiguat empfohlen.
Die Behandlung sollte nicht bei Patienten mit einem SBD < 100 mmHg begonnen werden.
Wirkmechanismus
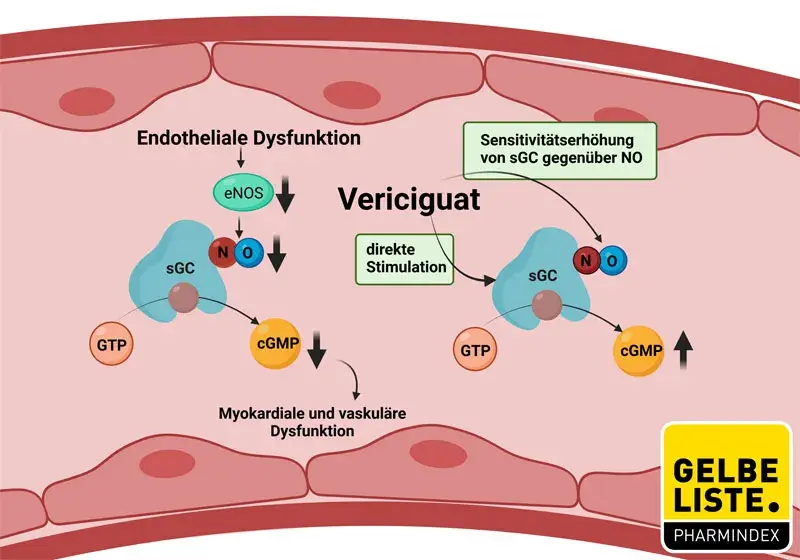
Vericiguat ist ein Stimulator der löslichen Guanylatzyklase (sGC), ein elementares Enzym des kardiopulmonalen Systems, das in der glatten Gefäßmuskulatur nach Stimulation die Umwandlung von GTP in cGMP katalysiert und infolgedessen eine Relaxation induziert. Die sGC ist darüber hinaus das Target von Stickstoffmonoxid (NO) und spielt eine pharmakologische Schlüsselrolle in der Therapie der Angina pectoris mit Nitraten oder Molsidomin.
Intrazelluläres cGMP spielt im Allgemeinen eine wichtige Rolle bei der Regulierung von Prozessen, die Gefäßtonus, Proliferation, Fibrose und Entzündung beeinflussen.
Die Pathophysiologie der Herzinsuffizienz ist mit einer gestörten NO-Synthese und reduzierten sGC-Aktivität assoziiert. Vericiguat stimuliert direkt und unabhängig von NO die sGC, wirkt aber auch in Synergie mit NO fördernd auf den NO-sGC-cGMP-Signalweg. Folglich erhöht sich die Konzentration an intrazellulärem cGMP, was die myokardiale sowie die vaskuläre Funktion verbessern kann.
Pharmakokinetik
Resorption
- Die absolute Bioverfügbarkeit von Vericiguat beträgt bei Einnahme mit einer Mahlzeit etwa 93%.
- Fett- und kalorienreiche Mahlzeiten erhöhen tmax von etwa 1 Stunde (nüchtern) auf etwa 4 Stunden (nach dem Essen), verringern die PK-Variabilität und erhöhen die Exposition gegenüber Vericiguat um 19% (AUC) bzw. 9% (cmax) bei der 5-mg-Tablette und um 44% (AUC) bzw. 41% (cmax) bei der 10-mg-Tablette im Vergleich zum nüchternen Zustand (vergleichbare Ergebnisse mit fettarmen und kohlenhydratreichen Mahlzeiten).
- Die Bioverfügbarkeit (AUC und cmax) von zerstoßenen Tabletten suspendiert in Wasser ist vergleichbar mit der Bioverfügbarkeit von unzerstoßenen Tabletten.
- Die Steady-State-Exposition ist schätzungsweise etwa 20% höher bei Patienten mit Herzinsuffizienz im Vergleich zu gesunden Probanden.
Verteilung
- Vericiguat wird zu etwa 98% an Plasmaproteine gebunden, wobei Serumalbumin den Hauptbindungspartner darstellt.
- Das Verteilungsvolumen im Steady State beträgt ungefähr 44 L.
- Vericiguat reichert sich im Plasma um bis zu 155-171% an und erreicht den pharmakokinetischen Steady State nach ungefähr 6 Tagen.
Metabolismus
- Der maßgebliche Metabolisierungsweg von Vericiguat ist die N-Glucuronidierung (vorwiegend durch UGT1A9 und UGT1A1) zum N-Glucuronid, das allerdings pharmakologisch inaktiv ist.
- Das N-Glucuronid macht dabei etwa 72% der gesamten Arzneimittel-abhängigen AUC aus, während das unveränderte Vericiguat etwa zu 28% der gesamten Arzneimittel-abhängigen AUC beiträgt.
- Die CYP-vermittelte Metabolisierung spielt eine untergeordnete Rolle (< 5%).
Elimination
- Vericiguat weist eine geringe Clearance auf (1,6 L/h bei gesunden Probanden).
- Die Halbwertszeit von Vericiguat beträgt etwa 20 Stunden bei gesunden Probanden und 30 Stunden bei Patienten mit Herzinsuffizienz.
- Ungefähr 53% der oral eingenommenen Dosis werden renal (vornehmlich als N-Glucuronid) und 45% über die Fäzes (vornehmlich als Vericiguat) eliminiert.
Dosierung
- Empfohlene Anfangsdosis: 1x täglich 2,5 mg Vericiguat
- Erhaltungsdosis: 1x täglich 10 mg Vericiguat (nachdem die Anfangsdosis etwa alle 2 Wochen verdoppelt wurde)
Nebenwirkungen
Die meisten Nebenwirkungen unter der Therapie mit Vericiguat lassen sich mit Hilfe des pharmakologischen Wirkmechanismus erklären und werden durch eine Relaxation der glatten Muskelzellen in den Gefäßen oder im Gastrointestinaltrakt verursacht.
Zu den häufigsten Nebenwirkungen zählen:
- Hypotonie (am häufigsten, in etwa 16,4% der Fälle)
- Kopfschmerzen
- Schwindel
- Dyspepsie
- Übelkeit und Erbrechen
- Gastroösophageale Refluxkrankheit (GERD)
- Anämie
Wechselwirkungen
Eine pharmakodynamische Wechselwirkung mit Arzneimitteln, die ebenfalls bei Herzinsuffizienz eingesetzt werden, ist aufgrund der potenzierenden antihypertensiven Effekte in jedem Fall zu berücksichtigen.
Zusätzlich ist bei der Anwendung von Wirkstoffen Vorsicht geboten, die Einfluss auf Vericiguat metabolisierende Enzyme haben (UGT1A9 und UGT1A1):
- UGT1A9/1A1-Inhibitoren: Inhibitoren dieser Enzyme können zu einer erhöhten Vericiguat-Exposition führen.
Kontraindikationen
Vericiguat ist kontraindiziert bei:
- Überempfindlichkeit gegen den Wirkstoff oder sonstige Bestandteile des Arzneimittels
- Gleichzeitiger Anwendung anderer Stimulatoren der löslichen Guanylatzyklase wie Riociguat
Schwangerschaft
Bisher liegen keine Erfahrungen zur Anwendung von Vericiguat bei Schwangeren vor. Allerdings haben tierexperimentelle Studien eine Reproduktionstoxizität bei gleichzeitig auftretender Toxizität für das Muttertier gezeigt. Dementsprechend sollte als Vorsichtsmaßnahme Vericiguat während der Schwangerschaft und bei Frauen im gebärfähigen Alter, die nicht verhüten, nicht angewendet werden.
Stillzeit
Tierexperimentelle Daten deuten darauf hin, dass Vericiguat in die Muttermilch übergehen kann. Aus diesem Grund kann ein Risiko für den Säugling nicht ausgeschlossen werden, weshalb eine Entscheidung darüber getroffen werden muss, ob das Stillen oder ob die Behandlung mit Vericiguat zu unterbrechen ist.
Verkehrstüchtigkeit
Vericiguat kann durch Nebenwirkungen wie Schwindel Einfluss auf die Verkehrstüchtigkeit und die Fähigkeit zum Bedienen von Maschinen haben.
Anwendungshinweise
Symptomatische Hypotonie
- Vericiguat kann, bedingt durch den pharmakologischen Wirkmechanismus, eine symptomatische Hypotonie verursachen.
- Die Möglichkeit einer symptomatischen Hypotonie sollte bei Patienten mit Hypovolämie, schwerer Obstruktion des linksventrikulären Ausflusstraktes, Hypotonie im Ruhezustand, autonomer Dysfunktion, Hypotonie in der Krankengeschichte oder gleichzeitiger Behandlung mit Antihypertensiva, PDE-5-Hemmern oder organischen Nitraten berücksichtigt werden.
- Falls bei Patienten Verträglichkeitsprobleme auftreten (symptomatische Hypotonie oder SBD unter 90 mmHg), wird eine vorübergehende Dosisreduktion oder das Absetzen von Vericiguat empfohlen.
Nieren- und Leberfunktionsstörungen
Patienten mit einer eGFR von < 15 mL/min/1,73 m2 zu Behandlungsbeginn, Dialysepatienten sowie Patienten mit schwerer Leberfunktionsstörung wurden nicht untersucht, weshalb die Behandlung mit Vericiguat in diesen Fällen nicht empfohlen wird.
Alternativen
Zur medikamentösen Therapie der chronischen Herzinsuffizienz stehen in Abhängigkeit von patientenindividuellen Faktoren (z.B. Multimorbidität, Komedikation, NYHA-Klasse, Form der Herzinsuffizienz) diese Alternativen zur Verfügung:
- ACE-Hemmer
- AT1-Antagonisten (Sartane)
- Betablocker
- Aldosteronrezeptor-Antagonisten
- SGLT2-Inhibitoren
- ARNI (Sacubitril/Valsartan)
- Ivabradin
- Diuretika
- Digitalisglykoside
Weitere Informationen sind der jeweiligen Fachinformation zu entnehmen.
Wirkstoff-Informationen
- EMA: Verquvo
- Freissmuth et al., Pharmakologie und Toxikologie, 2020, Springer
- Mutschler et al., Mutschler Arzneimittelwirkungen, 2019, Wissenschaftliche Verlagsgesellschaft Stuttgart
- AWMF: Langfassung Nationale VersorgungsLeitlinie Chronische Herzinsuffizienz (3. Auflage, Version 3, 2021)
-
Verquvo 2,5 mg CC Pharma Filmtabletten
CC Pharma GmbH
-
Verquvo 2,5 mg Emra Filmtabletten
Emra-Med Arzneimittel GmbH
-
Verquvo® 2,5 mg Filmtabletten
Bayer Vital GmbH Geschäftsbereich Pharma
-
Verquvo 2,5 mg kohlpharma Filmtabletten
kohlpharma GmbH
-
Verquvo 2,5 mg Orifarm Filmtabletten
Orifarm GmbH
-
Verquvo 5 mg CC Pharma Filmtabletten
CC Pharma GmbH
-
Verquvo® 5 mg Filmtabletten
Bayer Vital GmbH Geschäftsbereich Pharma
-
Verquvo 5 mg kohlpharma Filmtabletten
kohlpharma GmbH
-
Verquvo 5 mg Orifarm Filmtabletten
Orifarm GmbH
-
Verquvo 10 mg CC Pharma Filmtabletten
CC Pharma GmbH
-
Verquvo 10 mg Eurim Filmtabletten
Eurim-Pharm Arzneimittel GmbH
-
Verquvo® 10 mg Filmtabletten
Bayer Vital GmbH Geschäftsbereich Pharma
-
Verquvo 10 mg kohlpharma Filmtabletten
kohlpharma GmbH
-
Verquvo 10 mg Orifarm Filmtabletten
Orifarm GmbH











