Migalastat
Migalastat wird zur Behandlung der Fabry-Krankheit eingesetzt, einer seltenen lysosomale Speicherkrankheit, die durch Mutationen im GLA-Gen verursacht wird. Diese Mutationen führen zur Akkumulation von Globotriaosylceramid in verschiedenen Organen und Geweben.
Migalastat: Übersicht
Anwendung
Migalastat ist indiziert zur Dauerbehandlung von Erwachsenen und Jugendlichen >/= 12 Jahre mit gesicherter Morbus Fabry-Diagnose (alpha-Galaktosidase A-Mangel), die eine auf die Behandlung ansprechende Mutation aufweisen
Anwendungsart
Migalastat wird zur oralen Einnahme jeden zweiten Tag zur gleichen Uhrzeit empfohlen. Um eine optimale Wirkung zu erzielen, sollte das Medikament auf nüchternen Magen eingenommen werden, was bedeutet, dass mindestens zwei Stunden vor und zwei Stunden nach der Einnahme keine Nahrungsmittel konsumiert werden sollten. In dieser Zeit sind jedoch klare Flüssigkeiten, einschließlich kohlensäurehaltiger Getränke, erlaubt. Die Kapseln sollten unzerkaut und im Ganzen geschluckt werden, ohne sie zu teilen, zu zerkleinern oder zu kauen.
Wirkmechanismus
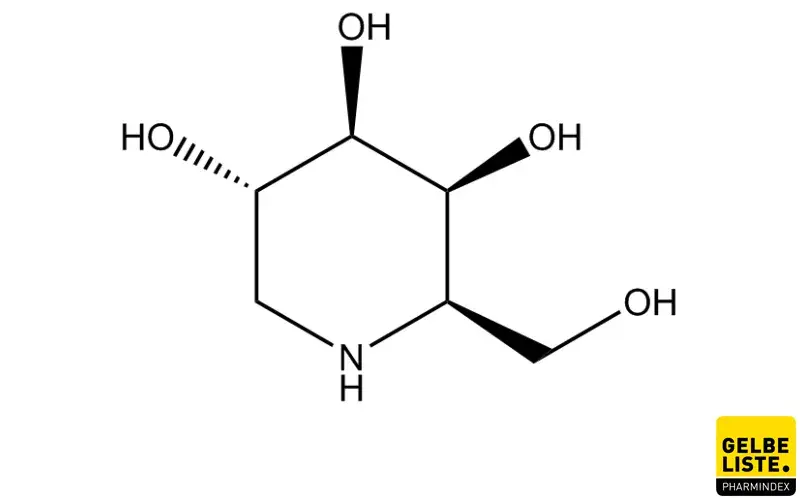
Migalastat wirkt als pharmakologisches Chaperon und wurde entwickelt, um bei bestimmten GLA-Mutationen zu helfen, die zu falsch gefalteten und instabilen α-Galaktosidase A (α-Gal A)-Proteinen führen. Diese Mutationen können zur Fabry-Krankheit führen. Migalastat bindet selektiv und reversibel mit hoher Affinität an die aktiven Zentren der mutierten α-Gal A-Formen, die auf diese Behandlung ansprechen. Die Bindung stabilisiert das mutierte Enzym im endoplasmatischen Retikulum und unterstützt dessen Transport zu den Lysosomen. In den Lysosomen wird die α-Gal A-Aktivität durch das Ablösen von Migalastat wiederhergestellt, wodurch der Abbau von GL-3 (Globotriaosylceramid) und ähnlichen Substraten ermöglicht wird. Nur bestimmte Mutationen sprechen auf die Behandlung mit Migalastat an; diese sind in den Fachinformationen aufgeführt.
Pharmakokinetik
Resorption
- Die absolute Bioverfügbarkeit nach oraler Gabe von 150 mg Migalastathydrochlorid beträgt etwa 75%.
- Der maximale Plasmaspiegel wird ca. drei Stunden nach Einnahme erreicht.
- Die Exposition im Plasma und die maximale Plasmakonzentration steigen dosisproportional bei Dosen von 50 mg bis 1250 mg.
- Nahrungseinnahme, insbesondere fettreiche Mahlzeiten, verringert die Resorption von Migalastat um 37–42%.
Verteilung
- Das Verteilungsvolumen reicht von 77 bis 133 Litern.
- Es wurde keine signifikante Plasmaproteinbindung festgestellt.
Metabolismus
- Migalastat wird nur geringfügig durch UGT (UDP-Glucuronosyltransferase) metabolisiert.
- Es wird nicht durch Cytochrom P450-Enzyme abgebaut, daher sind keine Wechselwirkungen mit diesen Enzymen zu erwarten.
- Etwa 77% der im Plasma nachweisbaren Substanz bestehen aus unverändertem Migalastat, während 13% aus drei Glucuronid-Metaboliten bestehen.
Elimination
- Rund 77% der Dosis werden über den Urin ausgeschieden, wobei 55% davon unverändertes Migalastat sind.
- Etwa 20% der Dosis werden über den Stuhl ausgeschieden.
- Die Eliminationshalbwertszeit beträgt etwa drei bis fünf Stunden.
Besondere Bevölkerungsgruppen
- Patienten mit Niereninsuffizienz: Bei Patienten mit schwerer Niereninsuffizienz (GFR <30 ml/min) war die Exposition um das 4,3-Fache erhöht.
- Leberfunktionsstörung: Es wird nicht erwartet, dass eine beeinträchtigte Leberfunktion die Pharmakokinetik von Migalastat beeinflusst.
- Ältere Patienten (>65 Jahre): Die Clearance unterscheidet sich nur geringfügig (ca. 20%) zwischen Patienten unter und über 65 Jahren.
- Geschlecht: Es gibt keine signifikanten Unterschiede in der Pharmakokinetik zwischen Männern und Frauen.
Dosierung
Empfohlene Dosierung
- Erwachsene und Jugendliche ab 16 Jahren sollten einmal an jedem zweiten Tag 123 mg Migalastat (1 Kapsel) einnehmen, immer zur gleichen Uhrzeit.
Verhalten bei vergessener Dosis
- Wird eine Dosis vergessen, sollte sie nur nachgeholt werden, wenn seit der geplanten Einnahmezeit nicht mehr als zwölf Stunden vergangen sind.
- Bei mehr als zwölf Stunden Verzögerung sollte die nächste Dosis wie gewohnt am nächsten geplanten Dosierungstag eingenommen werden. Es darf keine Dosis an zwei aufeinanderfolgenden Tagen eingenommen werden.
Kinder und Jugendliche
- Die Sicherheit und Wirksamkeit von Migalastat ist bei Kindern unter 16 Jahren nicht belegt, daher gibt es keine Dosierungsempfehlung für diese Altersgruppe.
Ältere Patienten
- Es ist keine Dosisanpassung basierend auf dem Alter erforderlich.
Patienten mit Niereninsuffizienz
- Migalastat wird nicht für Patienten mit einer geschätzten GFR von weniger als 30 ml/min/1,73 m² empfohlen.
Patienten mit Leberfunktionsstörung
- Es ist keine Dosisanpassung bei Patienten mit Leberfunktionsstörungen erforderlich.
Überdosierung
Im Falle einer Überdosierung sollte eine allgemeine medizinische Versorgung erfolgen. Die häufigsten beobachteten Nebenwirkungen bei hohen Dosen von bis zu 1250 mg und 2000 mg waren Kopfschmerzen und Benommenheit.
Nebenwirkungen
Zu den häufigen Nebenwirkungen, die während einer Therapie mit Migalastat auftreten können, zählen:
- Depression
- Kopfschmerzen
- Parästhesie
- Benommenheit
- Hypästhesie
- Schwindelgefühl
- Herzerkrankungen
- Herzklopfen
- Dyspnoe
- Nasenbluten
- Durchfall
- Übelkeit
- Bauchschmerzen
- Verstopfung
- Mundtrockenheit
- Stuhldrang
- Dyspepsie
- Hautausschlag
- Juckreiz
- Muskelspasmen
- Myalgie
- Schiefhals
- Schmerzen in einer Extremität
- Proteinurie
- Müdigkeit
- Schmerzen
- erhöhte Kreatinkinasekonzentration im Blut
- Gewichtszunahme
Wechselwirkungen
Folgende Wechselwirkungen sind bei der Anwendung von Migalastat zu beachten:
- Migalastat ist kein Induktor der Enzyme CYP1A2, 2B6 oder 3A4.
- Es ist kein Inhibitor oder Substrat von CYP-Enzymen wie CYP1A2, 2A6, 2B6, 2C8, 2C9, 2C19, 2D6, 2E1 oder 3A4/5.
- Migalastat ist weder ein Substrat noch ein Inhibitor für die Effluxtransporter MDR1, BCRP oder BSEP.
- Es ist auch kein Substrat für MATE1, MATE2-K, OAT1, OAT3 oder OCT2.
- Migalastat wirkt nicht als Inhibitor der humanen Aufnahmetransporter OATP1B1, OATP1B3, OAT1, OAT3, OCT1, OCT2, MATE1 oder MATE2-K.
Kontraindikationen
Die Anwendung von Migalastat ist generell kontraindiziert bei Überempfindlichkeit gegen den Wirkstoff.
Schwangerschaft
Die Anwendung von Migalastat während der Schwangerschaft wird nicht empfohlen, da nur begrenzte Daten zur Anwendung bei schwangeren Frauen vorliegen. In Tierversuchen mit Kaninchen wurde Entwicklungstoxizität nur bei Dosierungen beobachtet, die für die Mutter toxisch waren. Daher sollte Migalastat während der Schwangerschaft nur mit Vorsicht und nach sorgfältiger Nutzen-Risiko-Abwägung angewendet werden.
Stillzeit
Es ist nicht bekannt, ob Migalastat in die menschliche Muttermilch übergeht. Studien haben jedoch gezeigt, dass der Wirkstoff in die Milch von Ratten ausgeschieden wird. Daher kann ein Risiko für das gestillte Kind nicht ausgeschlossen werden. Es muss individuell abgewogen werden, ob das Stillen oder die Behandlung mit Migalastat unterbrochen werden sollte.
Verkehrstüchtigkeit
Migalastat hat keinen oder nur einen zu vernachlässigenden Einfluss auf die Verkehrstüchtigkeit und die Fähigkeit, Maschinen zu bedienen.
Anwendungshinweise
Bei der Anwendung von Migalastat sind folgende Warnhinweise zu beachten:
- Keine Kombination mit Enzymersatztherapie: Daten zeigen, dass eine gleichzeitige Anwendung von Migalastat und einer Enzymersatztherapie die Exposition gegenüber Agalsidase um das bis zu 5-Fache erhöhen kann. Migalastat ist nicht für den kombinierten Einsatz mit Enzymersatztherapie vorgesehen.
- Regelmäßige Überwachung: Bei Patienten, die mit Migalastat behandelt werden, sollten alle sechs Monate die Nierenfunktion, echokardiographische Parameter und biochemische Marker überprüft werden. Bei klinischer Verschlechterung sollten zusätzliche Untersuchungen oder ein Abbruch der Behandlung in Betracht gezogen werden.
- Indikationseinschränkung: Migalastat ist nur für Patienten mit auf die Behandlung ansprechenden Mutationen geeignet. Es sollte nicht bei Patienten mit nicht ansprechenden Mutationen angewendet werden.
- Proteinurie: Bei mit Migalastat behandelten Patienten wurde kein Rückgang der Proteinurie festgestellt.
- Einschränkung bei Niereninsuffizienz: Migalastat wird nicht für Patienten mit schwerer Niereninsuffizienz (GFR < 30 ml/min/1,73 m²) empfohlen.
Alternativen
Die Fabry-Krankheit kann auch mit Enzymersatztherapien behandelt werden, die das fehlende oder defekte Enzym α-Galaktosidase A ersetzen.
- Freissmuth et al., Pharmakologie und Toxikologie, 2020, Springer
- Fachinformationen ausgewählter Migalastat-Hersteller (z. B. Galafold 123 mg Hartkapseln, Amicus Therapeutics)












