Ribavirin
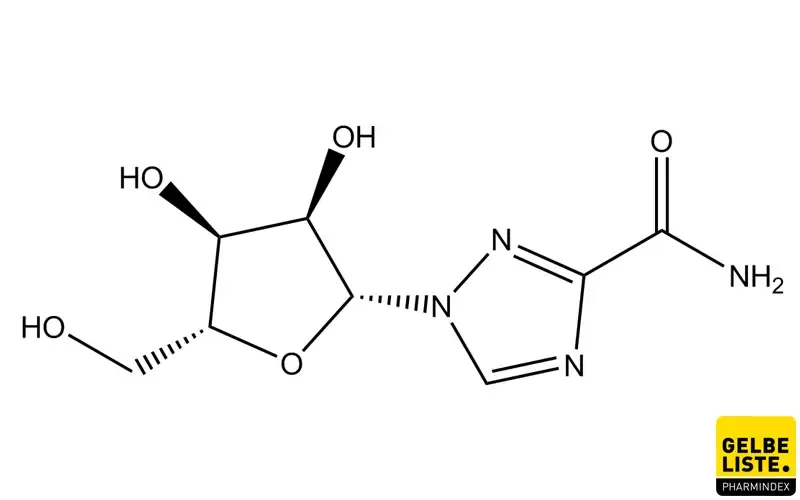
Ribavirin (1-ß-D-Ribofuranosyl-1,2,4-triazol-3-carboxamid) ist ein Guanosin-Nucleosid-Analogon mit antiviralen Breitbandeigenschaften, das erstmals 1972 synthetisiert wurde. Das Virostatikum wird hauptsächlich zur Behandlung der Hepatitis C angewendet.
Ribavirin: Übersicht
Anwendung
Ribavirin ist indiziert zur Behandlung von chronischer Hepatitis C (HCV-Infektion) bei Erwachsenen und darf nur als Teil eines Kombinations-Dosierungsschemas mit Peginterferon alfa-2b oder Interferon alfa-2b angewendet werden.
Unabhängig vom Genotyp sollten alle Patienten, deren HCV-RNA-Serumspiegel in Woche 12 unter der Nachweisgrenze liegen, 48 Wochen lang therapiert werden. Bei erneut behandelten Patienten, die dieses virologische Ansprechen (d. h. HCV-RNA unter der Nachweisgrenze) in Woche 12 verfehlen, ist es unwahrscheinlich, dass sie nach 48 Wochen Therapie ein anhaltendes virologisches
Ansprechen erreichen.
Anwendungsart
Ribavirin ist für die orale Anwendung vorgesehen.
Wirkmechanismus
Ribavirin, das ein Analogon des Nukleosids Guanosin ist, wird innerhalb der Zelle phosphoryliert. Der genaue molekulare Mechanismus, welcher der Wirkung von Ribavirin bei der Behandlung von HCV zugrunde liegt, ist weiterhin unklar. Einer der ersten vorgeschlagenen Wirkmechanismen von Ribavirin ist die starke kompetitive Hemmung der Inosinmonophosphatdehydrogenase (IMPDH) durch Ribavirin-Monophosphat (RMP), die zu einer reduzierten Guanosinmonophosphat-Biosynthese durch die Verringerung der Umwandlung von Inosinmonophosphat zu Xanthosinmonophosphat mit anschließender intrazellulärer Verarmung von GTP führt. Diese Hemmung der IMPDH wurde bereits bei relativ niedrigen Ribavirinkonzentrationen (10 μM Ribavirin) beobachtet und führt zu deutlichen Veränderungen im Gleichgewicht der intrazellulären Nukleotidkonzentrationen. Diese Veränderungen im Nukleotidpool in Zellen können sekundär einen großen Einfluss auf die Wirtszell- und virale Genexpression sowie auf die virale Replikation haben.
Ein weiterer forgeschlagener Mechanismus ist, dass RTP als kompetitiver Inhibitor für das Capping von mRNAs wirkt, was anschließend zu einer beeinträchtigten Translation führt, indem es ein kovalentes RMP-Capping-Enzym-Zwischenprodukt anstelle des normalerweise beobachteten Guanosinmonophosphat-Enzym-Zwischenprodukts bildet. Eukaryotische mRNAs und viele virale mRNAs enthalten umfangreiche Modifikationen am 5'-Ende (bekannt als "Fünf-Prime-Kappe"), wobei häufig Guanin verwendet wird, das in Position 7 methyliert ist, da dies für die Stabilität und effiziente Translation von mRNA wesentlich ist. Somit hat das RNA-Capping einen großen sekundären Einfluss auf die Translation von sowohl viralen als auch Wirtszell-mRNAs.
Pharmakokinetik
Resorption
- Ribavirin wird nach oraler Anwendung rasch resorbiert (mittlereTmax = 1,5 Stunden) und verteilt.
- die Halbwertszeiten für eine Einzeldosis betragen für die Resorption 0,05 Stunden, für die Verteilung 3,73 Stunden und für die Eliminierung 79 Stunden.
- Ribavirin wird umfassend resorbiert, wobei ca. 10% einer radioaktiv markierten Dosis mit den Fäzes ausgeschieden werden.
- Die absolute Bioverfügbarkeit beträgt ca. 45 – 65%, was auf einen First-Pass-Metabolismus zurückzuführen zu sein scheint.
- Das Verteilungsvolumen beträgt ungefähr 5.000 l.
- Ribavirin bindet nicht an Plasmaproteine.
Verteilung
- Der Transport von Ribavirin in Nicht-Plasma-Kompartiment wurde sehr ausgiebig an Erythrozyten untersucht.
- Es wurde nachgewiesen, dass er primär über einen äquilibrierenden Nukleosid-Transporter des es-Typs erfolgt. Dieser Transportertyp ist praktisch auf allen Zelltypen vorhanden und könnte für das hohe Verteilungsvolumen von Ribavirin verantwortlich sein.
- Das Verhältnis zwischen Vollblut- und Plasma-Ribavirin-Konzentration beträgt annähernd 60:1.
- Der überwiegende Anteil des gesamten Ribavirins im Blut liegt in Form von Ribavirin-Nukleotiden in Erythrozyten vor.
Biotransformation
- Die Metabolisierung von Ribavirin erfolgt über reversible Phosphorylierung und durch einen Abbauweg mit Deribosylierung und Amidhydrolyse, so dass ein Triazolcarbonsäure-Metabolit entsteht.
- Ribavirin sowie seine Triazolcarbamid- und Triazolcarbonsäure-Metaboliten werden ebenfalls über die Niere ausgeschieden.
- Nach oralen Einzeldosen wiesen die pharmakokinetischen Größen von Ribavirin eine hohe inter- und intraindividuelle Variabilität (intraindividuelle Variabilität von etwa 30% bei AUC und Cmax) auf.
Elimination
- Bei Mehrfachdosierung kumuliert Ribavirin ausgiebig im Plasma wobei AUC12h der Mehrfachdosis das 6-fache der Einzeldosis beträgt.
- Nach oraler Einnahme von 2 × 600 mg/Tag wurde der Steady State nach ca. vier Wochen erreicht, wobei die mittleren Plasmakonzentrationen im Steady State ungefähr 2.200 ng/ml betrugen.
- Nach Absetzen der Therapie betrug die Halbwertszeit ungefähr 298 Stunden, was wahrscheinlich die langsame Eliminierung aus den Nicht-Plasma-Kompartimenten widerspiegelt.
Dosierung
Die Dosierung von Ribavirin richtet sich nach dem Körpergewicht des Patienten. Der Wirkstoff muss entweder in Kombination mit Peginterferon alfa-2b (1,5 µg/kg/Woche) oder Interferon alfa-2b (3 Mio I.E. dreimal in der Woche) angewendet werden. Die Wahl der Kombinations-Dosierungsschemata hängt von der Charakteristik des Patienten ab und sollte auf der erwarteten Wirksamkeit und Unbedenklichkeit der Kombinationsbehandlung für den individuellen Patienten basieren.
- Bei einem Gewicht unter 65 kg beträgt die tägliche Ribavirin-Dosis 800 mg
- Bei einem Gewicht von 65 – 80 kg beträgt die tägliche Ribavirin-Dosis 1.000 mg
- Bei einem Gewicht von 81 – 105 kg beträgt die tägliche Ribavirin-Dosis 1.200 mg
- Bei einem Gewicht von über 105 kg beträgt die tägliche Ribavirin-Dosis 1.400 mg
Nebenwirkungen
Die Hauptnebenwirkung von Ribavirin ist die hämolytische Anämie mit einer mittleren Hämoglobinabnahme von etwa 20 g/l während der Behandlung. Aufgrund der mit Anämie verbundenen Risiken bei Patienten mit anamnestischer oder bestehender Herzerkrankung ist Ribavirin bei diesen Patienten kontraindiziert. Abgesehen von Anämie ist Ribavirin auch mit einem erhöhten Risiko für Juckreiz, Hautausschlag, Husten sowie neuropsychiatrischen Nebenwirkungen, beispielsweise Schlaflosigkeit, verbunden.
Wechselwirkungen
Da Ribavirin einen inhibitorischen Effekt auf die Inosin-Monophosphat-Dehydrogenase hat, kannes mit dem Metabolismus von Azathioprin interferieren und möglicherweise zu einer Akkumulation von 6-Methylthioinosin-Monophosphat führen, die mit der Myelotoxizität bei Patienten, die mit Azathioprin behandelt werden, in Zusammenhang gebracht wurde.
Darüber hinaus wird die Bioverfügbarkeit von Ribavirin durch die gleichzeitige Anwendung eines Magnesium-, Aluminium- und Simethicon-haltigen Antazidums vermindert. Die
verminderte Bioverfügbarke wird auf eine verzögerte Passage von Ribavirin oder einen veränderten pH-Wert zurückgeführt. Diese Wechselwirkung wird jedoch als klinisch nicht relevant angesehen.
Die Anwendung von Nukleosid-Analoga allein oder in Kombination mit anderen Nukleosiden, führte zu Laktatazidose. In vitro erhöht Ribavirin pharmakologisch die phosphorylierten Metaboliten von Purin-Nukleosiden. Diese Aktivität könnte das Risiko einer Purin-Nukleosid-Analoga (z. B. Didanosin oder Abacavir) induzierten Laktatazidose erhöhen. Die gleichzeitige Anwendung wird
deshalb nicht empfohlen.
Wenn Zidovudin Bestandteil eines HIV-Behandlungsschemas war, wurde über die Verschlechterung einer Anämie aufgrund von Ribavirin berichtet. Der genaue Mechanismus ist nicht bekannt.
Es gibt keine Hinweise darauf, dass Ribavirin Wechselwirkungen mit nicht-nukleosidischen Reverse Transkriptase-Inhibitoren oder Protease-Inhibitoren eingeht. In der Literatur finden sich widersprüchliche Aussagen bezüglich der gleichzeitigen Anwendung von Abacavir und Ribavirin: Einige Daten weisen darauf hin, dass HIV/HCV co-infizierte Patienten, die eine ART mit Abacavir erhalten, möglicherweise eine geringere Ansprechrate auf eine Therapie mit pegyliertem Interferon/Ribavirin haben. Eine gleichzeitige Therapie mit beiden Arzneimitteln sollte unter besonderer Vorsicht erfolgen.
Kontraindikationen
Ribavirin darf nicht angewendet werden bei:
- Überempfindlichkeit gegen den Wirkstoff oder einen der genannten sonstigen Bestandteile des Arzneimittels
- Schwangerschaft und Stillzeit
- anamnestisch vorbestehender schwerer Herzkrankheit, einschließlich instabile oder nicht beherrschte Herzerkrankung in den letzten sechs Monaten
- schweren, stark schwächenden Erkrankungen
- chronischer Niereninsuffizienz
- Kreatinin-Clearance < 50 ml/Minute und/oder dialysepflichtigen Patienten
- schwerer Leberfunktionsstörung (Child-Pugh Klassifikation B oder C) oder dekompensierter Leberzirrhose
- Hämoglobinopathien (z. B. Thalassämie, Sichelzellenanämie).
Kinder und Jugendliche:
- Bestehende oder in der Vorgeschichte bekannte schwere psychiatrische Störungen, insbesondere schwere Depression, Selbstmordgedanken oder Selbstmordversuch.
Schwangerschaft
Angesichts der potenziellen Teratogenität, die in Tiermodellen nachgewiesen wurde, ist Ribavirin während der Schwangerschaft und Stillzeit kontraindiziert. Es wird daher empfohlen, eine Schwangerschaft für vier Monate nach Ribavirin-Exposition bei behandelten Frauen und für sieben Monate bei weiblichen Partnern von behandelten Männern zu vermeiden.
Verkehrstüchtigkeit
Ribavirin hat keinen oder einen zu vernachlässigenden Einfluss auf die Verkehrstüchtigkeit und die Fähigkeit zum Bedienen von Maschinen. Aber das in Kombination gegebene Peginterferon alfa-2b oder Interferon alfa-2b kann eine Wirkung haben. Daher müssen Patienten, bei denen während der Behandlung Müdigkeit, Schläfrigkeit oder Verwirrtheit auftritt, vorsichtig sein und das Führen von Fahrzeugen oder Bedienen von Maschinen unterlassen.
Alternativen
Eine interferonbasierte Therapie entspricht heute nicht mehr dem Therapiestandard. Aufgrund der vielen Neuzulassung direkt antiviral wirkender Substanzen ändern sich die aktuellen Empfehlungen zur Therapie der Hepatitis C rasch. Bis zum Jahr 2013 wurde die Therapie der akuten Hepatitis C mit (pegylierten) Interferonen durchgeführt. Hiermit konnten mit einer 12- bis 24-wöchigen Behandlung Ausheilungen der Infektion in 82%-100% der Fälle erreicht werden. Allerdings ist die Behandlung mit Nebenwirkungen assoziiert, die in Häufigkeit und Schwere mit der chronischen Hepatitis C vergleichbar sind.
In Anbetracht der Verfügbarkeit von deutlich nebenwirkungsärmeren Interferon-freien antiviralen Therapien gegen HCV ist ein Einsatz von pegylierten Interferonen zur Therapie der akuten Hepatitis C nicht mehr gerechtfertigt. Eine akute Hepatitis C vom HCV-Genotyp 1 kann beispielsweise durch eine Behandlung mit Ledipasvir/Sofosbuvir für 6 Wochen ausgeheilt werden.
Wirkstoff-Informationen
- Reddy KR, Nelson DR, Zeuzem S. Ribavirin: current role in the optimal clinical management of chronic hepatitis C. J Hepatol. 2009 Feb;50(2):402-11. doi: 10.1016/j.jhep.2008.11.006
- Fachinformation Ribavirin ratiopharm
-
S3-Leitlinie „Prophylaxe, Diagnostik und Therapie der Hepatitis-C-Virus (HCV)-Infektion“, AWMF-Register-Nr.: 021/012












