Rituximab
Rituximab ist ein monoklonaler Antikörper der ein Protein namens CD20 auf der Oberfläche von B-Lymphozyten erkennt, daran bindet und so die Zelle abtötet. Das Biological weist ein breites Indikationsspektrum in der Onkologie und Rheumatologie auf wie bspw. die Behandlung der chronisch lymphatischen Leukämie sowie der rheumatoiden Arthritis.
Rituximab: Übersicht
Anwendung
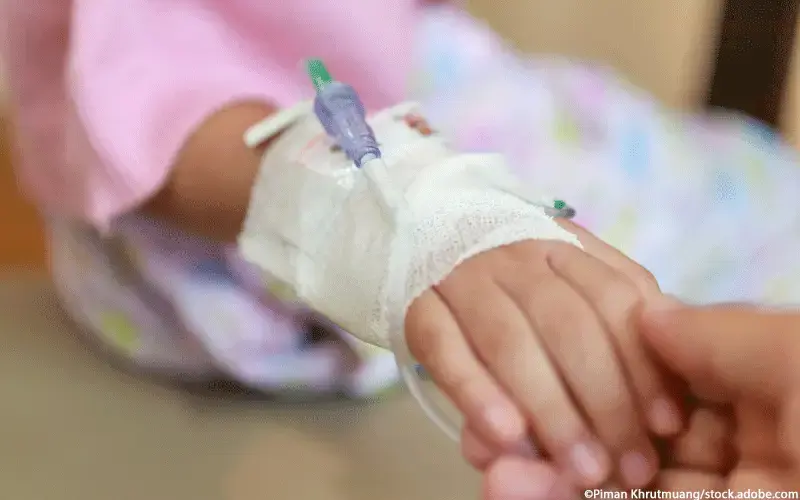
Medikamente mit dem Wirkstoff Rituximab werden hauptsächlich zur Therapie von Autoimmunerkrankungen und bestimmter Krebsarten eingesetzt. Bei einigen malignen B-Zell-Erkrankungen kann Rituximab hohe Response-Raten und Langzeit-Remissionen induzieren.
Indikationen als Monotherapeutikum:
- Non-Hodgkin-Lymphom
- Chronisch lymphatische Leukämie
- Rheumatoide Arthritis
- mittelschwerer bis schwerer Pemphigus vulgaris (PV)
Als Kombination zu einer Chemotherapie ist Rituximab-Gabe indiziert bei:
- Erstbehandlung eines follikulären Lymphoms im Stadium III – IV
- CD20-positivem, diffusem großzelligen B-Zell-Non-Hodgkin-Lymphom
Hinweise
Eine vollständige Ausrüstung zur Wiederbelebung sollte sofort verfügbar sein. Die Etiketten des Arzneimittels sind zu überprüfen, um sicherzustellen, dass der Patient die richtige, ihm verschriebene Darreichungsform (intravenöse oder subkutane Darreichungsform) und Stärke erhält.
Wirkmechanismus
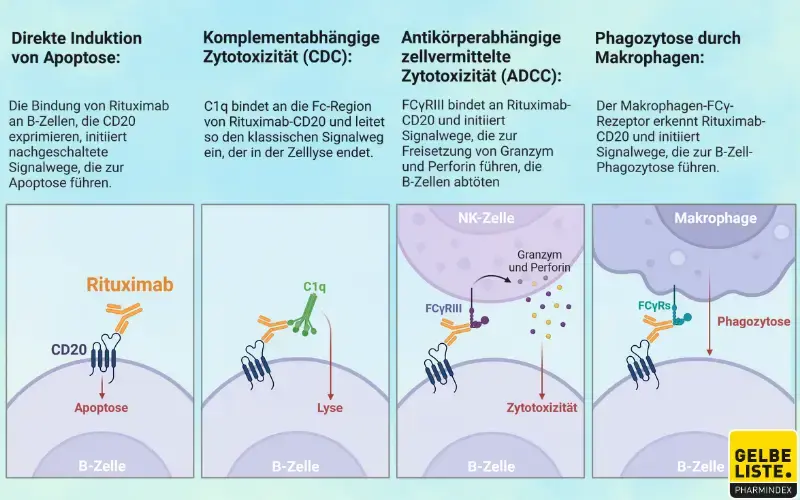
Rituximab bindet an ein Oberflächenprotein, das sogenannte CD20-Antigen, welches auf der Oberfläche von B-Zellen und B-Zell-Lymphomen exprimiert wird. CD20 ist auf > 95% aller Zellen von Non-Hodgkin-Lymphomen des B-Zell-Typs vorhanden. Durch die Bindung von Rituximab an CD20 werden verschiedene zelluläre Reaktionen auslöst, darunter:
- Antikörperabhängige zellvermittelte Zytotoxizität (ADCC): Natürliche Killerzellen erkennen den Fc-Bereich von Rituximab und töten die B-Zelle ab.
- Komplementabhängige Zytotoxizität (CDC): Durch die Bindung von Rituximab an CD20 wird das Komplementsystem aktiviert, was zur Lyse der B-Zelle führt.
- Direkte Induktion von Apoptose: Durch die Bindung von Rituximab an CD20 können intrazelluläre Signalwege aktiviert werden, die zum programmierten Zelltod führen.
- Phagozytose durch Makrophagen: Makrophagen können B-Zellen, an die Rituximab gebunden ist, erkennen und phagozytieren.
Da Stammzellen im Knochenmark kein CD20-Antigen exprimieren, werden diese durch den Wirkstoff nicht zerstört.
Pharmakokinetik
- Die Resorption von Rituximab ist nach subkutaner Anwendung langsam und erreicht nach ca. 3 Tagen eine maximale Plasmakonzentration.
- Die absolute Bioverfügbarkeit wird auf 71% geschätzt.
- Die mediane terminale Eliminationshalbwertszeit nach subkutaner Injektion wird mit 29,7 Tagen angegeben (individuell sehr unterschiedlich).
Dosierung
Die Dosierungsempfehlungen von Rituximab unterscheiden sich je nach Indikation und können der jeweiligen Fachinformation entnommen werden.
Prämedikation
Vor jeder Anwendung von Rituximab in beiden Darreichungsformen sollte immer eine Prämedikation stattfinden. Dabei sollte als Analgetikum/Antipyretikum z. B. Paracetamol und als Antihistaminikum z. B. Diphenhydramin verabreicht werden.
Glucocorticoide sollten verabreicht werden, wenn Rituximab nicht in Kombination mit einer Chemotherapie zur Behandlung eines Non-Hodgkin-Lymphoms oder einer chronischen lymphatischen Leukämie verabreicht wird, die ein Glucocorticoid enthält.
Arzneimittel zur Prophylaxe bei der intravenösen Anwendung
Verminderung des Risikos eines Tumorlysesyndroms:
Bei Patienten mit einer chronisch lymphatischen Leukämie 48 Stunden vor Behandlungsbeginn wird eine Prophylaxe mit einer adäquaten Hydratation und die Gabe von Urikostatika empfohlen.
Verringerung der Häufigkeit und den Schweregrad akuter Infusionsreaktionen und/oder eines Zytokin-Freisetzungs-Syndroms:
Bei Patienten mit einer chronisch lymphatischen Leukämie, die eine Lymphozytenzahl von > 25 x 109/l aufweisen, wird die intravenöse Gabe von 100 mg Prednison/Prednisolon kurz vor der Infusion von Rituximab empfohlen.
Verringerung der Häufigkeit und den Schweregrad infusionsbedingter Reaktionen:
Patienten mit rheumatoider Arthritis, Granulomatose mit Polyangiitis (Wegenersche Granulomatose) oder mikroskopischer Polyangiitis sollten während der Krankheitsremission oder Pemphigus vulgaris eine intravenöse Gabe von 100 mg Methylprednisolon erhalten, die 30 Minuten vor der Infusion von Rituximab beendet sein muss.
Bei Patienten mit Granulomatose mit Polyangiitis (Wegenersche Granulomatose) oder mikroskopischer Polyangiitis wird empfohlen, vor der ersten Infusion von Rituximab, Methylprednisolon intravenös für drei Tage in einer Dosierung von 1.000 mg pro Tag zu verabreichen (die letzte Dosis von Methylprednisolon kann am selben Tag wie die erste Rituximab-Infusion sein). Danach soll während und nach der 4-wöchigen Induktionstherapie mit Rituximab orales Prednison 1 mg/kg/Tag verabreicht werden (max. 80 mg/Tag), das je nach klinischer Notwendigkeit so schnell wie möglich ausschleichend abgesetzt werden sollte.
Prophylaxe gegen Pneumocystis jirovecii-Pneumonie:
Bei Patienten mit Granulomatose mit Polyangiitis (Wegenersche Granulomatose), mikroskopischer Polyangiitis oder Pemphigus vulgaris wird während und nach der Behandlung mit Rituximab, falls erforderlich, eine Prophylaxe gemäß lokalen klinischen Empfehlungen empfohlen.
Nebenwirkungen
Sehr häufig treten unter der Behandlung mit Rituximab folgende Nebenwirkungen auf:
- Bakterielle und virale Infektionen
- Erkrankungen des Blutes und des Lymphsystems
- Infusionsbedingte Reaktionen
- Angioödem
- Übelkeit
- Pruritus, Exanthem, Alopezie
- Fieber, Schüttelfrost, Asthenie, Kopfschmerzen
Wechselwirkungen
Folgende Wechselwirkungen müssen vor der Anwendung von Rituximab beachtet werden:
- Blutdrucksenkende Medikamente sollten 12 Stunden vor der Anwendung abgesetzt werden, da es unter Rituximab-Gabe zu einem Blutdruckabfall kommen kann.
- Bei vorbestehenden Herzerkrankungen oder einer kardiotoxischen Chemotherapie sollen Patienten engmaschig überwacht werden.
- Eine gleichzeitige Impfung mit viralen Lebendimpfstoffen wird nicht empfohlen.
Kontraindikationen
Rituximab darf nicht angewendet werden bei:
- Überempfindlichkeit gegen den Wirkstoff
- Aktive, schwere Infektionen (wie z.B. Tuberkulose, Sepsis und opportunistische Infektionen)
- Patienten mit stark geschwächtem Immunsystem
Schwangerschaft
Rituximab sollte nur nach Nutzen-Risiko-Abwägung bei Schwangeren angewendet werden. Immunglobuline der Klasse G können die Plazentaschranke passieren. Es liegen jedoch keine hinreichenden und gut kontrollierten Daten aus Studien bei schwangeren Frauen vor. Bei einigen Kindern, deren Mütter während der Schwangerschaft Rituximab erhielten, wurde über eine vorübergehende B-Zell-Depletion und Lymphozytopenie berichtet.
Stillzeit
Frauen sollten während und weitere 12 Monate nach der Behandlung mit Rituximab nicht stillen, da mütterliche IgG in die Milch übertreten und Rituximab in der Milch säugender Affen nachgewiesen wurde.
Verkehrstüchtigkeit
Nach der Verabreichung von Rituximab kann Schwindel auftreten, daher kann Rituximab einen geringen Einfluss auf die Verkehrstüchtigkeit und die Fähigkeit zum Bedienen von Maschinen haben. Es wurden jedoch keine Studien zu den Auswirkungen von Rituximab auf die Verkehrstüchtigkeit und die Fähigkeit zum Bedienen von Maschinen durchgeführt.
Anwendungshinweise
- Das größte Risiko von anwendungsbedingten Reaktionen besteht normalerweise während des ersten Behandlungszyklus.
- Die medianen IgG-Serumspiegel werden durch den Wirkstoff reduziert.
- Patienten müssen regelmäßig auf neu auftretende oder sich verschlechternde neurologische Symptome bzw. auf Anzeichen, die auf eine progressive multifokale Leukoenzephalopathie (PML) hindeuten, überwacht werden.
- Seit Markteinführung wurde von schweren infusionsbedingten Reaktionen mit tödlichem Ausgang berichtet.
- Während der Behandlung sollten regelmäßige Kontrollen des großen Blutbildes erfolgen.
- Frauen im gebährfähigen Alter müssen während und 12 Monate nach der Behandlung mit Rituximab wirksame kontrazeptive Methoden anwenden.
Alternativen
Es gibt Situationen, in denen Rituximab entweder nicht wirksam ist, nicht vertragen wird oder aus anderen Gründen nicht die erste Wahl darstellt. In solchen Fällen können verschiedene Behandlungsalternativen in Betracht gezogen werden. Die Wahl der Alternative hängt von der spezifischen Indikation, der Krankheitsaktivität und dem individuellen Patientenprofil ab.
Wirkstoff-Informationen
- Fachinformation Rixathon® 500 mg Konzentrat zur Herstellung einer Infusionslösung
- Fachinformation Rixathon® 100 mg Konzentrat zur Herstellung einer Infusionslösung
- Fachinformation MabThera® 1.400 mg Lösung zur subkutanen Injektion
- Fachinformation MabThera® 100 mg Konzentrat zur Herstellung einer Infusionslösung
- Fachinformation MabThera® 500 mg Konzentrat zur Herstellung einer Infusionslösung
- Fachinformation Truxima® 100 mg Konzentrat zur Herstellung einer Infusionslösung
- Fachinformation Truxima® 500 mg Konzentrat zur Herstellung einer Infusionslösung
Abbildung
Dr. Isabelle Viktoria Maucher, Created with Biorender
-
Ituxredi 100 mg Konzentrat zur Herstellung einer Infusionslösung
betapharm Arzneimittel GmbH
-
Ituxredi 500 mg Konzentrat zur Herstellung einer Infusionslösung
betapharm Arzneimittel GmbH
-
MabThera® 1 400 mg Lösung zur subkutanen Injektion
Roche Pharma AG
-
Mabthera 1.400 mg Abacus Lösung zur subkutanen Injektion
Abacus Medicine A/S
-
Mabthera 1.400 mg Canoma Lösung zur subkutanen Injektion
Canoma Pharma GmbH
-
Mabthera 1.400 mg CC Pharma Lösung zur subkutanen Injektion
CC Pharma GmbH
-
Mabthera 1.400 mg Eurim Lösung zur subkutanen Injektion
Eurim-Pharm Arzneimittel GmbH
-
MabThera 1.400 mg Fd Pharma Lösung zur subkutanen Injektion
FD Pharma GmbH
-
MabThera 1.400 mg Haemato-Pharm Lösung zur subkutanen Injektion
HAEMATO PHARM GmbH
-
Mabthera 1.400 mg kohlpharma Lösung zur subkutanen Injektion
kohlpharma GmbH
-
Mabthera 1.400 mg Orifarm Lösung zur subkutanen Injektion
Orifarm GmbH
-
Mabthera 1.400 mg Originalis Lösung zur subkutanen Injektion
Originalis B.V.
-
Mabthera 1.400 mg Paranova Lösung zur subkutanen Injektion
Paranova Pack A/S
-
MabThera 1.400 mg SynCo pharma Lösung zur subkutanen Injektion
SynCo pharma B.V.
-
Mabthera 100 mg Aaston Konzentrat zur Herstellung einer Infusionslösung
Aaston Healthcare GmbH
-
Mabthera 100 mg Abacus Konzentrat zur Herstellung einer Infusionslösung
Abacus Medicine A/S
-
Mabthera 100 mg Canoma Konzentrat zur Herstellung einer Infusionslösung
Canoma Pharma GmbH
-
Mabthera 100 mg Haemato-Pharm Konzentrat zur Herstellung einer Infusionslösung
HAEMATO PHARM GmbH
-
Mabthera 100 mg hvd Konzentrat zur Herstellung einer Infusionslösung
hvd medical GmbH
-
MabThera® 100 mg Konzentrat zur Herstellung einer Infusionslösung
Roche Pharma AG
-
Mabthera 100 mg Orifarm Konzentrat zur Herstellung einer Infusionslösung
Orifarm GmbH
-
Mabthera 500 mg 101 Carefarm Konzentrat zur Herstellung einer Infusionslösung
1 0 1 Carefarm GmbH
-
Mabthera 500 mg Aaston Konzentrat zur Herstellung einer Infusionslösung
Aaston Healthcare GmbH
-
Mabthera 500 mg Abacus Konzentrat zur Herstellung einer Infusionslösung
Abacus Medicine A/S
-
Mabthera 500 mg ACA Konzentrat zur Herstellung einer Infusionslösung
A.C.A. Müller ADAG Pharma AG
-
Mabthera 500 mg axicorp Konzentrat zur Herstellung einer Infusionslösung
axicorp Pharma B.V.
-
Mabthera 500 mg Canoma Konzentrat zur Herstellung einer Infusionslösung
Canoma Pharma GmbH
-
Mabthera 500 mg CC Pharma Konzentrat zur Herstellung einer Infusionslösung
CC Pharma GmbH
-
Mabthera 500 mg Emra Konzentrat zur Herstellung einer Infusionslösung
Emra-Med Arzneimittel GmbH
-
Mabthera 500 mg Eurim Konzentrat zur Herstellung einer Infusionslösung
Eurim-Pharm Arzneimittel GmbH
-
Mabthera 500 mg European Konzentrat zur Herstellung einer Infusionslösung
European Pharma B.V.
-
Mabthera 500 mg Haemato-Pharm Konzentrat zur Herstellung einer Infusionslösung
HAEMATO PHARM GmbH
-
Mabthera 500 mg hvd Konzentrat zur Herstellung einer Infusionslösung
hvd medical GmbH
-
Mabthera 500 mg Inopha Konzentrat zur Herstellung einer Infusionslösung
Inopha GmbH
-
Mabthera 500 mg kohlpharma Konzentrat zur Herstellung einer Infusionslösung
kohlpharma GmbH
-
MabThera® 500 mg Konzentrat zur Herstellung einer Infusionslösung
Roche Pharma AG
-
Mabthera 500 mg Medicopharm Konzentrat zur Herstellung einer Infusionslösung
Medicopharm AG
-
Mabthera 500 mg Nmg Pharma Konzentrat zur Herstellung einer Infusionslösung
NMG Pharma GmbH
-
Mabthera 500 mg Orifarm Konzentrat zur Herstellung einer Infusionslösung
Orifarm GmbH
-
Mabthera 500 mg Originalis Konzentrat zur Herstellung einer Infusionslösung
Originalis B.V.
-
Mabthera 500 mg SynCo pharma Konzentrat zur Herstellung einer Infusionslösung
SynCo pharma B.V.
-
Rixathon 100 mg Abacus Konzentrat zur Herstellung einer Infusionslösung
Abacus Medicine A/S
-
Rixathon 100 mg Haemato-Pharm Konzentrat zur Herstellung einer Infusionslösung
HAEMATO PHARM GmbH
-
Rixathon® 100 mg Konzentrat zur Herstellung einer Infusionslösung
Hexal AG
-
Rixathon 500 mg 101 Carefarm Konzentrat zur Herstellung einer Infusionslösung
1 0 1 Carefarm GmbH
-
Rixathon 500 mg Abacus Konzentrat zur Herstellung einer Infusionslösung
Abacus Medicine A/S
-
Rixathon 500 mg ACA Konzentrat zur Herstellung einer Infusionslösung
A.C.A. Müller ADAG Pharma AG
-
Rixathon 500 mg Allomedic Konzentrat zur Herstellung einer Infusionslösung
Allomedic GmbH
-
Rixathon 500 mg axicorp Konzentrat zur Herstellung einer Infusionslösung
axicorp Pharma GmbH
-
Rixathon 500 mg BB Farma Konzentrat zur Herstellung einer Infusionslösung
BB Farma S.R.L.