Tofacitinib
Tofacitinib (Xeljanz) ist ein Immunsuppressivum aus der Wirkstoffgruppe der selektiven Januskinasen-Inhibitoren (JAK-Hemmer) zur Behandlung von aktiver rheumatoider Arthritis, Psoriasis-Arthritis oder Colitus ulcerosa.
Tofacitinib: Übersicht
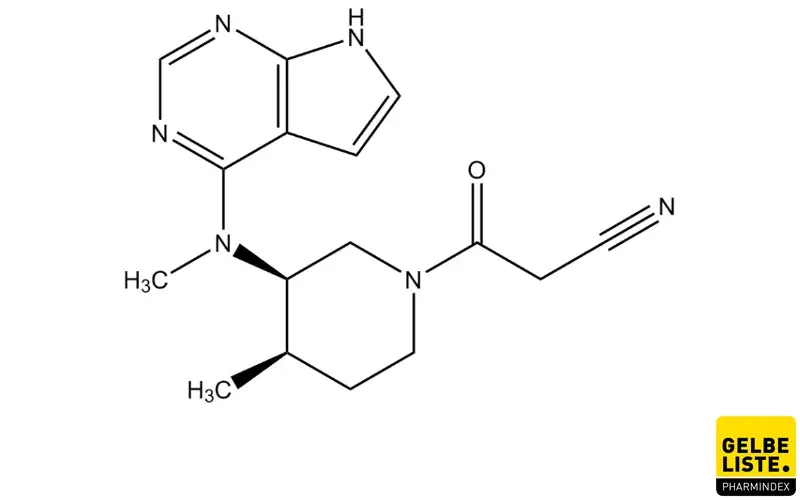
Anwendung
Tofacitinib (Xeljanz) ist in Kombination mit Methotrexat (MTX) indiziert zur Behandlung der mittelschweren bis schweren aktiven rheumatoiden Arthritis (RA) bei erwachsenen Patienten, die auf ein oder mehrere krankheitsmodifizierende Antirheumatika unzureichend angesprochen oder diese nicht vertragen haben. Tofacitinib kann als Monotherapie gegeben werden, wenn MTX nicht vertragen wird oder wenn eine Behandlung mit MTX ungeeignet ist.
Darüber hinaus ist Tofacitinib in Kombination mit MTX indiziert zur Behandlung der aktiven Psoriasis-Arthritis (PsA) bei erwachsenen Patienten, die auf eine vorangegangene krankheitsmodifizierende antirheumatische (DMARD-) Therapie unzureichend angesprochen oder diese nicht vertragen haben.
Außerdem kann Tofacitinib zur Behandlung erwachsener Patienten mit mittelschwerer bis schwerer aktiver Colitis ulcerosa (CU) angewendet werden, die auf eine konventionelle Therapie oder ein Biologikum unzureichend angesprochen haben, nicht mehr darauf ansprechen oder diese nicht vertragen haben.
COVID-19
Die Anwendung von Tofacitinib bei hospitalisierten Patienten mit COVID-19 Pneumonie scheint die Mortalität und die Fälle von Lungenversagen zu reduzieren. Demnach könnte die Inhibition von Januskinasen (JAK) ein potenzielles therapeutisches Target zur Prognoseverbesserung bei hospitalisierten COVID-19 Patienten darstellen (siehe auch Baricitinib).
Ergebnisse einer multizentrischen, randomisierten, doppelblinden, placebokontrollierten Studie zur Wirksamkeit und Sicherheit von Tofacitinib bei hospitalisierten COVID-19-Patienten, die im New England Journal of Medicine veröffentlicht wurde, zeigen, dass der Januskinase-Hemmer das Mortalitätsrisiko gegenüber Placebo senken konnte.
Anwendungsart
Tofacitinib ist als Filmtablette (5 oder 10 mg) oder als Retardtablette (11 mg) auf dem Markt erhältlich.
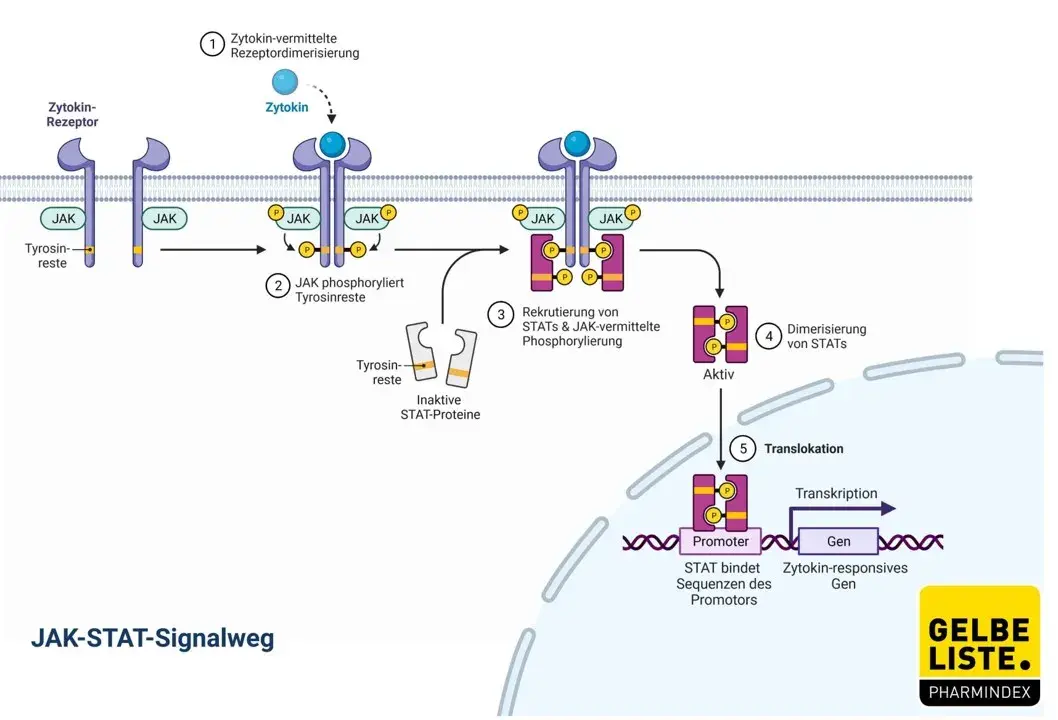
Wirkmechanismus
Tofacitinib ist ein potenter, selektiver Inhibitor der Januskinasen-(JAK-) Familie, der bevorzugt die Signalkaskade heterodimerer Zytokin-Rezeptoren inhibiert, die mit JAK1 und/oder JAK3 assoziieren. Die Hemmung von JAK1 und JAK3 durch Tofacitinib dämpft die Signalübertragung von Interleukinen (IL-2, IL-4, IL-6, IL-7, IL-9, IL-15 und IL-21) und von Typ-I- und Typ-II-Interferonen, wodurch die immunologische und inflammatorische Response moduliert wird.
Pharmakokinetik
Resorption
- Tofacitinib wird rasch resorbiert, wodurch maximale Plasmakonzentrationen (cmax) innerhalb von 0,5-1 Stunde erreicht werden.
- Die orale Bioverfügbarkeit beträgt 74%.
- Die gleichzeitige Einnahme mit fettreicher Nahrung hat keinen Einfluss auf die AUC, verringert jedoch die cmax um 32%.
- Die Einnahme erfolgt wie in den klinischen Studien nahrungsunabhängig.
- Tofacitinib zeigt einen dosisproportionalen Anstieg der systemischen Exposition.
- Steady-State-Konzentrationen werden nach 24-48 Stunden erreicht.
Verteilung
- Nach intravenöser Applikation (i.v.) beträgt das Verteilungsvolumen 87 l.
- Zirkulierendes Tofacitinib bindet zu etwa 40% an Plasmaproteine (überwiegend Albumin, offenbar nicht an α1-saures Glykoprotein).
- Tofacitinib verteilt sich gleichmäßig zwischen Erythrozyten und Plasma.
Metabolismus (Biotransformation)
- Tofacitinib wird hauptsächlich hepatisch über CYP3A4 metabolisiert, mit geringfügiger Beteiligung von CYP2C19.
Elimination
- Tofacitinib wird rasch eliminiert (Halbwertszeit ca. 3 Stunden).
- Tofacitinib wird zu etwa 70% über hepatische Metabolisierung und zu 30% unverändert renal eliminiert.
Pharmakokinetik bei Patienten mit rheumatoider Arthritis
- Reduktion der CYP-Aktivität aufgrund chronischer Entzündungsprozesse.
- Körpergewicht hat wenig Einfluss auf die systemische Exposition (AUC).
- Ältere Patienten haben eine minimal höhere AUC als Patienten im Durchschnittsalter von 55 Jahren.
- Frauen haben eine um etwa 7% geringere AUC als Männer.
- Konsistente Ergebnisse der populationsbezogenen Pharmakokinetik-Analyse bei Patienten mit aktiver PsA oder mittelschwerer bis schwerer CU.
Dosierung
Bei rheumatoider Arthritis und Psoriasis-Arthritis beträgt die empfohlene Dosis zweimal täglich 5 mg Tofacitinib und sollte nicht überschritten werden.
Die empfohlene Dosis bei der Einleitungstherapie von Colitis ulcerosa beträgt zweimal täglich 10 mg oral über einen Zeitraum von 8 Wochen. Wird bis Woche 8 kein ausreichender Therapieerfolg erzielt, kann die Einleitungsdosis von zweimal täglich 10 mg um weitere 8 Wochen verlängert werden (insgesamt 16 Wochen), gefolgt von zweimal täglich 5 mg als Erhaltungstherapie.
Bei Patienten, die bis Woche 16 keinen Therapieerfolg zeigen, sollte die Einleitungstherapie mit Tofacitinib beendet werden. Die empfohlene Dosis für die CU-Erhaltungstherapie beträgt zweimal täglich 5 mg Tofacitinib oral.
Die gleichzeitige Einnahme von MTX erfordert keine Dosisanpassung.
Umstellung von Filmtablette auf Retardtablette und umgekehrt
Patienten, die mit Tofacitinib 5 mg Filmtabletten zweimal täglich behandelt werden, können am Tag nach der letzten Dosis Tofacitinib 5 mg Filmtabletten auf Tofacitinib 11 mg Retardtabletten einmal täglich umgestellt werden. Patienten, die mit Tofacitinib 11 mg Retardtabletten einmal täglich behandelt werden, können am Tag nach der letzten Dosis Tofacitinib 11 mg Retard-tabletten auf Tofacitinib 5 mg Filmtabletten zweimal täglich umgestellt werden.
Nebenwirkungen
Die am häufigsten in klinischen Studien beobachteten Nebenwirkungen waren:
- Kopfschmerzen
- Infektionen der oberen Atemwege
- Nasopharyngitis
- Diarrhö
- Übelkeit
- Hypertonie
- Arthralgie (Gelenkschmerzen)
Aufgrund der Immunsuppression durch Tofacitinib kann es zu schwerwiegenden Infektionen kommen. Hierbei kam es während der Behandlung am häufigsten zu unter anderem:
- Pneumonie
- Zellulitis
- Herpes zoster
- Harnwegsinfektionen
- Divertikulitis
- Appendizitis
Thromboembolien
Eine Überprüfung der EMA ergab ein dosisabhängiges erhöhtes Risiko für die Entstehung schwerer venöser Thromboembolien, einschließlich Lungenembolien (einige Fälle verliefen tödlich), und tiefer Venenthrombosen bei Patienten, die Tofacitinib einnehmen. Die verfügbaren Daten zeigten auch, dass das Risiko für schwere Infektionen und tödliche Infektionen bei älteren Patienten über 65 Jahren im Vergleich zu jüngeren Patienten erhöht war. Daher sollte die Behandlung mit Tofacitinib bei diesen Patienten nur dann in Betracht gezogen werden, wenn keine geeignete Behandlungsalternative zur Verfügung steht.
Kardiovaskuläre Ereignisse
Am 25. März 2021 informierte der Hersteller von Xeljanz in einem Rote-Hand-Brief darüber, dass Ergebnisse einer klinischen Studie auf ein erhöhtes Risiko für schwerwiegende unerwünschte kardiovaskuläre Ereignisse und maligne Erkrankungen unter Tofacitinib im Vergleich zu TNF-alpha-Inhibitoren hindeuten.
Wechselwirkungen
Bei der Anwendung von Tofacitinib kann es bei gleichzeitiger Anwendung zu Wechselwirkungen mit folgenden Verbindungen kommen:
CYP3A4- und CYP2C19-Inhibitoren
Die tägliche Tofacitinib-Gesamtdosis sollte bei Patienten, die starke CYP3A4-Inhibitoren (z. B. Ketoconazol) erhalten, und bei Patienten, die gleichzeitig mindestens ein Arzneimittel erhalten, das zu einer mittelstarken Hemmung von CYP3A4 und zu einer starken Hemmung von CYP2C19 führt (z. B. Fluconazol), halbiert werden.
- Bei Patienten, die zweimal täglich 5 mg erhalten, sollte die Tofacitinib-Dosis auf einmal täglich 5 mg reduziert werden.
- Bei Patienten, die zweimal täglich 10 mg erhalten, sollte die Tofacitinib-Dosis auf zweimal täglich 5 mg reduziert werden.
Starke CYP3A4-Induktoren
Bei gleichzeitiger Anwendung mit starken CYP3A4-Induktoren (z. B. Rifampicin) verringert sich die Tofacitinib-Exposition, was zu zu einem Verlust oder zu einer Verringerung des klinischen Ansprechens führen kann.
Biologika
Die Anwendung von Tofacitinib in Kombination mit Biologika, wie TNF-Antagonisten, Interleukin(IL)-1R-Antagonisten, IL-6R-Antagonisten, monoklonalen Anti-CD20-Anti-körpern, IL-17-Antagonisten, IL-12/IL-23-Antagonisten, Integrin-Antikörpern, selektiven Co-Stimulations-Modulatoren und starken Immunsuppressiva wie Azathioprin, 6-Mercaptopurin, Ciclosporin und Tacrolimus wurde nicht untersucht und ist aufgrund der Möglichkeit einer verstärkten Immunsuppression und eines erhöhten Infektionsrisikos zu vermeiden.
Kontraindikation
Tofacitinib darf nicht angewendet werden:
- bei Überempfindlichkeit gegen den Wirkstoff oder sonstige Bestandteile des Arzneimittels
- bei aktiver Tuberkulose (TB)
- bei schweren Infektionen wie z. B. Sepsis oder opportunistischen Infektionen
- bei schwerer Leberfunktionsstörung
- in der Schwangerschaft und Stillzeit
Schwangerschaft
Die Anwendung von Tofacitinib ist während der Schwangerschaft kontraindiziert. Es gibt keine adäquaten und gut kontrollierten Studien zur Anwendung von Tofacitinib bei schwangeren Frauen. Der Wirkstoff erwies sich bei Ratten und Kaninchen als teratogen, und es beeinträchtigte die Geburt spwie die peri-/postnatale Entwicklung
Stillzeit
Die Anwendung von Tofacitinib ist während der Stillzeit kontraindiziert. Es ist nicht bekannt, ob Tofacitinib in die Muttermilch übergeht. Ein Risiko für das gestillte Kind kann nicht ausgeschlossen werden. Tofacitinib wurde in die Milch laktierender Ratten ausgeschieden.
Verkehrstüchtigkeit
Tofacitinib hat keinen oder einen zu vernachlässigenden Einfluss auf die Verkehrstüchtigkeit und die Fähigkeit zum Bedienen von Maschinen.
Hinweise
Venöse thromboembolische Ereignisse (VTE)
Schwerwiegende VTE-Ereignisse, einschließlich Lungenembolien, einige davon mit tödlichem Verlauf und tiefe Venenthrombosen wurden bei Patienten beobachtet, die Tofacitinib einnahmen. In einer klinischen Studie zu Tofacitinib wurde ein dosisabhängig erhöhtes VTE-Risiko im Vergleich zu TNF-Inhibitoren beobachtet.
VTE-Risikofaktoren umfassen:
- frühere VTE
- Patienten, die sich einem größeren chirurgischen Eingriff unterziehen
- Immobilisation
- Myokardinfarkt (in den vorhergehenden 3 Monaten)
- Herzinsuffizienz
- Anwendung von kombinierten hormonellen Kontrazeptiva oder einer Hormonersatztherapie
- Vorliegen einer erblichen Gerinnungsstörung
- Krebserkrankung
- höheres Lebensalter
- Übergewicht (BMI ≥ 30)
- Diabetes
- Hypertonie
- Rauchen
Schwere Infektionen
Unter der Therapie von Tofacitinib kann es zu schweren Infektionen aufgrund bakterieller, mykobakterieller, invasiv-fungaler, viraler oder anderer opportunistischer Krankheitserreger kommen. Das Risiko für opportunistische Infektionen ist in asiatischen Regionen höher. Patienten mit rheumatoider Arthritis, die Kortikosteroide einnehmen, können anfällig für Infektionen sein. Bei Patienten mit aktiven Infektionen, einschließlich lokalisierter Infektionen sollte eine Therapie mit Tofacitinib nicht eingeleitet werden.
Virusreaktivierung
In klinischen Studien mit Tofacitinib sind eine Virusreaktivierung und Fälle einer Reaktivierung von Herpesviren (z. B. Herpes Zoster) aufgetreten. Bei Patienten, die mit Tofacitinib behandelt wurden, scheint das Auftreten von Herpes Zoster erhöht zu sein bei:
- Patienten japanischer oder koreanischer Herkunft.
- Patienten mit einer ALC unter 1.000 Zellen/mm3
- Patienten mit langjähriger RA, die zuvor mit 2 oder mehr biologischen krankheitsmodifizierenden Antirheumatika (bDMARD) behandelt wurden.
- Patienten, die mit zweimal täglich 10 mg behandelt wurden.
Vor Beginn der Therapie mit Tofacitinib sollte eine Untersuchung auf eine Virushepatitis entsprechend den klinischen Leitlinien durchgeführt werden.
Malignität und lymphoproliferative Erkrankung
Risiken und Nutzen der Behandlung mit Tofacitinib sind vor der Einleitung der Therapie abzuwägen bei Patienten mit aktuellem oder zurückliegendem Malignom (ausgenommen ein erfolgreich behandelter, nicht-melanozytärer Hautkrebs (NMSC) oder wenn überlegt wird, die Behandlung mit Tofacitinib bei Patienten, die ein Malignom entwickeln, fortzusetzen. Es besteht die Möglichkeit, dass Tofacitinib die Körperabwehr gegen Malignome beeinträchtigt. Bei mit Tofacitinib behandelten Patienten traten Lymphome auf. Patienten mit rheumatoider Arthritis, insbesondere solche mit hochaktivem Krankheitsverlauf, haben für die Entwicklung von Lymphomen möglicherweise ein höheres Risiko (bis zu einem Mehrfachen) als die Allgemeinbevölkerung. Die Wirkung von Tofacitinib auf die Bildung von Lymphomen ist unklar. Andere Malignome wurden in klinischen Studien und bei der Anwendung nach der Zulassung beobachtet, darunter, aber nicht ausschließlich, Lungenkrebs, Brustkrebs, Melanome, Prostatakrebs und Bauchspeicheldrüsenkrebs. Die Wirkung von Tofacitinib auf die Entwicklung und den Verlauf von Malignomen ist nicht bekannt.
Weitere Hinweise können der Fachinformation entnommen werden.
Alternativen
Als alternative Therapieoptionen für Tofacitinib kommen folgende Wirkstoffe in Frage:
- DMARDs
- Glukokortikoide
- andere JAK-Inhibitoren wie z.B. Baricitinib, Upadacitinib
- 5-Aminosalicylate (5-ASA) wie z.B. Mesalazin (bei Colitis ulcerosa)
-
XELJANZ® 1 mg/ml Lösung zum Einnehmen
Pfizer Pharma GmbH
-
Xeljanz 5 mg Abacus Filmtabletten
Abacus Medicine A/S
-
Xeljanz 5 mg axicorp B.V. Filmtabletten
axicorp Pharma B.V.
-
Xeljanz 5 mg CC Pharma Filmtabletten
CC Pharma GmbH
-
Xeljanz 5 mg Eurim Filmtabletten
Eurim-Pharm Arzneimittel GmbH
-
Xeljanz 5 mg European Filmtabletten
European Pharma B.V.
-
XELJANZ® 5 mg Filmtabletten
Pfizer Pharma GmbH
-
Xeljanz 5 mg Haemato-Pharm Filmtabletten
HAEMATO PHARM GmbH
-
Xeljanz 5 mg kohlpharma Filmtabletten
kohlpharma GmbH
-
Xeljanz 5 mg Orifarm Filmtabletten
Orifarm GmbH
-
Xeljanz 5 mg Originalis Filmtabletten
Originalis B.V.
-
Xeljanz 5 mg Paranova Filmtabletten
Paranova Pack A/S
-
Xeljanz 5 mg SynCo pharma Filmtabletten
SynCo pharma B.V.
-
Xeljanz 10 mg Abacus Filmtabletten
Abacus Medicine A/S
-
Xeljanz 10 mg axicorp B.V. Filmtabletten
axicorp Pharma B.V.
-
Xeljanz 10 mg axicorp Filmtabletten
axicorp Pharma B.V.
-
Xeljanz 10 mg CC-Pharma Filmtabletten
CC Pharma GmbH
-
Xeljanz 10 mg Eurim Filmtabletten
Eurim-Pharm Arzneimittel GmbH
-
XELJANZ® 10 mg Filmtabletten
Pfizer Pharma GmbH
-
Xeljanz 10 mg kohlpharma Filmtabletten
kohlpharma GmbH
-
Xeljanz 10 mg Paranova Filmtabletten
Paranova Pack A/S
-
Xeljanz 11 mg Abacus Retardtabletten
Abacus Medicine A/S
-
Xeljanz 11 mg axicorp B.V. Retardtabletten
axicorp Pharma B.V.
-
Xeljanz 11 mg CC Pharma Retardtabletten
CC Pharma GmbH
-
Xeljanz 11 mg kohlpharma Retardtabletten
kohlpharma GmbH
-
Xeljanz 11 mg Orifarm Retardtabletten
Orifarm GmbH
-
XELJANZ® 11 mg Retardtabletten
Pfizer Pharma GmbH














