Bevacizumab
Bevacizumab ist ein monoklonaler Antikörper gegen den Gefäßwachstumsfaktor VEGF . Der Angiogenese-Hemmer wird zur Behandlung verschiedener fortgeschrittener Krebserkrankungen sowie zur Behandlung der neovaskulären altersbedingten Makuladegeneration angewendet.
Bevacizumab: Übersicht
Anwendung
Bevacizumab ist ein humanisierter monoklonaler Antikörper, der an den Gefäßwachstumsfaktor VEGF (Vascular Endothelial Growth Factor) bindet und diesen hemmt. Das Arzneimittel ist somit ein Angiogenese-Hemmer, der die Neubildung von Blutgefäßen inhibiert, die Tumore für ihr Wachstum benötigen. Bevacizumab ist in Kombination mit anderen Arzneimitteln für die Behandlung verschiedener Tumorerkrankungen zugelassen, wie z. B.:
- metastasiertes Kolon- oder Rektumkarzinom
- metastasiertes Mammakarzinom
- inoperables fortgeschrittenes, metastasiertes oder rezidivierendes nicht-kleinzellige Bronchialkarzinom
- fortgeschrittenem und/oder metastasiertem Nierenzellkarzinom
- fortgeschrittenem epithelialem Ovarialkarzinom, Eileiterkarzinom oder primärem Peritonealkarzinom
- rezidivierendem oder metastasiertem Zervixkarzinom
Bevacizumab ist zudem zur Behandlung der neovaskulären altersbedingten Makuladegeneration (nAMD) zugelassen.
Anwendungsart
Tumortherapie
Bevacizumab sollte über einen Zeitraum von 90 Minuten über eine i.v.-Infusion appliziert werden. Wenn die erste Infusion gut vertragen wird, kann die zweite Infusion über 60 Minuten erfolgen. Wenn auch diese gut vertragen wurde, können alle folgenden Infusionen über 30 Minuten erfolgen.
Therapie der neovaskulären altersbedingten Makuladegeneration
Bevacizumab wird als intravitreale Injektion in den Glaskörper des Auges verabreicht. Die Zubereitung und Injektion erfolgen unter aseptischen Bedingungen unmittelbar nacheinander. Die Injektion erfolgt nach Desinfektion und lokaler Betäubung 3,5 bis 4,0 mm hinter dem Limbus, wobei der horizontale Meridian vermieden wird. Wiederholte Injektionen sind stets an unterschiedlichen Stellen der Sklera durchzuführen.
Wirkmechanismus
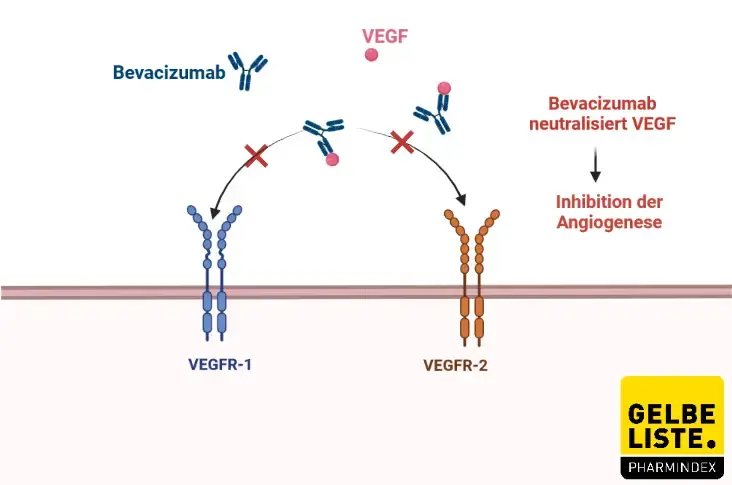
Der monoklonale Antikörper Bevacizumab richtet sich gezielt gegen den Wachstumsfaktor VEGF, der von Tumoren exprimiert wird und für die Bildung neuer Blutgefäße (Angiogenese) sorgt. Durch die Neutralisierung der biologischen Aktivität von VEGF reduziert Bevacizumab die Vaskularisierung von Tumoren, normalisiert das vorhandene Tumorgefäßsystem und hemmt die Bildung neuer Tumorgefäßsysteme, wodurch das Tumorwachstum gehemmt wird. In gleicher Weise wird das krankhafte Gefäßwachstum im Bereich der Makula bei der nAMD gehemmt und die Flüssigkeitsansammlung im retinalen Gewebe reduziert.
Pharmakokinetik
Resorption
- Nach intravenöser Verabreichung von 2 mg/kg an gesunde Probanden wurde eine maximale Serumkonzentration (Cmax) von 40 μg/ml nach ca. 2 Stunden erreicht.
- Nach intravitrealer Gabe gelangt nur ein geringer Anteil systemisch in den Kreislauf.
Verteilung
- Nach intravenöser Verabreichung betrug das Volumen des zentralen Kompartiments (Vc) üblicherweise bei weiblichen Patienten 2,73 Liter und bei männlichen Patienten 3,28 Liter. Diese Werte befinden sich in dem Bereich, der für Immunglobuline G (IgG) und andere monoklonale Antikörper beschrieben wurde. Das Volumen des peripheren Kompartiments (Vp) betrug bei Anwendung von Bevacizumab in Kombination mit zytostatischen Wirkstoffen üblicherweise bei weiblichen Patienten 1,69 Liter und bei männlichen Patienten 2,35 Liter. Nach der Korrektur entsprechend dem Körpergewicht hatten männliche Patienten einen höheren Vc-Wert (+20%) als Frauen.
- Die Verteilung nach intravitrealer Anwendung beschränkt sich überwiegend auf das Auge. Geringe Mengen können über das Blut zirkulieren; die systemische Verteilung nach intravitrealer Gabe ist jedoch deutlich geringer als bei intravenöser Anwendung.
Metabolismus
- Bevacizumab wird als monoklonaler Antikörper ähnlich wie endogenes IgG überwiegend durch proteolytischen Abbau in kleinere Peptide und Aminosäuren über zelluläre Mechanismen verstoffwechselt.
Elimination
- Die Clearance nach intravenöser Verabreichung beträgt bei weiblichen Patienten durchschnittlich 0,188 Liter/Tag und bei männlichen Patienten durchschnittlich 0,220 Liter/Tag. Nach Korrektur entsprechend dem Körpergewicht hatten die männlichen Patienten eine höhere Bevacizumab-Clearance (+17%) als Frauen. Nach dem Zwei-Kompartiment-Modell beträgt die Eliminationshalbwertszeit für weibliche Patienten üblicherweise 18 Tage und für männliche Patienten 20 Tage.
- Aufgrund der geringen systemischen Resorption ist die systemische Elimination nach intravitrealer Injektion vernachlässigbar.
Dosierung
Tumortherapie
Die Dosierung in der Tumortherapie unterscheidet sich je nach Anwendungsgebiet und Tumorart. Die genauen Dosierungsempfehlungen können der jeweiligen Fachinformation entnommen werden.
Neovaskuläre altersbedingte Makuladegeneration
- Standarddosis: Die empfohlene Dosis beträgt 1,25 mg Bevacizumab.
- Initiale Behandlung: Zu Beginn wird monatlich injiziert – in der Regel sind mindestens drei aufeinanderfolgende Injektionen erforderlich, um eine maximale Wirksamkeit zu erreichen.
- Erhaltungsphase: Nach Erreichen der maximalen Sehschärfe oder dem Ausbleiben weiterer Krankheitsaktivität können die Behandlungsintervalle individuell angepasst werden. Die Entscheidung basiert auf der Beurteilung der Sehschärfe sowie bildgebender und funktioneller Befunde (z. B. OCT oder Fluoreszenzangiographie).
- Therapiepause: Wenn sich keine weiteren klinischen oder anatomischen Verbesserungen zeigen, sollte die Behandlung beendet werden. Auch bei medizinischer Notwendigkeit ist eine Unterbrechung möglich.
Nebenwirkungen
Zu den sehr häufigen Nebenwirkungen, die während einer intravenösen Therapie mit Bevacizumab auftreten können, zählen:
- periphere sensorische Neuropathie
- Hypertonie
- Diarrhö
- Übelkeit
- Erbrechen
- Abdominalschmerz
- Asthenie
- Ermüdung (Fatigue)
Zu den häufigen Nebenwirkungen, die während einer intravitrealen Therapie mit Bevacizumab auftreten können, zählen:
- Mouches volantes
- Augenschmerzen
- Bindehautblutung
- erhöhter intraokularer Druck
Die vollständigen Angaben können der jeweiligen Fachinformation entnommen werden.
Wechselwirkungen
Folgende Wechselwirkungen sind bei der Anwendung von Bevacizumab zu beachten:
Kombinationsbehandlung mit Bevacizumab und Sunitinibmalat
In zwei klinischen Studien zum metastasierten Nierenzellkarzinom wurde bei 7 von 19 Patienten, die gleichzeitig mit Bevacizumab (10 mg/kg alle zwei Wochen) und Sunitinibmalat (50 mg täglich) behandelt wurden, über das Auftreten einer mikroangiopathischen hämolytischen Anämie berichtet.
Darüber hinaus wurden bei einigen dieser Patienten eine Hypertonie (einschließlich einer hypertensiven Krise), erhöhte Kreatininwerte und neurologische Symptome beobachtet. Alle diese Befunde waren nach Absetzen von Bevacizumab und Sunitinibmalat reversibel.
Kombinationsbehandlung mit platin- oder taxanhaltigen Therapien
Unter der Kombinationsbehandlung mit platin- oder taxanhaltigen Therapien wurden erhöhte Raten schwerer Neutropenien, febriler Neutropenien oder Infektionen mit oder ohne schwerer Neutropenie (einschließlich einiger Todesfälle) bei NSCLC- oder metastasierten Mammakarzinom- Patienten beobachtet.
Monoklonale EGFR-Antikörper in Kombination mit Bevacizumab und Chemotherapie
Monoklonale EGFR-Antikörper dürfen zur Behandlung des metastasierten Kolorektalkarzinoms nicht zusammen mit Bevacizumab-haltigen Chemotherapie-Schemata angewendet werden. Ergebnisse der randomisierten Phase-III-Studien PACCE und CAIRO-2 bei Patienten mit metastasiertem Kolorektalkarzinom lassen im Vergleich zur alleinigen Anwendung von Bevacizumab plus Chemotherapie auf eine Abnahme des progressionsfreien Überlebens und/oder des Gesamtüberlebens sowie auf eine Zunahme der Nebenwirkungen schließen, wenn die monoklonalen EGFR-Antikörper Panitumumab oder Cetuximab in Kombination mit Bevacizumab plus Chemotherapie gegeben werden.
Intravitreale Behandlung mit Bevacizumab
Aufgrund des Eliminationsmechanismus des Wirkstoffs sind klinisch relevante Wechselwirkungen nicht zu erwarten. Dennoch wird empfohlen, Bevacizumab nicht gleichzeitig mit anderen systemischen oder intravitreal verabreichten Anti-VEGF-Arzneimitteln anzuwenden, um additive Wirkungen oder unerwünschte Effekte zu vermeiden.
Kontraindikationen
Die intravenöse Anwendung von Bevacizumab ist generell kontraindiziert bei:
- Überempfindlichkeit gegen den Wirkstoff oder einen der genannten sonstigen Bestandteile des jeweiligen Arzneimittels
- Überempfindlichkeit gegen CHO-Zellprodukte oder andere rekombinante humane oder humanisierte Antikörper
- Schwangerschaft
Die intravitreale Anwendung von Bevacizumab ist kontraindiziert bei:
- Überempfindlichkeit gegen den Wirkstoff
- Patienten mit aktiven oder vermuteten okulären oder periokularen Infektionen
- Aktive intraokuläre Entzündung
Schwangerschaft
Bevacizumab ist während der Schwangerschaft kontraindiziert. Es liegen keine klinischen Studiendaten über die Anwendung bei Schwangeren vor. In tierexperimentellen Studien wurde eine Reproduktionstoxizität einschließlich Missbildungen beobachtet. Da IgGs bekanntermaßen die Plazentaschranke überwinden können; ist zu erwarten, dass Bevacizumab die Angiogenese beim Fetus hemmt, weshalb der Antikörper in Verdacht steht, bei einer Anwendung während der Schwangerschaft schwerwiegende Geburtsfehler zu verursachen.
Stillzeit
Es ist nicht bekannt, ob Bevacizumab in die Muttermilch übergeht. Da allerdings humanes IgG in die Muttermilch ausgeschieden wird und Bevacizumab Wachstum und Entwicklung des Säuglings beeinträchtigen könnte, müssen Frauen während der Therapie das Stillen absetzen und dürfen auch bis mindestens 6 Monate nach der letzten Bevacizumab-Anwendung nicht stillen.
Verkehrstüchtigkeit
Bevacizumab hat keinen oder nur einen zu vernachlässigenden Einfluss auf die Verkehrstüchtigkeit und die Fähigkeit zum Bedienen von Maschinen. Nach intravenöser Anwendung wurden jedoch Fälle von Schläfrigkeit und Synkopen berichtet, die das Reaktionsvermögen beeinträchtigen können. Nach intravitrealer Injektion kann es zudem zu vorübergehenden Sehstörungen kommen, etwa durch die Injektion selbst oder durch nachfolgende augenärztliche Untersuchungen. Patienten sollten daher keine Fahrzeuge führen oder Maschinen bedienen, solange Symptome wie verschwommenes Sehen, Schwindel oder verminderte Konzentrationsfähigkeit bestehen. Die Teilnahme am Straßenverkehr oder das Bedienen von Maschinen ist erst wieder möglich, wenn die volle Seh- und Reaktionsfähigkeit wiederhergestellt ist.
Anwendungshinweise
Bei der intravenösen Anwendung von Bevacizumab sind folgende Warnhinweise zu beachten:
- Gastrointestinale Perforationen und Fisteln: Bevacizumab kann das Risiko für GI- und Gallenblasenperforationen erhöhen, besonders nach Strahlentherapie. Bei Perforation ist die Therapie abzusetzen.
- GI-vaginale Fisteln: Bei zuvor bestrahlten Patientinnen mit Zervixkarzinom kann es zu GI-vaginalen Fisteln kommen. Ein Rezidiv erhöht das Risiko zusätzlich.
- Nicht-GI-Fisteln: Fisteln außerhalb des GI-Trakts, z. B. ösophagotracheale, können auftreten. Bei schweren Fällen muss die Behandlung beendet werden.
- Wundheilungsstörungen: Die Wundheilung kann beeinträchtigt sein. Die Behandlung darf erst nach vollständiger Heilung begonnen oder fortgesetzt werden.
- Nekrotisierende Fasziitis: Selten gemeldet; tritt meist im Zusammenhang mit anderen Komplikationen auf. Bevacizumab ist in solchen Fällen abzusetzen.
- Hypertonie: Häufig unter Therapie. Regelmäßige Blutdruckkontrollen erforderlich. Bei unkontrollierter Hypertonie oder Krise ist das Medikament abzusetzen.
- Posteriores reversibles Enzephalopathie Syndrom (PRES): Seltene neurologische Komplikation mit Krampfanfällen oder Sehstörungen. Therapie bei bestätigtem PRES beenden.
- Proteinurie: Tritt dosisabhängig auf. Regelmäßige Urinkontrolle empfohlen. Bei nephrotischem Syndrom ist Bevacizumab dauerhaft abzusetzen.
- Arterielle Thromboembolie: Erhöhtes Risiko für Schlaganfälle und Herzinfarkte, besonders bei älteren Patienten oder entsprechender Vorgeschichte. Bei Auftreten: Behandlung dauerhaft beenden.
- Venöse Thromboembolie: Lungenembolien und andere venöse Ereignisse möglich. Grad-4-Ereignisse erfordern Therapieabbruch, Grad-1–3-Fälle engmaschig überwachen.
- Blutungen: Risiko schwerer Blutungen, v. a. tumorassoziiert. Ab Grad 3 ist die Behandlung abzusetzen. Bei ZNS-Metastasen besondere Vorsicht, bei intrakraniellen Blutungen Abbruch erforderlich.
- Lungenblutung/Hämoptoe: Tödlich verlaufende Lungenblutungen möglich, insbesondere bei NSCLC. Patienten mit frischer Hämoptoe >2,5 ml dürfen nicht behandelt werden.
- Aneurysmen & Dissektionen: VEGF-Hemmer können Aneurysmen oder Gefäßdissektionen fördern. Vorsicht bei Patienten mit Hypertonie oder entsprechender Vorgeschichte.
- Herzinsuffizienz: Kann asymptomatisch oder symptomatisch auftreten, v. a. nach Anthracyclin- oder Strahlentherapie. Regelmäßige kardiologische Überwachung empfohlen.
- Neutropenie & Infektionen: Erhöhtes Risiko für febrile Neutropenie und Infektionen bei Kombination mit myelotoxischer Chemotherapie. Selten tödlich.
- Überempfindlichkeit: Anaphylaktische Reaktionen möglich. Bei Symptomen Infusion sofort abbrechen, medizinische Maßnahmen einleiten.
- Kieferosteonekrose: V. a. bei gleichzeitiger i. v. Bisphosphonatgabe und nach zahnärztlichen Eingriffen. Vorab Zahnsanierung erwägen.
- Intravitreale Anwendung: Nicht für intraokulare Injektion zugelassen. Risiko schwerer Augenkomplikationen und bleibender Sehschäden.
- Systemische Effekte bei intravitrealer Gabe: Nach lokaler Anwendung können systemische Nebenwirkungen wie Blutungen oder Thrombosen auftreten.
- Ovarialinsuffizienz: Bevacizumab kann Fertilität beeinträchtigen. Beratung zu Fertilitätserhalt vor Therapiebeginn empfohlen.
Bei der intravitrealen Anwendung von Bevacizumab sind folgende Warnhinweise zu beachten:
- Injektionsbedingte Reaktionen: Bevacizumab kann nach intravitrealer Anwendung zu Endophthalmitis, Entzündungen oder Netzhautkomplikationen führen. Eine sterile Injektionstechnik und engmaschige Nachsorge sind essenziell.
- Augeninnendruckanstieg: Nach der Injektion kann der Augeninnendruck vorübergehend steigen. Eine Kontrolle vor und nach der Anwendung ist notwendig, insbesondere bei Glaukompatienten.
- Beidseitige Anwendung: Die gleichzeitige Injektion in beide Augen wurde nicht untersucht und sollte wegen möglicher erhöhter Risiken nur mit Vorsicht erfolgen.
- Immunogenität: Da es sich um ein Proteinpräparat handelt, kann Bevacizumab immunogene Reaktionen verursachen. Patienten sollten ungewöhnliche Augenbeschwerden rasch melden.
- Kombination mit anderen Anti-VEGF-Präparaten: Eine gleichzeitige Gabe mit anderen Anti-VEGF-Arzneimitteln sollte unterbleiben, da keine Sicherheitsdaten vorliegen.
- Gründe für Therapiepause: Die Behandlung soll unterbrochen werden bei Visusverlust ≥30 Buchstaben, Netzhautabriss, zentraler subretinaler Blutung, erhöhtem Augeninnendruck, thromboembolischen Ereignissen oder kürzlicher Augen-OP.
- Pigmentepitheleinrisse: Bei großflächiger Ablösung des retinalen Pigmentepithels besteht ein erhöhtes Risiko für Einrisse – Vorsicht bei der Therapieeinleitung.
- Netzhautablösung und Makulaforamina: Die Behandlung ist abzubrechen, wenn Netzhautablösung oder Makulaforamina im fortgeschrittenen Stadium auftreten.
- Systemische Risiken: Systemische Blutungen oder thromboembolische Ereignisse wurden nach intravitrealer Anwendung berichtet. Vorsicht bei Patienten mit kardio- oder zerebrovaskulärer Vorerkrankung.
Alternativen
Weitere antineovaskuläre Arzneimittel sind:
Andere Anti-VEGF-Therapien zur Behandlung der nAMD umfassen:
Wirkstoff-Informationen
-
Abevmy 25 mg/ml Konzentrat zur Herstellung einer Infusionslösung, 4 ml
Biocon Biologics Germany GmbH
-
Abevmy 25 mg/ml Konzentrat zur Herstellung einer Infusionslösung, 16 ml
Biocon Biologics Germany GmbH
-
Alymsys 25 mg/ml CC Pharma Konzentrat zur Herstellung einer Infusionslösung, 16 ml
CC Pharma GmbH
-
Alymsys® 25 mg/ml Konzentrat zur Herstellung einer Infusionslösung, 4 ml
Zentiva Pharma GmbH
-
Alymsys® 25 mg/ml Konzentrat zur Herstellung einer Infusionslösung, 16 ml
Zentiva Pharma GmbH
-
Avastin 25 mg/ml Abacus Konzentrat zur Herstellung einer Infusionslösung, 4 ml
Abacus Medicine A/S
-
Avastin 25 mg/ml Abacus Konzentrat zur Herstellung einer Infusionslösung, 16ml
Abacus Medicine A/S
-
Avastin 25 mg/ml Canoma Konzentrat zur Herstellung einer Infusionslösung, 16 ml
Canoma Pharma GmbH
-
Avastin 25 mg/ml CC Pharma Konzentrat zur Herstellung einer Infusionslösung, 4 ml
CC Pharma GmbH
-
Avastin 25 mg/ml CC Pharma Konzentrat zur Herstellung einer Infusionslösung, 16 ml
CC Pharma GmbH
-
Avastin 25 mg/ml Emra Konzentrat zur Herstellung einer Infusionslösung, 16 ml
Emra-Med Arzneimittel GmbH
-
Avastin 25 mg/ml Eurim Konzentrat zur Herstellung einer Infusionslösung, 4 ml
Eurim-Pharm Arzneimittel GmbH
-
Avastin 25 mg/ml Eurim Konzentrat zur Herstellung einer Infusionslösung, 16 ml
Eurim-Pharm Arzneimittel GmbH
-
Avastin 25 mg/ml Haemato Konzentrat zur Herstellung einer Infusionslösung, 4 ml
HAEMATO PHARM GmbH
-
Avastin 25 mg/ml Haemato Konzentrat zur Herstellung einer Infusionslösung, 16 ml
HAEMATO PHARM GmbH
-
Avastin 25 mg/ml hvd Konzentrat zur Herstellung einer Infusionslösung, 4 ml
hvd medical GmbH
-
Avastin 25 mg/ml hvd Konzentrat zur Herstellung einer Infusionslösung, 16 ml
hvd medical GmbH
-
Avastin 25 mg/ml kohlpharma Konzentrat zur Herstellung einer Infusionslösung, 4 ml
kohlpharma GmbH
-
Avastin 25 mg/ml kohlpharma Konzentrat zur Herstellung einer Infusionslösung, 16 ml
kohlpharma GmbH
-
Avastin® 25 mg/ml Konzentrat zur Herstellung einer Infusionslösung, 4 ml
Roche Pharma AG
-
Avastin® 25 mg/ml Konzentrat zur Herstellung einer Infusionslösung, 16 ml
Roche Pharma AG
-
Avastin 25 mg/ml NMG Pharma Konzentrat zur Herstellung einer Infusionslösung, 4 ml
NMG Pharma GmbH
-
Avastin 25 mg/ml NMG Pharma Konzentrat zur Herstellung einer Infusionslösung, 16 ml
NMG Pharma GmbH
-
Avastin 25 mg/ml Orifarm Konzentrat zur Herstellung einer Infusionslösung, 4 ml
Orifarm GmbH
-
Avastin 25 mg/ml Orifarm Konzentrat zur Herstellung einer Infusionslösung, 16 ml
Orifarm GmbH
-
Avastin 25 mg/ml SynCo pharma Konzentrat zur Herstellung einer Infusionslösung, 4 ml
SynCo pharma B.V.
-
Avastin 25 mg/ml SynCo pharma Konzentrat zur Herstellung einer Infusionslösung, 16 ml
SynCo pharma B.V.
-
Aybintio® 25 mg/ml Konzentrat zur Herstellung einer Infusionslösung, 4 ml
Organon Healthcare GmbH
-
Aybintio® 25 mg/ml Konzentrat zur Herstellung einer Infusionslösung, 16 ml
Organon Healthcare GmbH
-
MVASI 25 mg/ml Eurim Konzentrat zur Herstellung einer Infusionslösung, 4 ml
Eurim-Pharm Arzneimittel GmbH
-
MVASI 25 mg/ml Eurim Konzentrat zur Herstellung einer Infusionslösung, 16 ml
Eurim-Pharm Arzneimittel GmbH
-
MVASI® 25 mg/ml Konzentrat zur Herstellung einer Infusionslösung, 4 ml
Amgen GmbH
-
MVASI® 25 mg/ml Konzentrat zur Herstellung einer Infusionslösung, 16 ml
Amgen GmbH
-
Oyavas® 25 mg/ml Konzentrat zur Herstellung einer Infusionslösung, 4 ml
STADAPHARM GmbH
-
Oyavas® 25 mg/ml Konzentrat zur Herstellung einer Infusionslösung, 16 ml
STADAPHARM GmbH
-
Oyavas® 25 mg/ml Konzentrat zur Herstellung einer Infusionslösung, 16 ml HU
STADAPHARM GmbH
-
Oyavas® 25 mg/ml Konzentrat zur Herstellung einer Infusionslösung, 16 ml IE
STADAPHARM GmbH
-
Vegzelma 25 mg/ml 1 4U Pharma Konzentrat zur Herstellung zur einer Infusionslösung, 16 ml
1 4 U Pharma GmbH
-
Vegzelma 25 mg/ml Abacus Konzentrat zur Herstellung einer Infusionslösung, 16 ml
Abacus Medicine A/S
-
Vegzelma 25 mg/ml ACA Konzentrat zur Herstellung zur einer Infusionslösung, 16 ml
A.C.A. Müller ADAG Pharma AG
-
Vegzelma 25 mg/ml axicorp Konzentrat zur Herstellung zur einer Infusionslösung, 16 ml
axicorp Pharma B.V.
-
Vegzelma 25 mg/ml Eurim Konzentrat zur Herstellung einer Infusionslösung, 16 ml
Eurim-Pharm Arzneimittel GmbH
-
Vegzelma 25 mg/ml kohlpharma Konzentrat zur Herstellung einer Infusionslösung, 16 ml
kohlpharma GmbH
-
VEGZELMA 25 mg/ml Konzentrat zur Herstellung einer Infusionslösung, 4 ml
Celltrion Healthcare Deutschland GmbH
-
VEGZELMA 25 mg/ml Konzentrat zur Herstellung einer Infusionslösung, 16 ml
Celltrion Healthcare Deutschland GmbH
-
Vegzelma 25 mg/ml SynCo pharma Konzentrat zur Herstellung einer Infusionslösung, 4 ml
SynCo pharma B.V.
-
Vegzelma 25 mg/ml SynCo pharma Konzentrat zur Herstellung einer Infusionslösung, 16 ml
SynCo pharma B.V.
-
Zirabev 25 mg/ml Abacus Konzentrat zur Herstellung einer Infusionslösung, 16 ml
Abacus Medicine A/S
-
Zirabev 25 mg/ml axicorp Konzentrat zur Herstellung einer Infusionslösung, 16 ml
axicorp Pharma B.V.
-
Zirabev® 25 mg/ml Konzentrat zur Herstellung einer Infusionslösung, 4 ml
Pfizer Pharma GmbH














