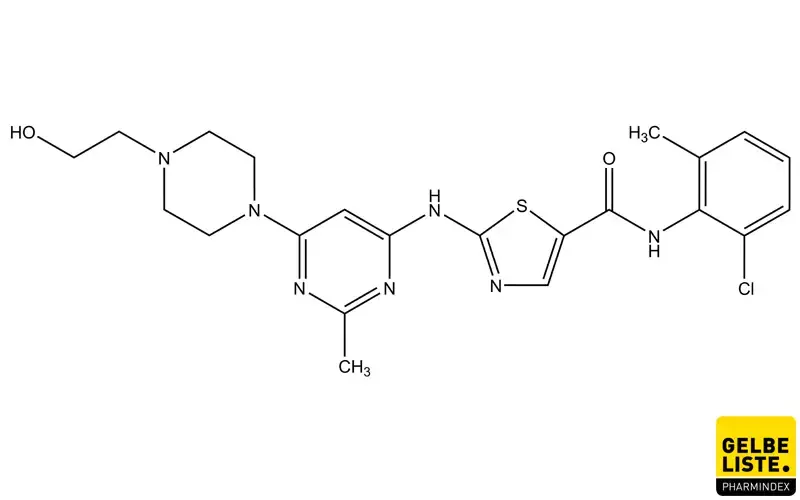
Dasatinib
Dasatinib ist ein oraler dualer BCR/ABL- und Src-Familien-Tyrosinkinase-Inhibitor, der für die Anwendung bei Patienten mit chronischer myeloischer Leukämie (CML) zugelassen ist.
Dasatinib: Übersicht
Anwendung
Dasatinib ist bei erwachsenen Patienten angezeigt für die Behandlung von:
- neu diagnostizierter Philadelphia-Chromosom-positiver (Ph+) chronischer myeloischer Leukämie (CML) in der chronischen Phase.
- CML in der chronischen oder akzelerierten Phase oder in der Blastenkrise mit Resistenz oder Intoleranz gegenüber einer vorherigen Behandlung einschließlich Imatinib.
- Ph+ akuter lymphatischer Leukämie (ALL) oder lymphatischer Blastenkrise der CML mit Resistenz oder Intoleranz gegenüber einer vorherigen Therapie.
Für die Behandlung von Kindern und Jugendlichen ist Dasatinib indiziert bei:
- neu diagnostizierter Philadelphia-Chromosom-positiver (Ph+) chronischer myeloischer Leukämie (CML) in der chronischen Phase (Ph+ CML-CP) oder Ph+ CML-CP mit Resistenz oder Intoleranz gegenüber einer vorherigen Therapie einschließlich Imatinib.
- neu diagnostizierter Ph+ ALL in Kombination mit Chemotherapie.
Wirkmechanismus
Dasatinib ist ein oraler Tyrosinkinase-Inhibitor der zweiten Generation und hemmt bereits in nanomolaren Konzentrationen die Kinasen BCR-ABL, SRC, LCK, YES, FYN, c-KIT, EPHA2 und PDGFRβ. Basierend auf Modellierungsstudien bindet Dasatinib an mehrere Konformationen der ABL-Kinase. In vitro hemmt der Wirkstoff das Wachstum von Zelllinien mit chronischer myeloischer Leukämie (CML) und akuter lymphoblastischer Leukämie (ALL), die BCR-ABL überexprimieren. Unter den Bedingungen der Assays war Dasatinib außerdem in der Lage, die Imatinib-Resistenz zu überwinden, die aus Mutationen der BCR-ABL-Kinase-Domäne, der Aktivierung alternativer Signalwege unter Beteiligung der Kinasen der SRC-Familie (LYN, HCK) und der Überexpression von Multidrug-Resistance-Genen resultierte.
Pharmakokinetik
Resorption
- Dasatinib wird nach der Einnahme rasch resorbiert.
- Maximale Konzentrationen werden nach 0,5 bis 3 Stunden erreicht.
- Nach oraler Gabe von Dosierungen zwischen 25 mg und 120 mg zweimal täglich ist der Anstieg der mittleren Exposition (AUCτ) in etwa proportional zur Dosiszunahme.
- Die mittlere terminale Halbwertszeit von Dasatinib beträgt ca. 5 bis 6 Stunden.
Verteilung
- Dasatinib besitzt ein großes scheinbares Verteilungsvolumen (2.505 l), was darauf hindeutet.
- Bei klinisch relevanten Dasatinib-Konzentrationen betrug die Bindung an Plasmaproteine etwa 96%.
Biotransformation
- Dasatinib unterliegt einer ausgeprägten Metabolisierung, wobei mehrere Enzyme an der Bildung der Metaboliten beteiligt sind.
- In gesunden Probanden, denen 100 mg 14C-markiertes Dasatinib gegeben wurde, bestand die zirkulierende Radioaktivität im Plasma zu 29% aus unverändertem Dasatinib.
- Dasatinib-Metaboliten spielen wahrscheinlich keine entscheidende Rolle bei der Pharmakologie des Arzneimittels.
- CYP3A4 ist ein Hauptenzym, das für die Metabolisierung von Dasatinib verantwortlich ist.
Elimination
- Die mittlere terminale Halbwertzeit von Dasatinib beträgt 3 bis 5 Stunden.
- Die mittlere scheinbare orale Clearance beträgt 363,8 l/h (CV% 81,3%)
Dosierung
Zu Beginn der Therapie von chronischen Phase der CML wird eine Dosis von 100 mg Dasatinib einmal täglich empfohlen. Die empfohlene Initialdosis in der akzelerierten Phase oder in der myeloischen oder lymphatischen Blastenkrise (fortgeschrittene Stadien) der CML oder bei Ph+ ALL beträgt 140 mg Dasatinib einmal täglich
Nebenwirkungen
Bei der Anwendung von Dasatinib kam es in klinischen Studien sehr häufig (≥1/10) zu folgenden Nebenwirkungen:
- Infektionen (dazu gehören bakterielle, virale, mykotische und nicht spezifizierte Infektionen)
- Myelosuppression (einschließlich Anämie, Neutropenie, Thrombozytopenie)
- Kopfschmerz
- Blutung
- Pleuraerguss, Dyspnoe
- Diarrhoe, Erbrechen, Übelkeit, Abdominalschmerz
- Hautausschlag
- Schmerzen des Muskel- und Skelettsystems
- Peripheres Ödemi , Fatigue, Fieber, Gesichtsödem
Wechselwirkungen
Dasatinib ist Substrat und Inhibitor von Cytochrom P450 (CYP) 3A4. Daher kann die gleichzeitige Anwendung von Arzneimitteln, die hauptsächlich von CYP3A4 metabolisiert werden oder die Aktivität von CYP3A4 beeinflussen zu Wechselwirkungen kommen.
Die gleichzeitige Anwendung von Dasatinib und einem Histamin-2 (H2)-Antagonisten (z. B. Famotidin), Protonenpumpeninhibitor (z. B. Omeprazol) oder Aluminiumhydroxid/Magnesiumhydroxid kann die Dasatinib-Exposition reduzieren. Daher wird die Anwendung von H 2-Antagonisten und Protonenpumpeninhibitoren nicht empfohlen, und Aluminiumhydroxid/Magnesiumhydroxid-Präparate sollten bis 2 Stunden vor und ab 2 Stunden nach der Anwendung von Dasatinib gegeben werden.
Kontraindikationen
Bei bekannter Überempfindlichkeit gegen den Wirkstoff dard Dasatinib nicht angewendet werden.
Schwangerschaft
Bei Anwendung in der Schwangerschaft kann Dasatinib zu kongenitalen Missbildungen einschließlich Defekten des Neuralrohrs führen. Darüber hinaus haben tierexperimentelle Studien eine Reproduktionstoxizität gezeigt. Dasatinib darf deshalb während der Schwangerschaft nicht angewendet werden, es sei denn, der klinische Zustand der Patientin erfordert eine Behandlung.
Stillzeit
Es gibt nur unzureichende/eingeschränkte Informationen zur Exkretion von Dasatinib in die Muttermilch von Menschen und Tieren. Physikalisch-chemische und die verfügbaren pharmakodynamischen/toxikologischen Daten lassen darauf schließen, dass Dasatinib in die Muttermilch übergeht, so dass ein Risiko für Säuglinge nicht ausgeschlossen werden kann.
Während der Behandlung sollte das Stillen deshalb eingestellt werden.
Verkehrstüchtigkeit
Dasatinib hat geringen Einfluss auf die Verkehrstüchtigkeit und die Fähigkeit zum Bedienen von Maschinen, da es unter der Behandlung zu Schwindelgefühl oder unscharfem Sehen kommen kann.
Wirkstoff-Informationen
EMA: Fachinformation Sprycel
-
Daruph 16 mg Filmtabletten
Zentiva Pharma GmbH
-
Daruph 40 mg Filmtabletten
Zentiva Pharma GmbH
-
Daruph 55 mg Filmtabletten
Zentiva Pharma GmbH
-
Daruph 63 mg Filmtabletten
Zentiva Pharma GmbH
-
Daruph 79 mg Filmtabletten
Zentiva Pharma GmbH
-
Daruph 111 mg Filmtabletten
Zentiva Pharma GmbH
-
Dasatilen® 20 mg Filmtabletten
TAD Pharma GmbH
-
Dasatilen® 50 mg Filmtabletten
TAD Pharma GmbH
-
Dasatilen® 70 mg Filmtabletten
TAD Pharma GmbH
-
Dasatilen® 80 mg Filmtabletten
TAD Pharma GmbH
-
Dasatilen® 100 mg Filmtabletten
TAD Pharma GmbH
-
Dasatilen® 140 mg Filmtabletten
TAD Pharma GmbH
-
Dasatinib - 1 A Pharma® 20 mg Filmtabletten
1 A Pharma GmbH
-
Dasatinib - 1 A Pharma® 50 mg Filmtabletten
1 A Pharma GmbH
-
Dasatinib - 1 A Pharma® 70 mg Filmtabletten
1 A Pharma GmbH
-
Dasatinib - 1 A Pharma® 80 mg Filmtabletten
1 A Pharma GmbH
-
Dasatinib - 1 A Pharma® 100 mg Filmtabletten
1 A Pharma GmbH
-
Dasatinib - 1 A Pharma® 140 mg Filmtabletten
1 A Pharma GmbH
-
Dasatinib 101 Carefarm 100 mg Filmtabletten
1 0 1 Carefarm GmbH
-
Dasatinib AL 20 mg Filmtabletten
ALIUD PHARMA® GmbH
-
Dasatinib AL 20 mg Filmtabletten STADA
STADAPHARM GmbH
-
Dasatinib AL 50 mg Filmtabletten
ALIUD PHARMA® GmbH
-
Dasatinib AL 50 mg Filmtabletten STADA
STADAPHARM GmbH
-
Dasatinib AL 70 mg Filmtabletten
ALIUD PHARMA® GmbH
-
Dasatinib AL 70 mg Filmtabletten STADA
STADAPHARM GmbH
-
Dasatinib AL 80 mg Filmtabletten
ALIUD PHARMA® GmbH
-
Dasatinib AL 80 mg Filmtabletten STADA
STADAPHARM GmbH
-
Dasatinib AL 100 mg CC Pharma Filmtabletten
CC Pharma GmbH
-
Dasatinib AL 100 mg Filmtabletten
ALIUD PHARMA® GmbH
-
Dasatinib AL 100 mg Filmtabletten STADA
STADAPHARM GmbH
-
Dasatinib AL 140 mg Filmtabletten
ALIUD PHARMA® GmbH
-
Dasatinib AL 140 mg Filmtabletten STADA
STADAPHARM GmbH
-
Dasatinib Heumann 20 mg Filmtabletten
Heumann Pharma GmbH & Co. Generica KG
-
Dasatinib Heumann 50 mg Filmtabletten
Heumann Pharma GmbH & Co. Generica KG
-
Dasatinib Heumann 70 mg Filmtabletten
Heumann Pharma GmbH & Co. Generica KG
-
Dasatinib Heumann 80 mg Filmtabletten
Heumann Pharma GmbH & Co. Generica KG
-
Dasatinib Heumann 100 mg Filmtabletten
Heumann Pharma GmbH & Co. Generica KG
-
Dasatinib Heumann 140 mg Filmtabletten
Heumann Pharma GmbH & Co. Generica KG
-
Dasatinib® Mylan 50 mg Filmtabletten
Viatris Healthcare GmbH
-
Dasatinib® Mylan 80 mg Filmtabletten
Viatris Healthcare GmbH
-
Dasatinib-ratiopharm® 20 mg Filmtabletten
ratiopharm GmbH
-
Dasatinib-ratiopharm® 50 mg Filmtabletten
ratiopharm GmbH
-
Dasatinib-ratiopharm® 70 mg Filmtabletten
ratiopharm GmbH
-
Dasatinib-ratiopharm® 80 mg Filmtabletten
ratiopharm GmbH
-
Dasatinib-ratiopharm® 100 mg Filmtabletten
ratiopharm GmbH
-
Dasatinib-ratiopharm® 140 mg Filmtabletten
ratiopharm GmbH
-
Dasatinib Tillomed 20 mg Filmtabletten
Tillomed Pharma GmbH
-
Dasatinib Tillomed 50 mg Filmtabletten
Tillomed Pharma GmbH
-
Dasatinib Tillomed 70 mg Filmtabletten
Tillomed Pharma GmbH
-
Dasatinib Tillomed 80 mg Filmtabletten
Tillomed Pharma GmbH














