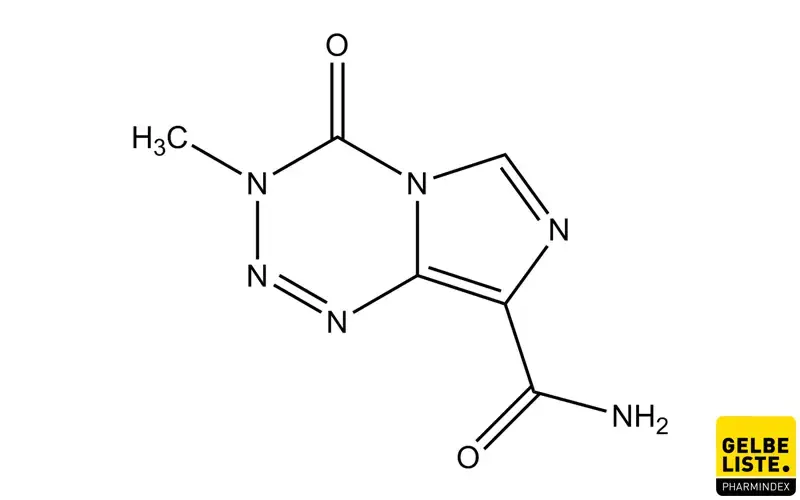
Temozolomid
Das Prodrug Temozolomid gehört zur Wirkstoffklasse der Alkylanzien. Aufgrund seiner lipophilen Grundstruktur kann der Wirkstoff die Blut-Hirn-Schranke passieren und ist somit für die Behandlung von malignen Gliomen geeignet.
Temozolomid: Übersicht
Anwendung
Temozolomid ist indiziert zur Behandlung von:
Glioblastoma multiforme
- Erwachsene Patienten mit erstmalig diagnostiziertem Glioblastoma multiforme begleitend zur Radiotherapie (RT) und anschließend als Monotherapie
Malignen Gliomen
- Kinder ab 3 Jahren, Jugendliche und erwachsene Patienten mit einem nach Standardtherapie rezidivierenden oder progredienten malignen Gliom, wie z.B. Glioblastoma multiforme, oder anaplastischen Astrozytom
Wirkmechanismus
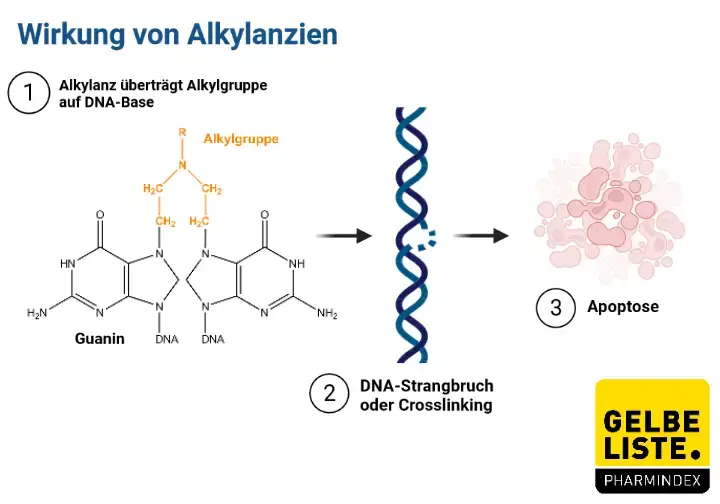
Das zytotoxische Alkylans Temozolomid ist ein Triazen-Derivat, das bei physiologischem pH-Wert in seine aktive Wirkform Monomethyltriazenylimidazolcarboxamid (MTIC) umgewandelt wird. MTIC alkyliert vorwiegend Guanin-Basen. Dabei wird die Zytotoxizität hauptsächlich auf die Alkylierung an der O-6-Position von Guanin mit zusätzlicher Alkylierung an der N-7-Position zurückgeführt.
Maligne Tumorzellen sind auf DNA-Replikationsmechanismen angewiesen, um schnelle Zellteilungsraten aufrecht zu erhalten. Eine Modifikation der DNA durch Alkylierung der DNA-Basen kann die DNA-Synthese hemmen und folglich die Proliferation von schnell teilenden Zellen verhindern.
Die ausgeprägte Lipophilie des Prodrugs Temozolomid ermöglicht die Überwindung der Blut-Hirn-Schranke. Insbesondere für die Therapie von malignen Gliomen ist eine Blut-Hirn-Schranken-Gängigkeit vorteilhaft.
Dosierung
Erstmalig diagnostizierten Glioblastoma multiforme (Erwachsene)
Temozolomid wird in Kombination mit fokaler Strahlentherapie (Begleittherapie -Phase) angewendet, gefolgt von bis zu 6 Zyklen Temozolomid-Monotherapie (Monotherapie-Phase).
Begleittherapie-Phase
Temozolomid wird täglich oral verabreicht mit einer Dosis von 75 mg/m2 für 42 Tage gleichzeitig mit fokaler Radiotherapie (60 Gy angewendet in 30 Fraktionen). Es werden keine Dosisreduktionen empfohlen, aber über eine Verzögerung oder einen Abbruch der Temozolomid-Anwendung sollte wöchentlich entsprechend hämatologischen und nicht-hämatologischen Toxizitätskriterien entschieden werden.
Die Anwendung von Temozolomid kann während der Begleitphase von 42 Tagen (bis zu 49 Tagen) durchgängig angewendet werden, wenn alle der folgenden Bedingungen erfüllt sind:
- absolute Zahl der neutrophilen Granulozyten (Absolute Neutrophil Count, ANC) ≥ 1,5 x 109/l
- Zahl der Thrombozyten ≥ 100 x 109/l
- nicht-hämatologische Toxizität bewertet nach Common Toxicity Criteria (CTC) ≤ Grad 1 (außer Haarausfall, Übelkeit und Erbrechen).
Monotherapie-Phase
Vier Wochen nach Beendigung der Begleittherapie wird Temozolomid für bis zu 6 Zyklen als Monotherapie angewendet. Die Dosis in Zyklus 1 (Monotherapie) ist 150 mg/m2 einmal täglich für
5 Tage gefolgt von 23 Tagen ohne Behandlung. Zu Beginn von Zyklus 2 wird die Dosis auf 200 mg/m2 erhöht, wenn die nicht-hämatologische Toxizität nach CTC für Zyklus 1 bewertet wurde.
Wurde die Dosierung im Zyklus 2 nicht erhöht, so sollte auch in den folgenden Zyklen die Dosierung nicht erhöht werden. Sobald die Dosierung erhöht wurde, wird sie bei 200 mg/m2 pro Tag über die ersten 5 Tage jedes folgenden Zyklus beibehalten, außer Toxizität tritt auf.
Während der Behandlung sollte am Tag 22 (21 Tage nach der ersten Temozolomid-Dosis) ein komplettes Blutbild erstellt werden.
Rezidiv oder Fortschreiten des malignen Glioms (Erwachsene oder pädiatrische Patienten im Alter von 3 Jahren oder älter)
Ein Therapiezyklus umfasst 28 Tage. Bei Patienten ohne vorherige Chemotherapie wird Temozolomid in einer Dosis von 200 mg/m² Körperoberfläche einmal täglich oral in den ersten 5 Tagen angewendet gefolgt von einer Anwendungspause von 23 Tagen (insgesamt 28 Tage).
Bei chemotherapeutisch vorbehandelten Patienten beträgt die Initialdosis 150 mg/m² Körperoberfläche einmal täglich, die beim zweiten Zyklus auf 200 mg/m² Körperoberfläche einmal täglich über die Dauer von 5 Tagen gesteigert wird, vorausgesetzt, es tritt keine hämatologische Toxizität auf.
Nebenwirkungen
Die am häufigsten berichteten Nebenwirkungen unter der Anwendung von Temozolomid sind:
- Übelkeit
- Erbrechen
- Obstipation
- Anorexie
- Kopfschmerzen
- Müdigkeit
- Konvulsionen
- Ausschlag
Wechselwirkungen
Die Einnahme von Temozolomid mit Nahrung führte zu einer Abnahme der Cmax um 33% und der Fläche unter der Kurve (AUC) um 9%. Da nicht ausgeschlossen werden kann, dass diese Auswirkungen klinisch relevant sind, sollte Temozolomid ohne Nahrung angewendet werden.
Kontraindikationen
Temozolomid darf nicht angewendet werden bei:
- Überempfindlichkeit gegen den Wirkstoff
- Überempfindlichkeit gegen Dacarbazin (DTIC)
- Schwerer Myelosuppression
Schwangerschaft
Temozolomid darf nicht bei schwangeren Frauen angewendet werden. Wenn die Anwendung während der Schwangerschaft dennoch in Betracht gezogen werden muss, ist die Patientin über das potenzielle Risiko für den Fetus zu informieren.
Stillzeit
Es ist nicht bekannt, ob Temozolomid beim Menschen in die Muttermilch übergeht. Aus diesem Grund muss während der Behandlung abgestillt werden.
Verkehrstüchtigkeit
Temozolomid hat geringen Einfluss auf die Verkehrstüchtigkeit und die Fähigkeit zum Bedienen von Maschinen, da unter der Anwendung Müdigkeit und Somnolenz auftreten können.
Alternativen
Die Therapiealternativen richten sich nach dem jeweiligen Indikationsgebiet und sind darüber hinaus abhängig von patientenindividuellen Faktoren wie dem Alter der Patienten, Komorbiditäten oder dem Schweregrad der Erkrankung.
Zusätzlich sollte das Mutationsprofil berücksichtigt werden.
Gliome (im Erwachsenenalter)
- Tumorresektion
- Strahlentherapie
- Bevacizumab
- Kombination aus BRAF-Inhibitoren wie Dabrafenib und MEK-Inhibitoren wie Trametinib (bei BRAF-Mutation)
- Andere Zytostatika wie Procarbazin, Nitrosoharnstoffe (ACNU, BCNU, CCNU) oder Vincristin
- Supportive Therapie (z.B. Steroide)
- Tumor-Treating Fields (TTF)
Weitere Informationen können der jeweiligen Fachinformation entnommen werden.
Wirkstoff-Informationen
- EMA: Fachinformation Temodal
- Freissmuth et al., Pharmakologie und Toxikologie, 2020, Springer
- Mutschler et al., Mutschler Arzneimittelwirkungen, 2019, Wissenschaftliche Verlagsgesellschaft Stuttgart
- Onkopedia: Gliome im Erwachsenenalter, abgerufen am 07.09.2022
Abbildung
Created with Biorender
-
Temozolomid Devatis 5 mg Hartkapseln
Devatis GmbH
-
Temozolomid Devatis 20 mg Hartkapseln
Devatis GmbH
-
Temozolomid Devatis 100 mg Hartkapseln
Devatis GmbH
-
Temozolomid Devatis 140 mg Hartkapseln
Devatis GmbH
-
Temozolomid Devatis 180 mg Hartkapseln
Devatis GmbH
-
Temozolomid Devatis 250 mg Hartkapseln
Devatis GmbH
-
Temozolomid Fair-Med Healthcare 5 mg Hartkapseln
Fairmed Healthcare GmbH
-
Temozolomid Fair-Med Healthcare 20 mg Hartkapseln
Fairmed Healthcare GmbH
-
Temozolomid Fair-Med Healthcare 100 mg Hartkapseln
Fairmed Healthcare GmbH
-
Temozolomid Fair-Med Healthcare 140 mg Hartkapseln
Fairmed Healthcare GmbH
-
Temozolomid Fair-Med Healthcare 180 mg Hartkapseln
Fairmed Healthcare GmbH
-
Temozolomid Fair-Med Healthcare 250 mg Hartkapseln
Fairmed Healthcare GmbH
-
Temozolomid Fair-Med Healthcare Eris 5 mg Hartkapseln
Eris Pharma GmbH
-
Temozolomid Fair-Med Healthcare Eris 20 mg Hartkapseln
Eris Pharma GmbH
-
Temozolomid Fair-Med Healthcare Eris 100 mg Hartkapseln
Eris Pharma GmbH
-
Temozolomid Fair-Med Healthcare Eris 140 mg Hartkapseln
Eris Pharma GmbH
-
Temozolomid Fair-Med Healthcare Eris 180 mg Hartkapseln
Eris Pharma GmbH
-
Temozolomid Fair-Med Healthcare Eris 250 mg Hartkapseln
Eris Pharma GmbH
-
Temozolomid-ratiopharm® 5 mg Hartkapseln
ratiopharm GmbH
-
Temozolomid-ratiopharm® 20 mg Hartkapseln
ratiopharm GmbH
-
Temozolomid-ratiopharm® 100 mg Hartkapseln
ratiopharm GmbH
-
Temozolomid-ratiopharm® 140 mg Hartkapseln
ratiopharm GmbH
-
Temozolomid-ratiopharm® 180 mg Hartkapseln
ratiopharm GmbH
-
Temozolomid-ratiopharm® 250 mg Hartkapseln
ratiopharm GmbH
-
Temozolomid Reliance 5 mg Hartkapseln
Cipla Europe NV
-
Temozolomid Ribosepharm 5 mg Hartkapseln
Hikma Pharma GmbH
-
Temozolomid Ribosepharm 20 mg Hartkapseln
Hikma Pharma GmbH
-
Temozolomid Ribosepharm 100 mg Hartkapseln
Hikma Pharma GmbH
-
Temozolomid Ribosepharm 140 mg Hartkapseln
Hikma Pharma GmbH
-
Temozolomid Ribosepharm 180 mg Hartkapseln
Hikma Pharma GmbH
-
Temozolomid Ribosepharm 250 mg Hartkapseln
Hikma Pharma GmbH
-
Temozolomid Teva 100 mg BB Farma Hartkapseln
BB Farma S.R.L.
-
Temozolomid Teva 140 mg BB Farma Hartkapseln
BB Farma S.R.L.
-
Temozolomid Teva 180 mg BB Farma Hartkapseln
BB Farma S.R.L.
-
Temozolomid Teva 250 mg BB Farma Hartkapseln
BB Farma S.R.L.
-
Temozolomide SUN 5 mg Hartkapseln
Sun Pharmaceuticals Germany GmbH
-
Temozolomide SUN 20 mg BB Farma Hartkapseln
BB Farma S.R.L.
-
Temozolomide SUN 20 mg Hartkapseln
Sun Pharmaceuticals Germany GmbH
-
Temozolomide SUN 100 mg Abacus Hartkapseln
Abacus Medicine A/S
-
Temozolomide SUN 100 mg BB Farma Hartkapseln
BB Farma S.R.L.
-
Temozolomide SUN 100 mg Hartkapseln
Sun Pharmaceuticals Germany GmbH
-
Temozolomide SUN 140 mg 101 Carefarm Hartkapseln
1 0 1 Carefarm GmbH
-
Temozolomide SUN 140 mg Abacus Hartkapseln
Abacus Medicine A/S
-
Temozolomide SUN 140 mg BB Farma Hartkapseln
BB Farma S.R.L.
-
Temozolomide SUN 140 mg Hartkapseln
Sun Pharmaceuticals Germany GmbH
-
Temozolomide SUN 180 mg Abacus Hartkapseln
Abacus Medicine A/S
-
Temozolomide SUN 180 mg BB Farma Hartkapseln
BB Farma S.R.L.
-
Temozolomide SUN 180 mg Hartkapseln
Sun Pharmaceuticals Germany GmbH
-
Temozolomide SUN 250 mg Abacus Hartkapseln
Abacus Medicine A/S
-
Temozolomide SUN 250 mg BB Farma Hartkapseln
BB Farma S.R.L.