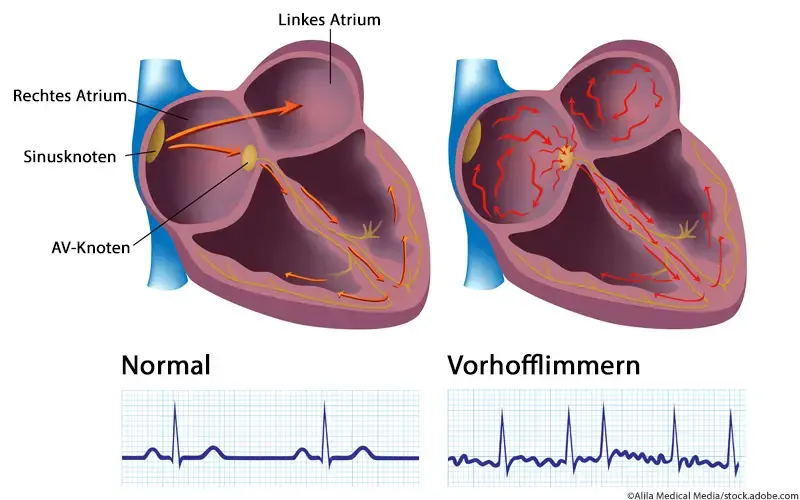
Vorhofflimmern (VHF) ist die häufigste anhaltende Herzrhythmusstörung und betrifft weltweit Millionen von Menschen. In Europa liegt die Prävalenz bei etwa 2 bis 3 % der erwachsenen Bevölkerung, mit steigender Tendenz aufgrund der demografischen Entwicklung. Die Erkrankung ist mit einem deutlich erhöhten Risiko für Schlaganfälle, Herzinsuffizienz und eine erhöhte Mortalität assoziiert. Trotz Fortschritten in der Behandlung bleiben die zugrunde liegenden molekularen Mechanismen weitgehend unklar, was die Entwicklung neuer, gezielter Therapieansätze erschwert.
Bisherige genomweite Assoziationsstudien (GWAS) haben bereits zahlreiche genetische Variationen identifiziert, die mit einem erhöhten Risiko für Vorhofflimmern verbunden sind. Allerdings war bekannt, dass weitere genetische Faktoren existieren, die bislang nicht erfasst wurden. Eine neue Meta-Analyse, veröffentlicht in 'Nature Genetics', erweitert nun dieses Wissen und liefert detailliertere Einblicke in die genetische Architektur von Vorhofflimmern.
Neue genetische Loci und polygenes Risikoprofil für Vorhofflimmern
In der aktuellen Untersuchung analysierte ein internationales Forscherteam genetische Daten von mehr als 180.000 Patienten mit Vorhofflimmern und fast 1,5 Millionen Kontrollpersonen. Durch die Zusammenführung von 68 Studien weltweit konnten über 350 genetische Loci identifiziert werden, die mit einem erhöhten VHF-Risiko assoziiert sind. Dies stellt eine Verdopplung der zuvor bekannten genetischen Risikoregionen dar.
Besonders relevant ist die Entdeckung von 139 Loci, die Gene umfassen, die an der Muskelkontraktilität, der Entwicklung des Herzmuskels und der Zellkommunikation beteiligt sind. Diese Gene sind in Vorhofmyozyten besonders aktiv, was darauf hindeutet, dass sie eine direkte Rolle in der Pathogenese von Vorhofflimmern spielen.
Ein weiteres zentrales Ergebnis der Studie ist die Optimierung der Risikovorhersage durch einen polygenen Risiko-Score (PRS). Dieser PRS, der auf den neu identifizierten genetischen Variationen basiert, zeigte eine bessere Vorhersagefähigkeit für das VHF-Risiko als der bisher genutzte CHARGE-AF Risiko-Score. Dies könnte zukünftig die Identifikation von Hochrisikopatienten verbessern und gezieltere Präventionsstrategien ermöglichen.
Seltene genetische Varianten und strukturelle Herzveränderungen
Neben der Untersuchung häufiger genetischer Variationen analysierte eine zweite Studie, ebenfalls in 'Nature Genetics' veröffentlicht, seltene genetische Varianten in über 50.000 VHF-Patienten und mehr als 270.000 Kontrollpersonen. Hierbei wurden neue pathogene Varianten in vier Genen entdeckt: MYBPC3, LMNA, PKP2 und KDM5B. Diese Gene sind bereits für ihre Rolle bei Kardiomyopathien bekannt, was darauf hindeutet, dass strukturelle Herzerkrankungen und Vorhofflimmern gemeinsame genetische Grundlagen haben könnten.
Zusätzlich identifizierte das Forscherteam strukturelle DNA-Veränderungen, die mit einem erhöhten VHF-Risiko assoziiert sind. Deletionen im CTNNA3-Gen sowie Duplikationen im GATA4-Gen beeinflussen offenbar die Herzmuskelstruktur und könnten zur elektrischen Instabilität der Vorhöfe beitragen.
Ein experimenteller Ansatz mit Gen-Editing-Techniken zeigte, dass eine Deaktivierung des KDM5B-Gens in Stammzell-abgeleiteten atrialen Myozyten zu Veränderungen der elektrischen Aktivität führt – ein Mechanismus, der bei Vorhofflimmern eine Rolle spielt.
Genetische Erkenntnisse als Grundlage für personalisierte Prävention und Therapie
Die Ergebnisse der beiden Studien erweitern das Verständnis der genetischen Grundlagen von Vorhofflimmern erheblich. Die Identifikation neuer Risiko-Allele könnte langfristig zu personalisierten Präventions- und Behandlungsstrategien führen. Der neue polygene Risiko-Score könnte insbesondere bei asymptomatischen Patienten helfen, frühzeitig Hochrisikopersonen zu identifizieren und Präventionsmaßnahmen gezielt einzuleiten.
Vorhofflimmern ist eine häufige Erkrankung, aber unsere pharmakologischen Therapieoptionen sind noch begrenzt, da wir die zugrunde liegenden molekularen Mechanismen bislang nur unzureichend verstehen. Diese Studien liefern neue potenzielle Ziele für die Arzneimittelentwicklung, erklärte Patrick Ellinor, Direktor der Cardiovascular Disease Initiative am Broad Institute of MIT and Harvard.
Genetische Forschung als Schlüssel zur besseren Behandlung von Vorhofflimmern
Die neu identifizierten Gene und genetischen Variationen müssen nun weiter untersucht werden, um ihre funktionellen Auswirkungen auf die Pathophysiologie von Vorhofflimmern besser zu verstehen. Zukünftige Forschungsarbeiten könnten klären, ob gezielte genetische Interventionen oder personalisierte Therapieansätze das Krankheitsrisiko senken oder die Progression von Vorhofflimmern verlangsamen können.
Große, internationale Konsortien wie das AFGen Consortium spielen eine entscheidende Rolle bei diesen Untersuchungen. Keine einzelne Studie ist groß genug, um bedeutende Ergebnisse zu liefern. Durch internationale Zusammenarbeit und den offenen Austausch von Daten können wir jedoch Fortschritte erzielen, die letztlich die Patientenversorgung verbessern, so Ellinor.