Aflibercept
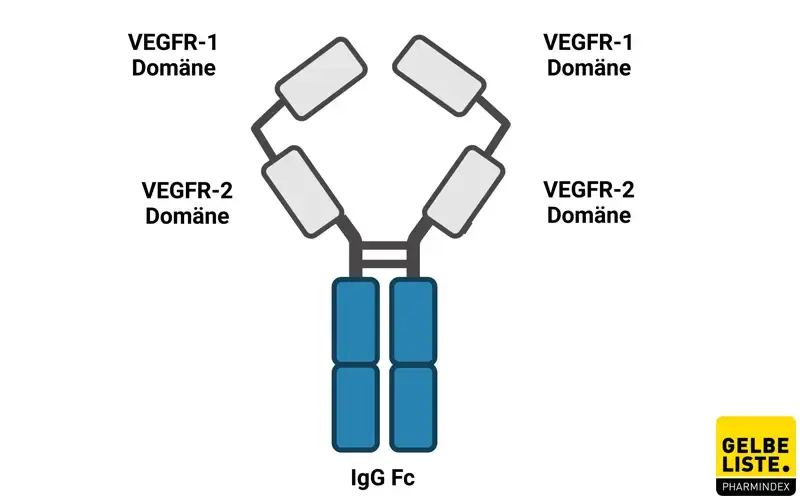
Aflibercept ist ein rekombinantes Fusionsprotein, das VEGF-A und PlGF mit hoher Affinität bindet. Durch Hemmung pathologischer Angiogenese und Gefäßpermeabilität wird es intravitreal bei exsudativen Netzhauterkrankungen wie nAMD oder DMÖ eingesetzt.
Aflibercept: Übersicht
Anwendung
Aflibercept wird zur Behandlung von Netzhauterkrankungen eingesetzt, bei denen ein durchlässiges oder krankhaft neugebildetes Gefäßsystem zu einer Visusverschlechterung führt. Die zugelassenen Anwendungsgebiete unterscheiden sich je nach Wirkstoffkonzentration:
Eine Konzentration von 40 mg/ml ist zugelassen bei Erwachsenen zur Behandlung
- der neovaskulären (feuchten) altersbedingten Makuladegeneration (nAMD),
- von Visusbeeinträchtigungen infolge eines Makulaödems nach retinalem Venenverschluss (RVV) (Venenastverschluss [VAV] oder Zentralvenenverschluss [ZVV]),
- von Visusbeeinträchtigungen durch diabetisches Makulaödem (DMÖ),
- sowie bei Visusbeeinträchtigungen durch myope choroidale Neovaskularisation (mCNV).
Eine Konzentration von 114,3 mg/ml wird bei Erwachsenen eingesetzt zur
- Behandlung der neovaskulären (feuchten) altersbedingten Makuladegeneration (nAMD),
- und bei Visusverlust durch diabetisches Makulaödem (DMÖ).
Anwendungsart
Aflibercept darf ausschließlich als intravitreale Injektion verabreicht werden und ist nur durch einen qualifizierten Arzt mit Erfahrung in der Durchführung intravitrealer Injektionen anzuwenden. Die Applikation muss unter streng aseptischen Bedingungen erfolgen, einschließlich chirurgischer Händedesinfektion, Verwendung steriler Handschuhe, eines sterilen Abdecktuchs sowie eines sterilen Lidsperrers.
Wirkmechanismus
Resorption und Verteilung
- Nach intravitrealer Injektion verbleibt Aflibercept überwiegend lokal im Auge und nur sehr geringe Mengen gelangen in den systemischen Kreislauf.
- Im Plasma liegt es überwiegend als inaktiver, stabiler VEGF‑Aflibercept‑Komplex vor; nur freies Aflibercept kann endogenes VEGF binden.
- Die maximalen Plasmakonzentrationen werden ein bis drei Tage nach Injektion erreicht (ca. 0,02 µg/ml) und sind nach etwa zwei Wochen in der Regel nicht mehr nachweisbar.
- Aflibercept reichert sich auch nach intravitrealer Anwendung alle 4 Wochen nicht im Plasma an.
Elimination
- Wie andere protein basierte Therapeutika wird sowohl freies als auch gebundenes Aflibercept über proteolytischen Abbau zu Peptiden und Aminosäuren zerlegt.
Dosierung
Aflibercept 40 mg/ml
Feuchte altersabhängige Makuladegeneration (AMD)
- Initial: 2 mg (entsprechend 0,05 ml) intravitreal mit drei aufeinanderfolgenden monatlichen Injektionen
- Erhaltung: basierend auf dem funktionellen und/oder morphologischen Befund Verlängerung auf 2-monatiges Behandlungsintervall
- Alternativ: "Treat and Extend" Dosierungsschema mit Verlängerung der Injektionsintervalle in 2- oder 4-wöchigen Schritten basierend auf dem funktionellen und/oder morphologischen Befund
- Bei Befundverschlechterung: Intervallverkürzung
Makulaödem infolge eines retinalen Venenverschlusses (ZVV oder VAV)
- Initial und Erhaltung: 2 mg (entsprechend 0,05 ml) monatlich
- Behandlungsdauer: bis der max. Visus erreicht ist und/oder keine Anzeichen von Krankheitsaktivität mehr zu erkennen sind, drei oder mehr aufeinanderfolgende monatliche Injektionen können notwendig sein
- Ende der Behandlung: wenn funktioneller und/oder morphologischer Befund darauf hinweisen, dass Patient nicht von einer weiteren Behandlung profitiert
- Alternativ: Unter Aufrechterhaltung des funktionellen und/oder morphologischen Befundes individuelles „Treat and Extend“-Schema mit schrittweiser Intervallverlängerung
- Bei Befundverschlechterung: Intervallverkürzung
Diabetisches Makulaödem (DMÖ)
- Initial: 2 mg (entsprechend 0,05 ml) intravitreal mit fünf aufeinanderfolgenden monatlichen Injektionen
- Erhaltung: basierend auf dem funktionellen und/oder morphologischen Befund Verlängerung auf 2-monatiges Behandlungsintervall
- Alternativ: "Treat and Extend" Dosierungsschema mit Verlängerung der Injektionsintervalle in 2-wöchigen Schritten auf bis zu 4 Monate basierend auf dem funktionellen und/oder morphologischen Befund
- Injektionsintervalle unter 4 Wochen wurden nicht untersucht
- Bei Befundverschlechterung: Intervallverkürzung
Myopie-assoziierte choroidale Neovaskularisation (mCNV)
- Einmalig: 2 mg (entsprechend 0,05 ml) als intravitreale Injektion
- Weitere Injektionen bei erneutem Krankheitsnachweis möglich
- Mindestabstand: 1 Monat
Aflibercept 114,3 mg/ml
nAMD und DMÖ
- Initial: 8 mg (entsprechend 0,07 ml) intravitreal mit drei aufeinanderfolgenden monatlichen Injektionen
- Erhaltung: Intervallverlängerung auf bis zu 4 Monate möglich
- Im Verlauf: Anpassung der Intervalle auf bis zu 6 Monate bei stabilem funktionellen und/oder morphologischen Befund. Bei Verschlechterung sollte eine Intervallverkürzung erfolgen.
- Mindestintervall in der Erhaltungsphase: 2 Monate
Umstellung von Aflibercept 40 mg/ml oder anderen Anti-VEGF-Therapien auf Aflibercept 114,3 mg/ml
- Bei stabilem Befund: bisherige Intervalle beibehalten oder verlängern
- Bei suboptimalem Ansprechen: Start mit bis zu drei aufeinanderfolgenden monatlichen Injektionen, danach individuelle Anpassung
- Kontrolle und Dosisanpassung erfolgen anhand funktioneller und morphologischer Befunde
Nebenwirkungen
Zu den häufigen Nebenwirkungen, die während einer Therapie mit Aflibercept auftreten können, zählen:
- verminderte Sehschärfe
- retinale Blutung
- Bindehautblutung
- Augenschmerzen
- Einriss des retinalen Pigmentepithels
- Abhebung des retinalen Pigmentepithels
- Netzhautdegeneration
- Glaskörperblutung
- Katarakt
- kortikale Katarakt
- Kernkatarakt
- subkapsuläre Katarakt
- Hornhauterosion
- Hornhautabrasion
- Anstieg des Augeninnendrucks
- verschwommenes Sehen
- Glaskörpertrübungen
- Glaskörperabhebung
- Schmerzen an der Injektionsstelle
- Fremdkörpergefühl im Auge
- erhöhter Tränenfluss
- Augenlidödem
- Blutung an der Injektionsstelle
- Keratitis punctata
- Bindehauthyperämie
- okulare Hyperämie
Die vollständigen Angaben können der jeweiligen Fachinformation entnommen werden.
Wechselwirkungen
Es liegen keine Studien zu möglichen Wechselwirkungen von Aflibercept mit anderen Arzneimitteln vor. Insbesondere wurde eine gleichzeitige Anwendung mit photodynamischer Therapie (PDT) unter Verwendung von Verteporfin nicht systematisch untersucht. Daher ist das Sicherheitsprofil einer solchen Kombinationstherapie unbekannt.
Kontraindikationen
Die Anwendung von Aflibercept ist generell kontraindiziert bei:
- Überempfindlichkeit gegen den Wirkstoff Aflibercept
- Bestehende oder vermutete okulare oder periokulare Infektion.
- Bestehende schwere intraokulare Entzündung.
Schwangerschaft
Zur Anwendung von Aflibercept in der Schwangerschaft liegen bislang keine Erfahrungen am Menschen vor. Obwohl die systemische Exposition nach intravitrealer Gabe sehr gering ist, sollte Aflibercept während der Schwangerschaft nur verabreicht werden, wenn der potenzielle Nutzen für die Mutter das mögliche Risiko für das ungeborene Kind überwiegt.
Stillzeit
Die verfügbaren Daten deuten darauf hin, dass Aflibercept in geringen Mengen in die Muttermilch übergehen kann. Aufgrund seiner molekularen Größe ist jedoch nur eine sehr geringe Aufnahme durch den Säugling zu erwarten. Über mögliche Auswirkungen auf gestillte Neugeborene oder Kinder liegen keine Erkenntnisse vor. Daher wird vorsichtshalber empfohlen, während der Behandlung mit Aflibercept nicht zu stillen.
Verkehrstüchtigkeit
Nach einer intravitrealen Injektion von Aflibercept oder einer entsprechenden augenärztlichen Untersuchung kann es vorübergehend zu Sehstörungen kommen. Diese können die Verkehrstüchtigkeit oder die Fähigkeit zum Bedienen von Maschinen beeinträchtigen. Patienten sollten daher erst wieder aktiv am Straßenverkehr teilnehmen oder Maschinen bedienen, wenn ihr Sehvermögen ausreichend stabil ist.
Anwendungshinweise
Bei der Anwendung von Aflibercept sind folgende Warnhinweise zu beachten:
Injektionsbedingte Komplikationen
Intravitreale Injektionen können zu Endophthalmitis, intraokularer Entzündung, rhegmatogener Netzhautablösung, Einriss der Netzhaut oder iatrogener traumatischer Katarakt führen. Aseptische Technik und Patientenedukation hinsichtlich der Erkennung und Meldung entsprechender Symptome sind zwingend erforderlich.
Erhöhter Augeninnendruck
Ein kurzfristiger Druckanstieg nach der Injektion ist möglich. Bei einem Augeninnendruck ≥30 mmHg sollte die Injektion zurückgestellt und der Druck zunächst kontrolliert werden.
Immunogenität
Aflibercept kann intraokulare Entzündungen auslösen. Patienten sollen über Anzeichen und Symptome einer intraokularen Entzündung wie z. B. Schmerzen, Photophobie oder Rötung informiert werden.
Systemische Effekte
Nicht-okulare Blutungen und thromboembolische Ereignisse sind möglich. Vorsicht bei kardiovaskulär vorbelasteten Patienten.
Behandlung beider Augen
Eine gleichzeitige Behandlung beider Augen wurde nicht systematisch untersucht. In solchen Fällen kann die systemische Belastung ansteigen.
Kombination mit anderen VEGF-Hemmern
Für eine gleichzeitige Anwendung mit anderen VEGF-Inhibitoren (systemisch oder okular) liegen keine Erfahrungen vor.
Pigmentepitheleinrisse
Besondere Vorsicht ist geboten bei Patienten mit ausgedehnten Abhebungen des retinalen Pigmentepithels, da ein erhöhtes Risiko für Risse besteht.
Netzhautveränderungen
Bei rhegmatogener Netzhautablösung oder Makulalöchern Grad 3 oder 4 sollte die Behandlung unterbrochen werden. Nach einem Netzhautriss darf erst nach Abheilung wieder behandelt werden.
Behandlungsunterbrechung empfohlen bei
- plötzliche Abnahme der bestkorrigierten Sehschärfe (BCVA) um ≥30 Buchstaben
- subretinaler Blutung im Zentrum der Fovea oder bei einer Blutungsgröße ≥50 % der Läsion
Intraokulare Eingriffe
Die Behandlung sollte 28 Tage vor oder nach einem durchgeführten oder geplanten intraokularen Eingriff ausgesetzt werden.
Schwangerschaft und Empfängnisschutz
Anwendung nur bei klarem Nutzen-Risiko-Verhältnis. Verhütung während und 3 Monate nach Therapie erforderlich.
Eingeschränkte Datenlage bei bestimmten Patientengruppen
- Patienten mit ischämischem ZVV und VAV
- Patienten mit Typ-1-Diabetes mit DMÖ oder bei Diabetikern mit HbA1c >12 % oder proliferativer diabetischer Retinopathie
- Patienten mit aktiver systemischer Infektion
- Patienten mit Netzhautablösung oder Makulaloch
- Patienten mit nicht eingestelltem Bluthochdruck
- Behandlung von mCNV bei nicht-asiatischen Patienten, vorbehandelter mCNV oder extrafovealen Läsionen
Wirkstoff-Informationen
- Freissmuth et al., Pharmakologie und Toxikologie, 2020, Springer.
- Fachinformationen ausgewählter Aflibercept-Hersteller (z. B. Eylea 40 mg/ml, kohlpharma).
-
Afiveg® 40 mg/ml Injektionslösung
STADAPHARM GmbH
-
Afiveg® 40 mg/ml Injektionslösung in einer Fertigspritze
STADAPHARM GmbH
-
Afqlir® 40 mg/ml Injektionslösung in einer Durchstechflasche
Hexal AG
-
Afqlir® 40 mg/ml Injektionslösung in einer Fertigspritze
Hexal AG
-
Ahzantive 40 mg/ml Injektionslösung in einer Fertigspritze
ratiopharm GmbH
-
Eiyzey® 40 mg/ml Injektionslösung in einer Durchstechflasche
OmniVision GmbH
-
Eiyzey® 40 mg/ml Injektionslösung in einer Fertigspritze
OmniVision GmbH
-
Eydenzelt™ 40 mg/ml Injektionslösung in einer Durchstechflasche
Celltrion Healthcare Deutschland GmbH
-
Eylea 40 mg/ml 1az Pharm Injektionslösung in einer Durchstechflasche
1az Pharm GmbH
-
Eylea 40 mg/ml 1az Pharm Injektionslösung in einer Fertigspritze
1az Pharm GmbH
-
Eylea 40 mg/ml 2care4 Injektionslösung in einer Fertigspritze
2care4 ApS
-
Eylea 40 mg/ml 101 Carefarm Injektionslösung in einer Fertigspritze
1 0 1 Carefarm GmbH
-
Eylea 40 mg/ml Aaragon Injektionslösung in einer Fertigspritze
Aaragon Pharma S.R.O.
-
Eylea 40 mg/ml Abacus Injektionslösung in einer Durchstechflasche
Abacus Medicine A/S
-
Eylea 40 mg/ml Abacus Injektionslösung in einer Fertigspritze
Abacus Medicine A/S
-
Eylea 40 mg/ml ACA Injektionslösung in einer Durchstechflasche
A.C.A. Müller ADAG Pharma AG
-
Eylea 40 mg/ml ACA Injektionslösung in einer Fertigspritze
A.C.A. Müller ADAG Pharma AG
-
Eylea 40 mg/ml Adequapharm Injektionslösung in einer Durchstechflasche
Adequapharm GmbH
-
Eylea 40 mg/ml axicorp Injektionslösung in einer Durchstechflasche
axicorp Pharma GmbH
-
Eylea 40 mg/ml axicorp Injektionslösung in einer Fertigspritze
axicorp Pharma GmbH
-
Eylea 40 mg/ml BB Farma Injektionslösung in einer Durchstechflasche
BB Farma S.R.L.
-
Eylea 40 mg/ml BB Farma Injektionslösung in einer Fertigspritze
BB Farma S.R.L.
-
Eylea 40 mg/ml CC Pharma Injektionslösung in einer Durchstechflasche
CC Pharma GmbH
-
Eylea 40 mg/ml CC Pharma Injektionslösung in einer Fertigspritze
CC Pharma GmbH
-
Eylea 40 mg/ml docpharm Injektionslösung in einer Fertigspritze
Docpharm GmbH
-
Eylea 40 mg/ml Emra Injektionslösung in einer Durchstechflasche
Emra-Med Arzneimittel GmbH
-
Eylea 40 mg/ml Eurim Injektionslösung in einer Durchstechflasche
Eurim-Pharm Arzneimittel GmbH
-
Eylea 40 mg/ml Eurim Injektionslösung in einer Fertigspritze
Eurim-Pharm Arzneimittel GmbH
-
Eylea 40 mg/ml European Injektionslösung in einer Durchstechflasche
European Pharma B.V.
-
Eylea 40 mg/ml European Injektionslösung in einer Fertigspritze
European Pharma B.V.
-
Eylea 40 mg/ml Fd Pharma Injektionslösung in einer Fertigspritze
FD Pharma GmbH
-
Eylea 40 mg/ml Haemato Pharm Injektionslösung in einer Durchstechflasche
HAEMATO PHARM GmbH
-
Eylea 40 mg/ml Haemato Pharm Injektionslösung in einer Fertigspritze
HAEMATO PHARM GmbH
-
Eylea 40 mg/ml hvd Injektionslösung in einer Durchstechflasche
hvd medical GmbH
-
Eylea 40 mg/ml hvd Injektionslösung in einer Fertigspritze
hvd medical GmbH
-
Eylea® 40 mg/ml Injektionslösung in einer Durchstechflasche
Bayer Vital GmbH Geschäftsbereich Pharma
-
Eylea® 40 mg/ml Injektionslösung in einer Fertigspritze
Bayer Vital GmbH Geschäftsbereich Pharma
-
Eylea 40 mg/ml kohlpharma Injektionslösung in einer Durchstechflasche
kohlpharma GmbH
-
Eylea 40 mg/ml kohlpharma Injektionslösung in einer Fertigspritze
kohlpharma GmbH
-
Eylea 40 mg/ml Medicopharm Injektionslösung in einer Durchstechflasche
Medicopharm AG
-
Eylea 40 mg/ml Medicopharm Injektionslösung in einer Fertigspritze
Medicopharm AG
-
Eylea 40 mg/ml NMG Pharma Injektionslösung in einer Durchstechflasche
NMG Pharma GmbH
-
Eylea 40 mg/ml NMG Pharma Injektionslösung in einer Fertigspritze
NMG Pharma GmbH
-
Eylea 40 mg/ml Orifarm Injektionslösung in einer Durchstechflasche
Orifarm GmbH
-
Eylea 40 mg/ml Orifarm Injektionslösung in einer Fertigspritze
Orifarm GmbH
-
Eylea 40 mg/ml Originalis Injektionslösung Durchstechflasche
Originalis B.V.
-
Eylea 40 mg/ml Originalis Injektionslösung in einer Fertigspritze
Originalis B.V.
-
Eylea 40 mg/ml Paranova Injektionslösung in einer Fertigspritze
Paranova Pack A/S
-
Eylea 40 mg/ml Synco Pharma Injektionslösung in einer Durchstechflasche
SynCo pharma B.V.
-
Eylea 40 mg/ml SynCo pharma Injektionslösung in einer Fertigspritze
SynCo pharma B.V.














