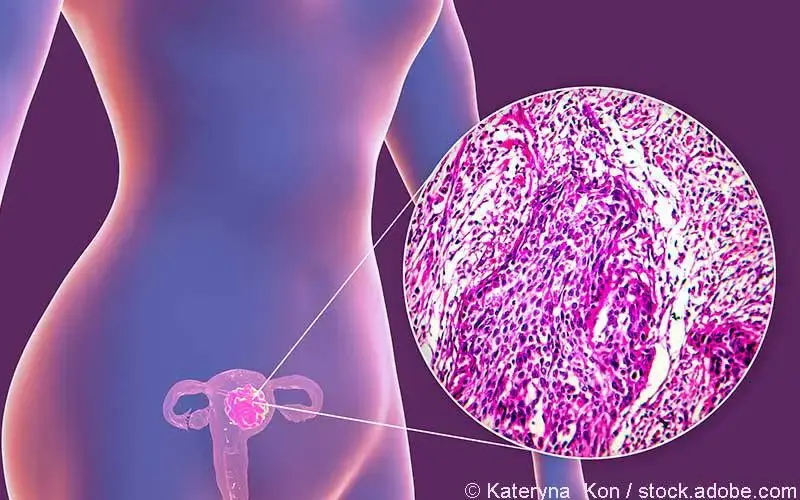
Das Endometriumkarzinom ist die häufigste maligne Erkrankung des weiblichen Genitaltrakts in den Industrieländern. Weltweit erkranken jährlich etwa 400.000 Frauen neu, rund 100.000 Betroffene sterben daran. Die Inzidenz steigt, was unter anderem mit steigender Adipositasprävalenz und veränderten Lebensgewohnheiten in Verbindung gebracht wird. Während diese etablierten Risikofaktoren wie Übergewicht, Hypertonie und Diabetes mellitus gut beschrieben sind, ist die genetische Prädisposition bislang nicht ausreichend charakterisiert.
Bisherige Erkenntnisse zur genetischen Prädisposition
Frühere genomweite Assoziationsstudien (GWAS) haben bereits mehrere Risikoloci identifiziert, die das Erkrankungsrisiko beeinflussen. Dennoch konnte die bekannte genetische Architektur bislang nur einen Teil der familiären Häufung erklären. Es bestand daher die Notwendigkeit, größere Kohorten in Metaanalysen einzubeziehen, um zusätzliche prädisponierende Loci aufzudecken.
Metaanalyse genomweiter Assoziationsstudien (GWAS)
Das Endometrial Cancer Association Consortium führte unter der Federführung der Medizinischen Hochschule Hannover eine groß angelegte Metaanalyse der genomweiten Assoziationsstudien (GWAS) durch: Sie verglichen die Genvarianten von insgesamt 17.278 Patientinnen mit Endometriumkarzinom mit dem Genom von 289.180 gesunden Frauen. Ausgewertet wurden Daten aus mehreren europäischen Biobanken (Großbritannien, Finnland, Estland) sowie aus Japan. Dieses Studiendesign erlaubte eine hohe statistische Power, um bisher nicht detektierte Risikovarianten zu identifizieren.
Fünf neue Risiko-Genloci entdeckt
Die Analyse führte zur Entdeckung von fünf zusätzlichen Risikoloci (3p25.2, 3q25.2, 6q22.31, 12q21.2 und 17q24.2). Genbasierte Untersuchungen bestätigten insbesondere Zusammenhänge mit NAV3 (12q21.2), PPARG (3p25.2) und BPTF (17q24.2). Darüber hinaus wurden zwei weitere Kandidatenregionen (ATF7IP2, RPP21) als potenziell relevant eingestuft.
Tumorsuppressorgen NAV3
Die funktionelle Validierung ergab, dass NAV3 eine tumorunterdrückende Rolle im Endometrium einnimmt:
- Herunterregulierung von NAV3 förderte Zellteilung und Wundheilungskapazität,
- Überexpression von NAV3 reduzierte die Zellviabilität und erhöhte den Zelltod.
Damit liefert die Studie erstmals Hinweise auf NAV3 als Tumorsuppressor bei Endometriumkarzinomzellen.
Ansatz für Risikostratifizierung, Prävention und Therapie
Mit der Identifikation weiterer Risikoloci wird die genetische Landschaft des Endometriumkarzinoms um rund ein Drittel erweitert.
Auch wenn ein unmittelbarer klinischer Nutzen derzeit noch nicht absehbar ist, könnten diese Daten langfristig zur Entwicklung von Risikostratifizierung und personalisierten Präventionsstrategien beitragen. Weiterführende Studien sollten untersuchen, wie diese genetischen Faktoren mit etablierten Risikoparametern interagieren und ob sich daraus Risikomodelle mit verbesserter prädiktiver Aussagekraft entwickeln lassen. Künftig könnten solche Modelle helfen, Hochrisikopatientinnen frühzeitig zu identifizieren und gezielt in Präventionsprogramme einzubinden.
Ein weiterer Forschungsansatz ergibt sich aus diesen Ergebnissen: Mit der Entdeckung, dass NAV3 als Tumorsuppressorgen fungiert, könnten sich möglicherweise neue Therapien entwickeln lassen.