
Die Bayer AG informiert in Abstimmung mit der Europäischen Arzneimittelagentur (EMA) und dem Bundesinstitut für Arzneimittel und Medizinprodukte (BfArM) über folgenden Sachverhalt:
Der Hersteller informiert in diesem Rote-Hand-Brief darüber, dass ein erhöhtes Risiko eines Anstiegs des Augeninnendrucks bei Anwendung der Eylea 40 mg/ml Injektionslösung in einer Fertigspritze (Aflibercept Lösung zur intravitrealen Injektion) besteht.

Die Bayer AG informiert in Abstimmung mit der Europäischen Arzneimittelagentur (EMA) und dem Bundesinstitut für Arzneimittel und Medizinprodukte (BfArM) über folgenden Sachverhalt:
Aflibercept (Eylea) wird bei Erwachsenen zur Behandlung der neovaskulären (feuchten) altersabhängigen Makuladegeneration (AMD), einer Visusbeeinträchtigung aufgrund eines Makulaödems infolge eines retinalen Venenverschlusses (RVV) (Venenastverschluss [VAV], Zentralvenenverschluss [ZVV]), eines diabetischen Makulaödems (DMÖ) oder einer myopen choroidalen Neovaskularisation (mCNV) eingesetzt.
Der Anstieg des Augeninnendrucks ist eine bekannte Nebenwirkung im Zusammenhang mit intravitrealen Injektionen, auch bei der Anwendung von Eylea. Nach Markteinführung der Eylea Fertigspritze in Europa im April 2020 wurde eine siebenfach höhere Melderate von erhöhtem Augeninnendruck bei Anwendung der Fertigspritze berichtet (etwa 1,1 Fälle pro 10.000 verkauften Fertigspritzen gegenüber 0,15 Fällen pro 10.000 verkauften Durchstechflaschen). Es gab Meldungen über vorübergehende Erhöhungen des Augeninnendrucks und reversible Visusbeeinträchtigungen nach intravitrealen Injektionen. Von den Fällen mit bekanntem Ausgang erholten sich die meisten ohne bleibende Schäden.
Es wurden keine Qualitätsmängel bei den Eylea Fertigspritzen oder der Injektionslösung festgestellt.
Nach weiterer Untersuchung der berichteten Fälle wird die Verabreichung eines zu hohen Injektionsvolumens aufgrund unsachgemäßer Handhabung bei der Vorbereitung und Injektion als Ursache für den erhöhten Augeninnendruck vermutet.
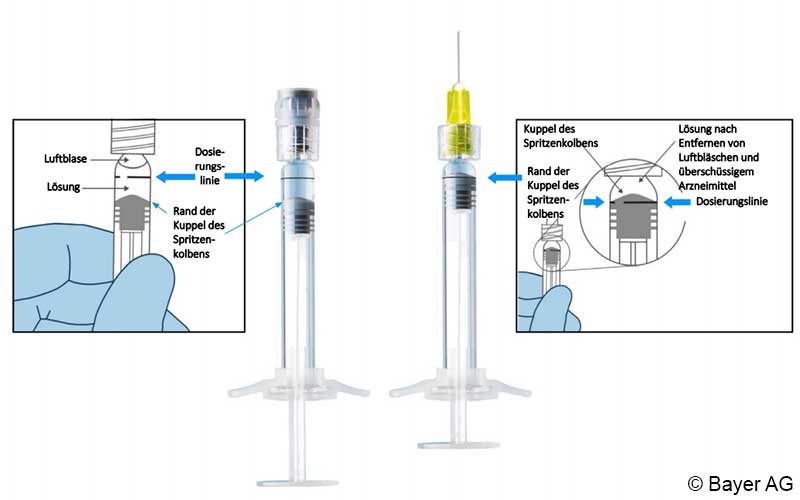
Außerdem handelt es sich bei der Eylea Fertigspritze um eine Glasspritze mit einem Gummikolben, der im Vergleich zu Kunststoffspritzen, wie sie bei der Anwendung der Durchstechflasche verwendet werden, etwas mehr Kraft bei der Anwendung erfordert. Um das Risiko für einen erhöhten Augeninnendruck weiter zu minimieren, sind Empfehlungen zur sachgemäßen Handhabung der Eylea Fertigspritze strikt zu befolgen:
Der Augeninnendruck sollte überwacht werden und, falls erforderlich, eine angemessene Behandlung eingeleitet werden. Unmittelbar nach der intravitrealen Injektion:
Es wird empfohlen, die bereitgestellten Schulungsmaterialien und die ausgehändigten Informationen zur sachgemäßen Anwendung der Fertigspritze, die in der Informationsbroschüre für Ärzte und dem Video zur intravitrealen Injektion der Eylea Schulungsmaterialien dargestellt sind, zu verwenden.
Die Schulungsmaterialien einschließlich des Patienten-Ratgebers sind über den Link https://produktinformation.bayer.de/eylea verfügbar und können auf Anfrage oder im Rahmen von Schulungen zusätzlich zur Verfügung gestellt werden.
Bayer AG Rote-Hand-Brief zu Eylea