Definition
Die Sarkoidose ist eine entzündliche Erkrankung unbekannter Ursache, die mit der Bildung von Granulomen einhergeht. Diese Granulome können in jedem Organ vorkommen, am häufigsten ist die Lunge betroffen [1].
Die Sarkoidose ist eine granulomatöse Erkrankung mit vielfältigen Organmanifestationen. Bei der Entstehung scheint eine genetische Prädisposition wichtig zu sein. Die Sarkoidose wird initial mit Glukokortikoiden behandelt, im Verlauf werden stärkere Immunsuppressiva eingesetzt.
Sarkoidose: Übersicht
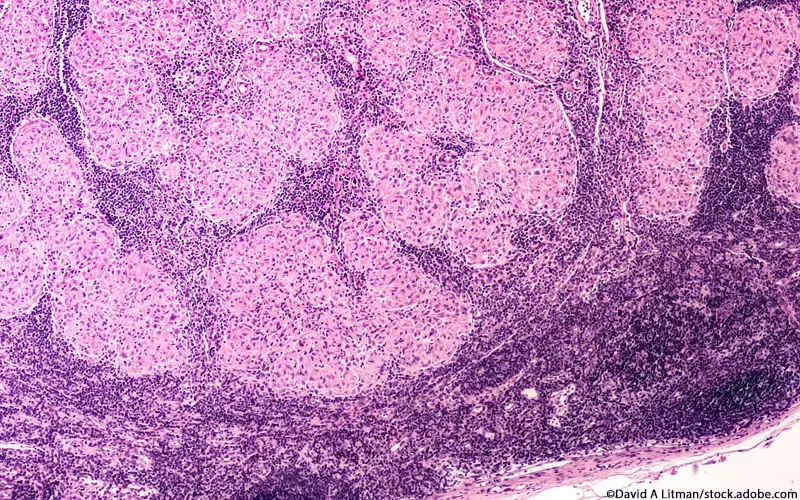
Die Sarkoidose ist eine entzündliche Erkrankung unbekannter Ursache, die mit der Bildung von Granulomen einhergeht. Diese Granulome können in jedem Organ vorkommen, am häufigsten ist die Lunge betroffen [1].
Die Inzidenz und Prävalenz von Sarkoidose schwankt stark zwischen verschiedenen geographischen Regionen und Altersgruppen. Es existieren aber auch Unterschiede zwischen den Geschlechtern und ethnischen Gruppen. So ist die Inzidenz bei Afroamerikanern mit 18 – 71 Fällen pro 100.000 Personen und in Skandinavien mit 11 – 24 Fällen pro 100.000 Personen im weltweiten Vergleich am höchsten. Die Inzidenz ist auf dem asiatischen Kontinent mit 1 pro 100.000 Personen am kleinsten.
Die Erkrankung beginnt durchschnittlich in einem Alter von 40 – 55 Jahren. Bei Männern wird die Erkrankung durchschnittlich 15 Jahre früher als bei Frauen erstmalig diagnostiziert, was möglicherweise mit wegfallenden protektiven Östrogenen während des Klimakteriums zusammenhängt. Insgesamt treten 45 – 60% der Fälle bei Frauen auf [1].
Eine genetische Prädisposition gilt als wichtiger Risikofaktor. Das Risiko, an Sarkoidose zu erkranken, steigt um das Zwei- bis Vierfache, wenn ein Familienmitglied ebenfalls erkrankt ist. Die Konkordanzrate bei monozygotischen Zwillingen beträgt 14,8% und bei dizygotischen Zwillingen 1,2%.
Auch Umwelteinflüsse wie die Inhalation von mikrobiellen Aerosolen oder anorganischen Partikeln scheinen mit einer erhöhten Inzidenz von Sarkoidose assoziiert zu sein. Hingegen ist Zigarettenrauchen ein insgesamt gut belegter Schutzfaktor, der das Risiko einer Sarkoidose-Erkrankung um ca. 50% senken kann. Übergewicht scheint ein relevanter Risikofaktor zu sein, während höhere Östrogenkonzentrationen möglicherweise protektiv wirken.
Bestimmte HLA-Allele sind mit unterschiedlichen Risiken für eine schwere Erkrankung assoziiert. HLA-DRB1*03 prädisponiert für eine spontan remittierende Erkrankung, während HLA-DRB1*14 und HLA-DRB1*15 mit einem chronischen Verlauf assoziiert sind [1,2].
Wahrscheinlich entsteht Sarkoidose infolge einer Exposition gegenüber bestimmten Antigenen bei Personen mit genetischer bzw. immunologischer Prädisposition. Das oder die kausalen Antigene sind bisher unbekannt. Immunologischen Dysregulationen wie eine übertriebene T-Helfer-1-Zellantwort und ein zahlenmäßiger und funktioneller Mangel an regulatorischen T-Zellen und invarianten natürlichen Killer-T-Zellen sind in der Genese von Sarkoidose involviert. Der JAK/STAT-Signalweg ist überaktiviert und stellt ein mögliches Ziel bei der Therapie von Sarkoidose dar.
Die wichtige Rolle der CD4+-T-Zellen wird dadurch verdeutlicht, dass eine HIV-induzierte CD4+-Lymphopenie zu einer Remission von Sarkoidose führt und eine antiretrovirale Therapie bei einer HIV-Infektion zu einer sarkoidoseähnlichen Bildung von Granulomen führen kann. Auch andere Medikamente mit einem starken Einfluss auf das Immunsystem wie Checkpoint-Inhibitoren können zu einer Sarkoidose bzw. sarkoidoseähnlichen granulomatösen Erkrankungen führen [1].
Da die Granulome der Sarkoidose in jedem Organ vorkommen können, sind die organspezifischen Symptome vielfältig. Neben Manifestationen an der Lunge, dem Herzen und dem Nervensystem sind häufig auch die Haut, die Nieren und die Augen betroffen. Das am stärksten die Lebensqualität einschränkende Symptom unabhängig von der Organmanifestation ist die Fatigue [1,3,4].
Bei 80-90% der Sarkoidose-Patienten sind die Lunge und/oder die mediastinalen Lymphknoten betroffen. Pulmonale Sarkoidose kann in obstruktiven und restriktiven Ventilationsstörungen resultieren und sich in persistierendem Husten und Dyspnoe äußern [1,3,4].
Bei ca. 5% der Sarkoidose-Patienten ist das Herz betroffen, auch wenn das Myokard wahrscheinlich bei mehr als 20% der Patienten in einem klinisch unauffälligen Maße betroffen ist. Kardiale Sarkoidose äußert sich z. B. in ventrikulären Arrhythmien, höhergradigen AV-Blocks oder progressiver Herzinsuffizienz [1,3,5].
Eine neurologische Beteiligung weisen 4-10% der Sarkoidose-Patienten auf. Dabei sind besonders häufig die Hirnnerven, die Meningen, das Hirnparenchym und das Rückenmark betroffen. Eine periphere Neuropathie der Hautnerven mit schmerzhafter Hyper- oder Hypästhesie kann im Rahmen eines nicht-granulomatösen parasarkoidalen Syndroms auftreten [1,3].
Das Löfgren-Syndrom ist eine Form der Sarkoidose, die bei jungen Frauen gehäuft vorkommt. Insgesamt stellt es ca. 5% der Sarkoidose-Fälle dar. Es ist gekennzeichnet durch ein akutes Auftreten und die Trias aus bihilärer Lymphadenopathie, Erythema nodosum und Arthritis mit Fieber [1,3,6].
Die Diagnostik der Sarkoidose ist komplex, da häufig mehr als ein Organ betroffen ist und die Symptome nicht immer eindeutig einem Organ zugeordnet werden können [1].
Eine Erhöhung der Serumkonzentration von Calcitriol, der Entzündungswerte und IgG sowie eine Hyperkalzämie und Hyperkalzurie können hinweisgebend für eine Sarkoidose sein. Die Serumkonzentration des Angiotensin-konvertierenden Enzyms (ACE) korreliert zwar mit der Anzahl der Granulome, eignet sich aufgrund der relativ geringen Sensitivität und Spezifität aber nur eingeschränkt für die Diagnose und Verlaufskontrolle. Der lösliche Interleukin-2-Rezeptor (sIL-2R) gilt als besserer Biomarker der Sarkoidose mit größerer Aussagekraft bei der Diagnose und Verlaufskontrolle [1,7].
Bei Patienten mit Verdacht auf das Löfgren-Syndrom wird die Diagnose bei typischer Symptomatik primär durch ein Röntgen-Thorax bestätigt. Bei vielen anderen Patienten ist eine Computertomographie (CT) der vermutlich betroffenen Organe zielführend. Eine CT kann dabei nicht nur die Diagnose stützen, sondern auch das Ausmaß der Verbreitung und etwaige Komplikationen wie eine Fibrose darstellen.
Auch die Echokardiographie, die Sonographie des Abdomens und die Magnetresonanztomographie (MRT) von Herz bzw. Gehirn spielen eine wichtige Rolle bei der Diagnose und Beurteilung der Ausbreitung.
Besonders bei kardialer und pulmonaler Sarkoidose ist die Positronenemissionstomographie (PET) mit 18F-Fluordesoxyglukose (18F-FDG) eine sensitive Methode der Bildgebung, um okkulte inflammatorische Herde zu entdecken [1,3,5].
Bei einer Bronchoskopie können typische Veränderungen bei endobronchialen Granulomen dargestellt werden. Endobronchiale ultraschallgesteuerte transbronchiale Nadelaspiration (EBUS-TBNA) oder konventionelle TBNA können genutzt werden, um andere Ursachen einer hilären Lymphadenopathie auszuschließen [1,3].
Eine histopathologische Sicherung der Diagnose sollte angestrebt werden, um die Sarkoidose gegen andere Erkrankungen abzugrenzen. Mögliche Differentialdiagnosen sind [1,3]:
Da in ca. 50% der Fälle eine Sarkoidose-Erkrankung innerhalb von zwei Jahren spontan zurückgeht, ist es wichtig, den Nutzen und die Risiken einer möglichen Therapie genau abzuwägen.
Als Erstlinientherapie gelten Glukokortikoide. Falls die Glukokortikoidtherapie bei Patienten mit symptomatischer pulmonaler Sarkoidose unzureichend war und zusätzlich ein erhöhtes Risiko für eine höhere Mortalität oder eine bleibende Behinderung aufgrund der Sarkoidose vorliegt, kann Methotrexat oder Infliximab eingesetzt werden.
Bei unzureichend kontrollierter Neurosarkoidose stellt Methotrexat die zweite und Infliximab die dritte Therapiestufe dar. Die gleiche Stufentherapie kann auch bei kardialer Sarkoidose in einem interdisziplinären Gremium erwogen werden.
Zusätzlich zur immunsuppressiven Therapie spielt die organspezifische Therapie eine wichtige Rolle, z. B. bei Herzinsuffizienz, Arrhythmien oder pulmonaler Hypertonie [1,3-5,8]
Obwohl in ca. 50% der Fälle eine spontane Remission auftritt, leiden viele Patienten sehr unter ihrer Erkrankung an Sarkoidose. Fünf Jahre nach der Erstdiagnose ist es unwahrscheinlich, dass eine Sarkoidose spontan zurückgeht.
Sarkoidose ist mit einem erhöhten Risiko für Infektionen, Herzinsuffizienz, zerebrovaskuläre Erkrankungen, venöse Thrombembolien, Neoplasien und rheumatologische Erkrankungen assoziiert. Auch die Mortalität ist insgesamt erhöht; dies gilt besonders für eine therapiebedürftige Sarkoidose [1,3,4].