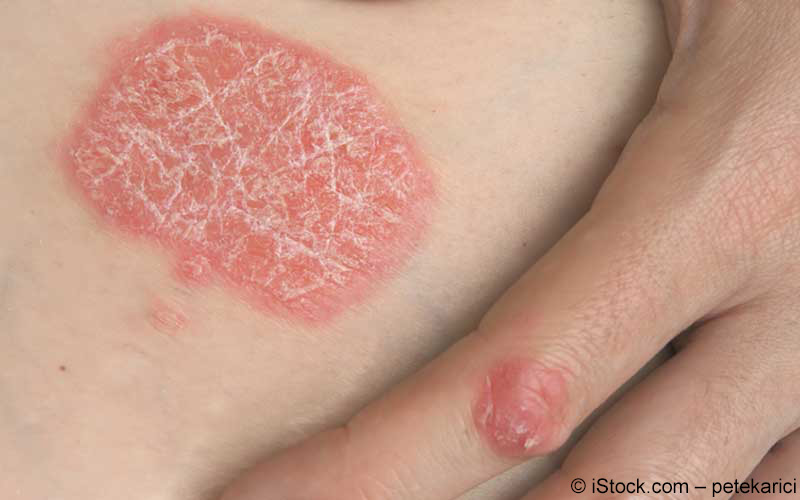
Amgevita des pharmzeutischen Unternehmens Amgen ist zur Behandlung bestimmter entzündlicher Erkrankungen bei Erwachsenen zugelassen, darunter mittelschwere bis heftige rheumatoide Arthritis, Psoriasis-Arthritis, schwere aktive ankylosierende Spondylitis (AS), schwere axiale Spondyloarthritis ohne radiographischen Nachweis von AS, mäßige bis schwere chronische Plaque-Psoriasis, mäßig bis schwerer Morbus Crohn und mäßig bis schwerer Colitis ulcerosa.
Amgevita ist auch für die Behandlung bestimmter pädiatrischer entzündlicher Erkrankungen, einschließlich mäßiger bis schwerer Morbus Crohn (ab 6 Jahren), schwerer chronischer Plaque-Psoriasis (ab 4 Jahren), enthesitis-assoziierter Arthritis (ab 6 Jahren) und polyartikulärer juveniler idiopathische Arthritis für Kinder ab 2 Jahren und älter zugelassen.
Amgevita wurde auf der Grundlage eines umfassenden Datenpakets zugelassen, das die Biosimilarität gegenüber Adalimumab auf der Grundlage analytischer, pharmakokinetischer und klinischer Daten unterstützt. Zusätzlich wurden zwei Phase-3-Studien eingereicht, die bei mittelschwerer bis schwerer Plaque-Psoriasis und moderaten bis schwerwiegenden Patienten mit rheumatoider Arthritis durchgeführt wurden. Die Phase-3-Studien trafen jeweils ihren primären Endpunkt, der keine klinisch bedeutsamen Unterschiede zu Adalimumab zeigte.
Amgevita wurde in den USA (U.S.) am 23. September 2016 von der US-amerikanischen Food and Drug Administration zugelassen. In den USA ist der Markenname AMJEVITA ™ (adalimumab-atto).
Wirkweise von Amgevita
In Amgevita ist der Wirkstoff Adalimumab enthalten. Adalimumab ist ein Tumornekrosefaktor alpha Inhibitor (TNFα). Der Wirkstoff bindet spezifisch an TNF, blockiert durch Wechselwirkung mit den p55- und p75-Zelloberflächen den TNF-Rezeptor und neutralisiert so die biologische Funktion von TNF: Adalimumab moduliert auch biologische Reaktionen, die durch TNF induziert oder reguliert werden, dazu gehören auch die für die Leukozyten Migration verantwortlichen Adhäsionsmoleküle ELAM-1, VCAM-1 und ICAM-1. Amgevita ist ein Humira–Biosimilar.











