Hintergrund
Die Global Initiative for Asthma (GINA) empfahl bis 2018 bei leichtem Asthma der Stufe 1 eine Monotherapie mit einem kurzwirksamen inhalativen Beta-Sympathomimetikum (short-acting beta-agonists [SABA]) bei Erwachsenen und Jugendlichen. Diese Behandlung wird nicht mehr empfohlen. Nach den neuen GINA-Empfehlungen, die 2019 veröffentlicht wurden, soll nun in Stufe 1 der Asthmatherapie bevorzugt ein niedrig-dosiertes inhalatives Glukokortikoid (inhaled corticosteroid [ICS]) in Kombination mit Formoterol bei Bedarf eingesetzt werden. Prof. Dr. Roland Buhl, Leiter des Schwerpunktes Pneumologie des Universitätsklinikums Mainz erläuterte in seinem Vortrag die Gründe, die zu dieser fundamentalen Änderung der Empfehlungen führten und welche Vorteile der neue Therapieansatz hat. [1]
Gründe für den Paradigmenwechsel
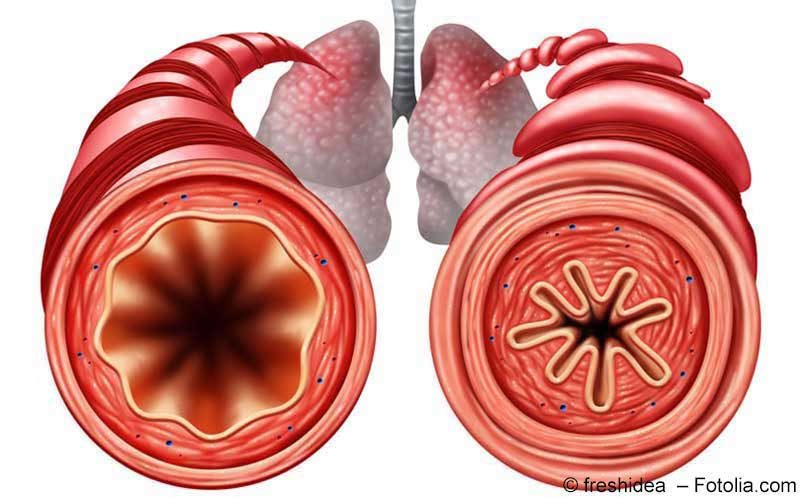
Die Erfahrung habe gezeigt, so Buhl, dass die SABA-Monotherapie auch Patienten mit leichtem Asthma nicht vor gravierenden Asthma-Risiken schütze, wie beispielsweise akuten Exazerbationen, lebensbedrohlichen Anfällen oder sogar den Tod durch Asthma. Erschwerend kämen die zum Teil erheblichen Nebenwirkungen hinzu, die mit SABA verbunden sein könnten. SABA könnten auch die entzündlichen Prozesse in den Luftwegen bei Asthma nicht kontrollieren. Mit Kombinationen von ICS und langwirksamen Beta-Sympathomimetika (long acting beta-agonist [LABA]) habe man hingegen sehr gute Erfahrungen hinsichtlich Wirksamkeit und Verträglichkeit gemacht.
Vorteile der Anwendung bei Bedarf
In der Stufe 1 empfiehlt GINA die Anwendung einer fixen ICS/Formoterol Kombination nur bei Asthma-Symptomen. Die Anwendung bei Bedarf ist intuitiv und entspricht den Bedürfnissen von Patienten, wie Buhl erklärt: “Wenn die Asthma-Symptome verschwunden sind, hört der Patient auf seinen „Reliever“ zu nehmen – genauso wie man auch die Einnahme von Schmerzmitteln stoppt, wenn der Kopfschmerz nachlässt.“
Die Befürchtung, dass die Anwendung bei Bedarf auf Dauer zu einer Verschlimmerung der Entzündungsprozesse in den Atemwegen führen und damit das Auftreten von Exazerbationen fördern könnte, wurde durch eine Studie von Beasley e al. (2019) widerlegt. [2] Es konnte gezeigt werden, dass sich die Werte für den Entzündungsmarker FeNO (fraktioniertes exhaliertes NO) über den Studienzeitraum von 52 Wochen bei der fixen Kombination Budenosid/Formoterol bei Bedarf nicht von einer Erhaltungstherapie mit Budenosid unterschieden.
Deutlich weniger Exazerbationen
Klinisch kam es in der dreiarmigen Studie unter Budenosid/Formoterol zu deutlich weniger Exazerbationen als unter SABA und zu etwa gleich viel Exazerbationen wie unter Erhaltungstherapie mit Budenosid. Allerdings erlitten Patienten bei Erhaltungstherapie mit Budenosid rund doppelt so viele schwere Exazerbationen wie die Budenosid/Formoterol Gruppe. Buhl führt dieses Ergebnis auf die intuitive Anwendung des Relievers zurück, der bei entsprechendem Bedarf vom Patienten intuitiv höher dosiert wird.
Einsatz von Biologika bei schwerem Asthma
Mittlerweile stehen zu Behandlung von schwerem nicht kontrollierbarem Asthma fünf monoklonale Antikörper zur Verfügung. Vor ihrem Einsatz stellt sich jedoch die Frage, ob der Patient überhaupt Vorteile von einer biologischen Therapie hat. In ihrem Vortrag auf dem virtuellen ERS Kongress hat Professor Dr. Celeste Michala Porsbjerg vom Bispebjerg-Frederiksberg Hospital und der Fakultät für Klinische Medizin der Universität Kopenhagen systematisch aufbereitet, wie man Patienten mit schwerem Asthma identifiziert, die tatsächlich von einer biologischen Therapie profitieren.[3]
„Schwer“ oder „schwierig zu behandeln?“
Vor dem Einsatz der Biologika muss genau überprüft werden, ob tatsächlich ein schweres nicht kontrolliertes Asthma vorliegt oder ein Asthma, das schwierig zu behandeln ist. In der SATS Studie wurde festgestellt, dass bei 88% der Patienten mit unkontrolliertem Asthma kein schweres Asthma sondern ein Asthma, das schwierig zu behandeln ist, vorlag. Nur 12% der Patienten mit unter unkontrolliertem Asthma litten unter einem schweren Asthma. [4]
Asthma, das schwierig zu behandeln ist
Bei Asthma, das schwierig zu behandeln ist, ist die schlechte Kontrolle die Folge von ungünstigen äußeren und inneren Umständen. Hierzu gehören zum Beispiel eine mangelhafte Therapieadhärenz, Fehler bei der Anwendung von Inhalationsgeräten, eine Exposition an Allergene oder reizende Substanzen oder Komorbiditäten. Wenn diese Faktoren ausgeschaltet oder gemanagt werden, kann das Asthma häufig mit der bisherigen oder einer klassischen Medikation unter Kontrolle gebracht werden. Schweres Asthma, hingegen, ist schwer zu kontrollieren, obwohl eine gute Therapieadhärenz und eine korrekte Anwendung der Inhalationsgeräte vorliegt und sowohl Expositionen als auch Komorbiditäten gut gemanagt werden.
Kann der Patient von Biologika profitieren?
Der Hauptnutzen von Biologika bei der Therapie von Asthma liegt in der Vorbeugung von Exazerbationen und Einsparung von oralen Kortikosteroiden (oral corticosteroids [OCS]). Nur in Einzelfällen lässt sich eine Verbesserung der Lungenfunktion und der klinischen Symptom erreichen, diese kann jedoch im individuellen Fall signifikant sein. Das heißt: Patienten mit hohem Exazerbationsrisiko und/oder Patienten, die regelmäßig OCS einnehmen, können theoretisch am meisten von einer biologischen Therapie profitieren.
Wer spricht auf die verschiedenen Biologika an?
Für das Ansprechen auf eine biologische Therapie gibt es außerdem je nach Antikörper unterschiedliche Prädiktoren.
- Anti IgE (Omalizumab): Eosinophile, FeNO, allergische Rhinitis, Beginn der Krankheit in der Kindheit.
- Anti-IL5 (Mepolizumab, Reslizumab, Benralizumab [anti-IL5R]): Eosinophile, Exazerbationsrate, Beginn der Erkrankung im Erwachsenenalter, Nasenpolypen
- Anti- IL4/13 (Dupilumab): Eosinophile, FeNO, Nasenpolypen.
Diese Prädiktoren sollten in ein Assessment vor der Behandlung mit Biologika berücksichtigt werden. „Ein systematisches Assessment vor der Behandlung der Patienten mit Biologika trägt entscheidend zum Therapieerfolg bei,“ schloss Pjorsberg ihren Vortrag.