Zunächst war unklar, ob der Corona-Impfstoff in Deutschland überhaupt auf den Markt kommen würde, da die EU-Kommission den Vorab-Kaufvertrag kündigen wollte. Nach einigen Verhandlungen werde die EU für 2022 nun doch 2,5 Millionen Dosen abnehmen. Ursprünglich geplant waren 60 Millionen Dosen bis 2023. Mit der Impfstoffbestellung zum 6. September 2022 konnten Arztpraxen erstmals den inaktivierten Ganzvirusimpfstoff bestellen.
Über den COVID-19-Impfstoff Valneva
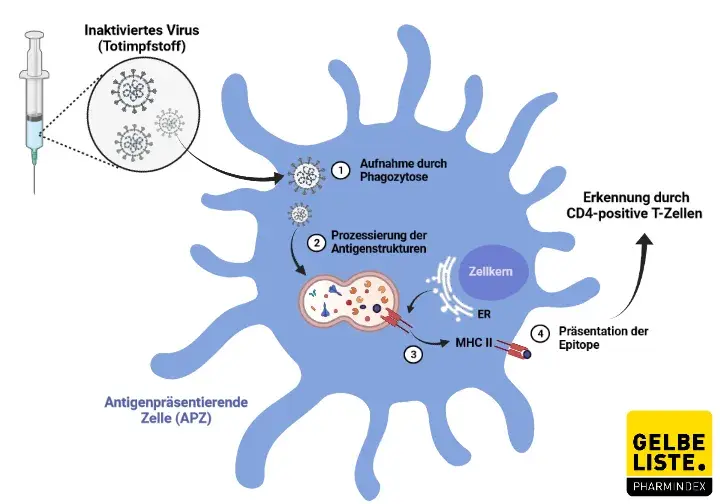
VLA2001 ist ein adjuvantierter, inaktivierter Ganzvirus-Impfstoff. Die Vakzine besteht aus inaktivierten ganzen SARS-CoV-2-Viruspartikeln mit hoher Spike-Protein-Dichte, in Kombination mit zwei Adjuvantien, Alum und CpG 1018. Die Kombination der beiden Adjuvanzien induzierte in präklinischen Studien höhere Antikörperspiegel als reine Alum-Formulierungen und eine Verschiebung der Immunantwort in Richtung Th1.
Der Impfstoff ist angezeigt für die aktive Immunisierung zur Vorbeugung gegen durch SARS-CoV-2 hervorgerufenes COVID-19 bei Personen zwischen 18 und 50 Jahren.
Wie wird der COVID-19-Impfstoff Valneva angewendet?
Der Impfstoff muss intramuskulär in den M. deltoideus des Oberarms injiziert werden.
Dosierung
Der COVID-19-Impfstoff Valneva wird intramuskulär in einer Impfserie mit zwei Dosen zu je 0,5 ml im Abstand von 28 Tagen appliziert.
Wie wirkt der COVID-19-Impfstoff Valneva?
Der COVID-19-Impfstoff Valneva enthält den ursprünglichen Stamm von SARS-CoV-2, der inaktiviert wurde und intakte Spike-Proteine auf der Virenoberfläche präsentiert. Der Impfstoff enthält außerdem die zwei Adjuvantien Aluminium und Cytosin-Phospho-Guanin, die zu einer Verstärkung der Immunantwort beitragen sollen.
Nach der Verabreichung induziert VLA2001 SARS-CoV-2-neutralisierende Antikörper sowie zelluläre Immunantworten (Th1) gegen das Spike-Protein und andere Oberflächenproteine, die zum Schutz gegen COVID-19 beitragen können.
Durch Verwendung des ganzen Viruspartikels, ist die zelluläre Immunantwort nicht auf das Spike-Protein beschränkt, sondern auch gegen andere Oberflächenantigene von SARS-CoV-2.