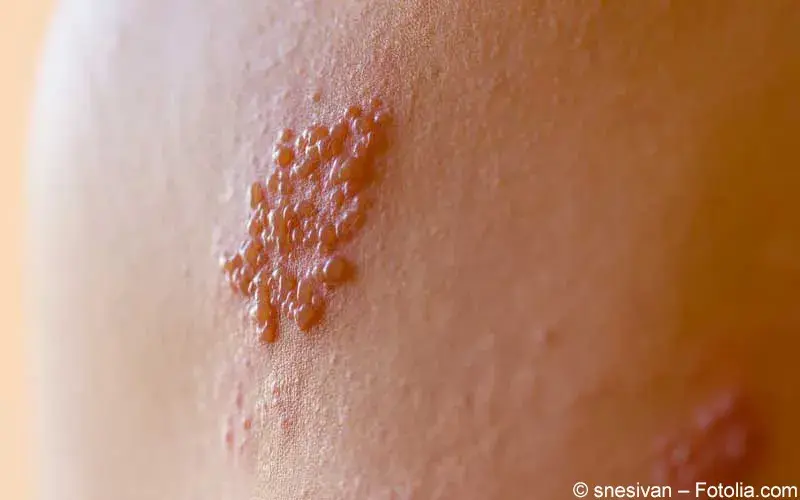
Herpes zoster-Impfstoffe
Subunit-Totimpfstoff (Shingrix)
Seit März 2018 ist ein adjunvanter Subunit-Totimpfstoff (Shingrix®) zur Verhinderung von Herpes zoster und postherpetischer Neuralgie für Personen ab 50 Jahren und ab 18 Jahren bei Personen mit erhöhtem Risiko zugelassen. Seit Mai 2018 ist er in Deutschland verfügbar.
Attenuierter Lebendimpfstoff (Zostavax®)
Zostavax® ist ein attenuierter Lebendimpfstoff, der seit 2006 zur Verhinderung eines Herpes Zoster bzw. einer postherpetischer Neuralgie für Personen ab dem Alter von 50 Jahren zugelassen ist. Der Impfstoff ist seit September 2013 in Deutschland verfügbar. Die STIKO sieht zum gegenwärtigen Zeitpunkt davon ab, die Impfung mit dem Herpes zoster-Lebendimpfstoff als Standardimpfung zu empfehlen. Die Entscheidung basiert auf der systematischen Bewertung der vorhandenen Daten zu Wirksamkeit, Schutzdauer und Sicherheit des Impfstoffs und wird durch die Ergebnisse einer mathematischen Modellierung zur Abschätzung der zu erwartenden epidemiologischen Effekte bekräftigt.
Nebenwirkungen der Herpes zoster-Impfstoffe
Shingrix: Die häufigsten Nebenwirkungen sind Schmerzen an der Injektionsstelle, Myalgien (Muskelschmerz), Müdigkeit und Kopfschmerzen. Die meisten dieser Reaktionen klangen nach zwei bis drei Tagen wieder ab. Siehe auch Shingrix Fachinformation.
Zostavax: in den zulassungsrelevanten klinischen Prüfungen stellten Reaktionen an der Injektionsstelle die häufigsten Nebenwirkungen dar. Kopfschmerz und Schmerz in der Extremität waren die häufigsten systemischen Nebenwirkungen. Die meisten dieser lokalen und systemischen Nebenwirkungen waren von geringer Intensität. Eine genaue Auflistung entnehmen Sie bitte der Zostavax Fachinformation.
Kontraindikationen
Shingrix: Zu den Kontraindikationen zählen Überempfindlichkeit gegen die Wirkstoffe oder gegen einen der sonstigen Bestandteile.
Zostavax:
- Bekannte Überempfindlichkeit gegen den Wirkstoff, einen der sonstigen Bestandteile des Impfstoffs oder einen der in Spuren vorhandenen Rückstände aus der Herstellung (z. B. Neomycin).
- Angeborene und erworbene Immundefizienz als Folge einer akuten oder chronischen Leukämie, eines Lymphoms, anderer Erkrankungen des Knochenmarks oder des lymphatischen Systems; Immundefizienz als Folge von HIV/AIDS; zelluläre Immundefizienz.
- Immunsuppressive Therapie (einschließlich hoher Dosen von Kortikosteroiden).
- ZOSTAVAX ist jedoch nicht kontraindiziert bei Personen unter topischer/inhalativer oder niedrig dosierter systemischer Kortikosteroidtherapie oder bei Personen unter Kortikosteroid-Substitutionstherapie, z. B. bei Nebenniereninsuffizienz.
- Aktive, unbehandelte Tuberkulose.
- Schwangerschaft. Darüber hinaus sollte nach der Impfung eine Schwangerschaft über einen Zeitraum von einem Monat verhindert werden.
Impfschema
Shingrix: Das Grundimmunisierungsschema besteht aus zwei Dosen mit jeweils 0,5 ml. Nach der ersten Dosis folgt eine zweite Dosis 2 Monate später. Falls es erforderlich ist, das Impfschema flexibel zu handhaben, kann die zweite Dosis im Abstand von 2 bis 6 Monaten nach der ersten Dosis verabreicht werden. Zur Notwendigkeit von Auffrischimpfungen nach Abschluss der Grundimmunisierung liegen keine Daten vor.
Zostavax: Alle Personen erhalten eine Dosis (0,65 ml). Ob eine Auffrischimpfung erforderlich ist, ist nicht bekannt. Zur Sicherheit und Wirksamkeit von ZOSTAVAX bei Kindern und Jugendlichen liegen keine Daten vor.
Impfschutz und Impfempfehlung
Die Wahrscheinlichkeit an Herpes zoster zu erkranken und die Schwere der Erkrankung nehmen mit dem Alter deutlich zu.
Der Herpes-zoster-Totimpfstoff ist daher von der STIKO seit Dezember 2018 als Standardimpfung für alle Personen ≥ 60 Jahren empfohlen.
Zusätzlich wird die Impfung mit dem Totimpfstoff für Personen ≥50 Jahren sowie für Erwachsene ab 18 mit einem erhöhten Risiko für das Auftreten eines Herpes zoster infolge einer Grundkrankheit oder für Menschen mit angeborener bzw. erworbener Immundefizienz bzw. Immunsuppression empfohlen. Dazu gehören u.a. Patienten mit HIV-Infektion, rheumatoider Arthritis, systemischem Lupus erythematodes, chronisch entzündlichen Darmerkrankungen, chronisch obstruktiven Lungenerkrankungen oder Asthma bronchiale, chronischer Niereninsuffizienz und Diabetes mellitus.
Ein erhöhtes Risiko besteht auch unter JAK-Inhibitoren und Anifrolumab. Bei gut kontrollierten Grunderkrankungen ist die Impfung nicht zwingend erforderlich.
Die Impfung bietet Schutz vor Herpes zoster und postherpetischer Neuralgie für Menschen ab 50 Jahren. Ab diesem Alter besitzt der Impfstoff eine Wirksamkeit von 92% zur Verhinderung von Herpes zoster und von 82% zur Prävention postherpetischer Neuralgie. Obwohl der Schutz vor Herpes zoster mit zunehmendem Alter leicht abnimmt, beträgt er bei Personen ab 70 Jahren immer noch etwa 90%.