-
Home
-
Wirkstoffgruppen
HIV-Therapeutika sind elementarer Bestandteil einer antiretroviralen Therapie (ART) bei Infektion mit dem Humanen Immundefizienz-Virus (HIV). Die Wirkstoffe werden anhand ihrer strukturellen Eigenschaften und Zielstrukturen, die sie adressieren, klassifiziert.
Anwendung
HIV-Therapeutika werden innerhalb der sogenannten antiretroviralen Therapie (ART), auch hochaktive antiretrovirale Therapie, kurz HAART (highly active antiretroviral therapy) eingesetzt bei Infektionen mit dem Humanen Immundefizienz-Virus (HIV) sowie zur Prä- und Postexpositionsprophylaxe einer HIV-Infektion.
Darüber hinaus werden HIV-Therapeutika auch bei Infektionen mit dem Hepatitis B Virus (HBV) angewendet.
HIV wird unterschieden in HIV-1 (weltweit) und HIV-2 (vorwiegend in Westafrika), die sich wiederum in weitere Subtypen gliedern lassen. Im Allgemeinen bezieht sich die Anwendung auf Infektionen mit HIV-1.
Wirkung
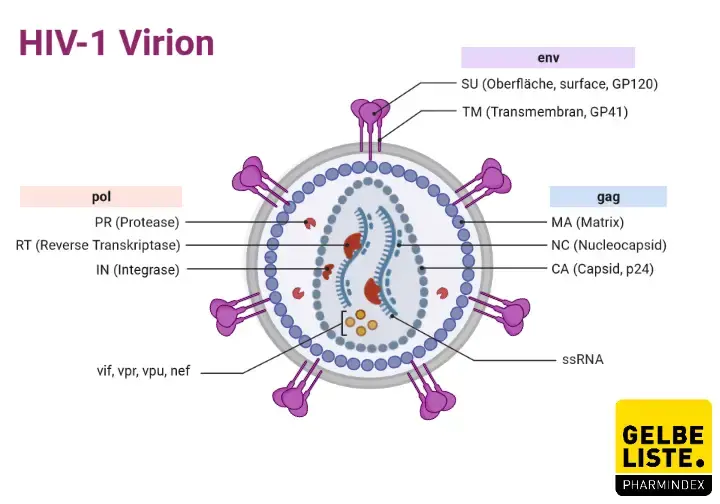
Humane Immundefizienz-Viren sind lymphotrope Lentiviren aus der Familie der Retroviren. Jedes individuelle Viruspartikel enthält zwei RNA-Stränge, die von einem Capsid-Protein (p24) und einer Lipidmembran mit Hüllproteinen (gp120, gp41) umschlossen sind. Das Oberflächenprotein gp120 befähigt das HI-Virus, sich an das Oberflächenprotein CD4 der Zielzelle (überwiegend T-Helferzellen, aber auch Makrophagen) zu heften und unter Beteiligung von Korezeptoren (CCR5, CXCR4) auf der Zielzelle mit dieser zu fusionieren.

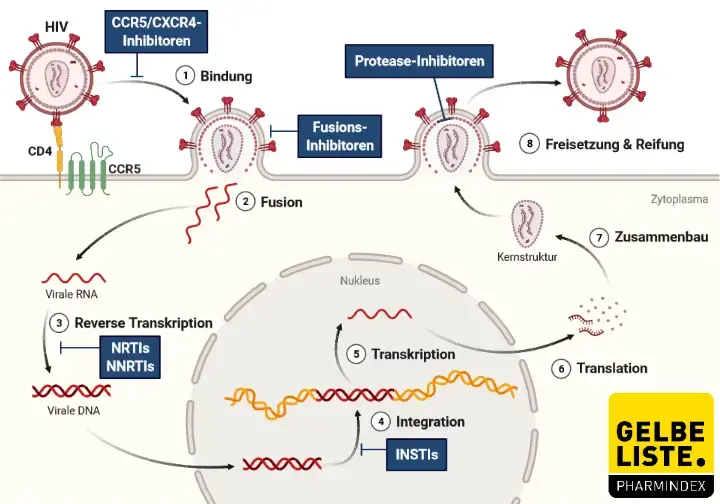
Diese Interaktion zwischen HI-Virus und Zielzelle liefert erste Angriffspunkte für antiretrovirale Wirkstoffe, die sogenannten Entry-Inhibitoren:
Reverse Transkriptase
Nach Eintritt in die Zielzelle wird mit Hilfe des viruseigenen Enzyms Reverse Transkriptase (RT) die virale RNA in provirale DNA umgeschrieben. Das Enzym RT dient in diesem Fall als weiterer Angriffspunkt für antiretrovirale Wirkstoffe, die sogenannten Reverse-Transkriptase-Inhibitoren (RTI).
RTI unterscheiden sich in ihrer chemischen Struktur und werden deshalb unterteilt in:
- Nukleosidische Reverse-Transkriptase-Inhibitoren (NRTI): Abacavir, Didanosin, Emtricitabin, Lamivudin, Stavudin, Zidovudin
- Nukleotidanaloge Reverse-Transkriptase-Inhibitoren (NtRTI): Tenofovir, Adefovir
- Nicht-nukleosidische Reverse-Transkriptase-Inhibitoren (NNRTI): Doravirin, Efavirenz, Etravirin, Nevirapin, Rilpivirin
Bei RTI handelt es sich in der Regel (Ausnahme NNRTI) um Prodrugs, da sie erst nach Phosphorylierung durch zelluläre Kinasen in ihre aktiven Wirkformen, die Nukleosid-Triphosphate (NTP), umgewandelt werden.
Darüber hinaus wirken RTI auch bei Infektionen mit dem Hepatitis B Virus, obwohl es sich bei HBV um ein DNA-Virus und nicht um ein Retrovirus (RNA-Virus) handelt. Hepatitis B Viren haben einen besonderen Replikationsmechanismus, denn die Replikation der DNA erfolgt im Zytosol unter Verwendung der mRNA als Vorlage für die viruseigene Polymerase, die sowohl eine Reverse Transkriptase- als auch eine RNAse-H-Aktivität besitzt. Aus diesem Grund sind RTI auch bei HBV-Infektionen wirksam.
Integrase
Die provirale DNA wird nach Transport in den Nukleus durch eine virale Integrase in das Wirtsgenom integriert, sodass prinzipiell jede infizierte Zelle während ihrer gesamten Lebensdauer neue Viruspartikel generieren kann. Die virale Integrase dient als Angriffspunkt für die sogenannten Integrase-Inhibitoren (Raltegravir, Dolutegravir, Elvitegravir, Bictegravir).
HIV-Protease
Um neue (funktionelle) Virusproteine herzustellen, benötigt das HI-Virus zusätzlich die HIV-Protease, die aus hochmolekularen Vorläuferproteinen die notwendigen Virusproteine abspaltet. Dieser Prozess kann durch die sogenannten HIV-Protease-Inhibitoren (Atazanavir, Darunavir, Fosamprenavir, Indinavir, Lopinavir, Ritonavir, Saquinavir, Tipranavir) gehemmt werden.
Nebenwirkungen
Das Nebenwirkungsprofil variiert je nach Wirkstoff:
Typisch für nicht-nukleosidische Reverse-Transkriptase-Inhibitoren NNRTI sind Hautausschläge.
Unter nukleosidischen Reverse-Transkriptase-Inhibitoren (NRTI) können folgende gruppentypische (Langzeit-)Nebenwirkungen auftreten, die vorwiegend mit der Hemmung der mitochondrialen DNA-Polymerase γ in Verbindung gebracht werden (mitochondriale Toxizität):
- Laktatazidose
- Hepatotoxizität
- Myelotoxizität
- Polyneuropathie
- Lipoatrophie
Die mitochondriale Toxizität ist in Abhängigkeit vom Wirkstoff unterschiedlich stark ausgeprägt, wobei das höchste Risiko unter Stavudin und Didanosin vorliegt. Aufgrund einer hohen Selektivität für virale DNA-Polymerasen (HIV und HBV) zeichnen sich Emtricitabin und Lamivudin durch eine eher geringe Toxizität aus.
Zu Beginn einer Therapie mit HIV-Protease-Inhibitoren können vermehrt gastrointestinale Störungen (z.B. sekretorische Diarrhö) auftreten. Zusätzlich sind diese Nebenwirkungen charakteristisch für einige Protease-Inhibitoren:
- Lipidstoffwechselstörungen (Dyslipidämie) und Lipodystrophie
- Hautreaktionen
- Geschmacksstörungen (Ritonavir und Indinavir)
- Nephrolithiasis (Indinavir)
- Transaminaseanstieg (Tipranavir)
- QT-Zeit-Verlängerung (Saquinavir)
Wechselwirkungen
Eine antiretrovirale Therapie sollte immer aus einer Kombination mehrerer Wirkstoffe bestehen, wodurch sich allerdings auch das Wechselwirkungsrisiko erhöht. Die potenziellen Wechselwirkungen können wirkstoffspezifisch variieren, wobei es einige gruppentypische Wechselwirkungen zu berücksichtigen gilt.
Nukleosid- und Nukleotid-Analoga
Nukleosid- bzw. Nukleotid-Analoga werden größtenteils renal eliminiert, sodass sich bei der gleichzeitigen Anwendung von Arzneimitteln, die durch aktive tubuläre Sekretion ausgeschieden werden, die Serumkonzentration der betroffenen Analoga oder dem gleichzeitig angewendeten Arzneimittel erhöhen kann (wegen der Konkurrenz um diesen Eliminationsweg).
Nicht-nukleosidische Reverse-Transkriptase-Inhibitoren (NNRTI)
Bei einigen NNRTI (z.B. Efavirenz und Nevirapin) sind Wechselwirkungen mit CYP-Enzymen (vor allem CYP3A4) zu beachten
Protease-Inhibitoren
HIV-Protease-Inhibitoren sind bekannt für ihre CYP3A4-inhibierenden Eigenschaften, was ihren Einsatz bei multimorbiden Patienten erschwert. Diese Eigenschaft wird wiederum genutzt (siehe Ritonavir), um beispielsweise andere Wirkstoffe zu „boostern“, indem deren Abbau inhibiert bzw. verzögert wird. Darüber hinaus fördern CYP3A4-Induktoren den Abbau von PI während CYP3A4-Inhibitoren ihn hemmen.
Integrase-Inhibitoren (INI)
Polyvalente Kationen vermindern durch Chelatisierung die Resorption von Integrase-Inhibitoren, was durch ausreichend zeitlichen Abstand zwischen den Einnahmen verhindert werden kann.
Inhibitoren (z.B. Atazanavir) oder Induktoren (z.B. Rifampicin) von UGT1A1 erhöhen bzw. erniedrigen die Plasmaspiegel einiger INI.
Wirkstoffspezifische Wechselwirkungen können in den zugehörigen Wirkstoffprofilen oder der jeweiligen Fachinformation nachgelesen werden.
Kontraindikation
Bei Überempfindlichkeit gegen den jeweiligen Wirkstoff oder sonstige Bestandteile des Arzneimittels ist die Anwendung kontraindiziert. Weitere wirkstoffspezifische Kontraindikationen können der jeweiligen Fachinformation entnommen werden.
Wirkstoffe
Zur antiretroviralen Therapie (einer HIV-1-Infektion) können folgende Wirkstoffe eingesetzt werden:
Entry-Inhibitoren
Nukleosidische Reverse-Transkriptase-Inhibitoren (NRTI)
Nukleotidische Reverse-Transkriptase-Inhibitoren (NtRTI)
Nicht-nukleosidische Reverse-Transkriptase-Inhibitoren (NNRTI)
Integrase-Inhibitoren (INI, INSTI)
HIV-Protease-Inhibitoren (PI)
Hinweise
Kombinationstherapie
- Generell ist zu beachten, dass die antiretrovirale Therapie immer aus einer Kombination mehrerer antiretroviraler Wirkstoffe bestehen sollte, um in erster Linie Resistenzen zu minimieren und synergistische Wirkungen zu erzielen. Allerdings dürfen nicht alle antiretroviralen Wirkstoffe bedenkenlos kombiniert werden.
- Nicht alle antiretroviralen Wirkstoffe dürfen bedenkenlos kombiniert werden.
Opportunistische Infektionen
- Patienten, die eine antiretrovirale Therapie erhalten, können dennoch opportunistische Infektionen und sonstige Komplikationen einer HIV-Infektion entwickeln.
- Deshalb ist auch weiterhin eine engmaschige klinische Überwachung durch Ärzte erforderlich, die in der Behandlung von Patienten mit Begleiterkrankungen einer HIV-Infektion erfahren sind.
HIV-Übertragung
- Obwohl gezeigt wurde, dass die erfolgreiche Virussuppression durch eine antiretrovirale Therapie das Risiko einer sexuellen Übertragung erheblich reduziert, kann ein Restrisiko nicht ausgeschlossen werden.
- Demnach sollten Vorsichtsmaßnahmen zur Vermeidung der Übertragung gemäß nationaler Leitlinien getroffen werden.